
��1��ij��ȤС������������װ�úͷ����ⶨ������SO2����������Ϊ���еIJ����� ������ţ�
|
��� |
A |
B |
C |
|
װ�� |
|
|
|
|
ԭ�� |
ͨ��V���������ⶨ���ɳ��������� |
��KMnO4��Һ�պ���ɫʱ���ⶨͨ����������V |
ͨ��V���������ⶨU�����ӵ����� |
��2����ȤС����ȡ336mL����״����ij��SO2��N2��ɵĻ������Y,����ͨ��������ˮ�У�Ȼ���������BaCl2��Һ�����ʵ�������ø������2��33g���ɴ���֪����Y��SO2���������Ϊ ��
��ij��ѧ��ȤС���Ϊ̽��Fe3+�Ƿ�������SO2�����������ʵ��װ�á�
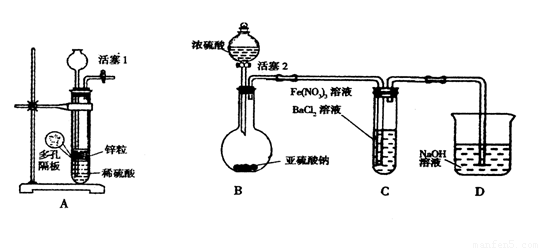
��1������ͼ���Ӻ�װ�á�ʵ��ǰӦ���� ����
��2���۲쵽װ��C�в����˰�ɫ������ͬѧ����������²��루ÿ������ֻ����һ�����ʵ������ԣ���
����1�� ��
����2��SO2��Fe3+�����ˣ�
����3��SO2��NO3��������
��3����ͬѧ��Ϊ����1��ȷ������������װ��A�������ų����ŵ�̽��ʵ�顣
��4����ͬѧ��Ϊ����2��ȷ����װ��C�з�Ӧ�����ӷ���ʽ��
��5����ͬѧ��Ϊ����3��ȷ�������ü�ͬѧ��ʵ��װ�ã����ʵ����֤���롣���ڴ����д��ʵ�鲽���Լ�Ԥ������ͽ��ۡ���ѡʵ���Լ���NaNO3��Һ��KSCN��Һ��FeCl3��Һ��BaCl2��Һ��
|
ʵ�鲽�� |
Ԥ������ͽ��� |
|
|
|
Fe(NO3)3��Һ
��1��B ��2��66��7��
��1�����װ�õ������� ��2��������SO2����H2O�У�������H2SO4
��4��SO2 + 2Fe3+ + Ba2+ + 2H2O=BaSO4��+ 2Fe2+ + 4H+
��5��
|
ʵ�鲽�� |
Ԥ������ͽ��� |
|
��װ��C�е���Һ��ΪNaNO3 ��BaCl2�Ļ����Һ�� Ȼ���Һ©���������з�Ӧ
|
��Ӧһ��ʱ�����C�г��ְ�ɫ��������֤������3��ȷ |
��������
�����������1��A��ͨ������������岻�����ɳ������ʴ���B�ж������������ط�Ӧ���������������ɫ��ɫ�����Լ�⣬��ȷ�������к��ж�����̼Ҳ�����ʯ�ҷ�Ӧ������2����ȤС����ȡ336mL����״����ij��SO2��N2��ɵĻ������Y,����ͨ��������ˮ�У�Ȼ���������BaCl2��Һ�����ʵ�������ø������2��33g���ɴ���֪����Y��SO2���������ΪSO2���л�ԭ�ԣ�ͨ��������ˮ�У�����SO2+Br2+2H2O=2HBr+H2SO4�����ӷ���ʽ����д���������е�����������������ӣ��������ӷ���ʽΪSO2+Br2+2H2O�T2Br-+SO42-+4H+�����ɵ����������Ȼ����������ɫ������������ϴ��Ȼ���ٹ�������ô��������ᱵ��������n��������壩=0��336L/22��4=0��015mol��
 �� SO2�����������0��01/0��015=66��7������1������ͼ���Ӻ�װ�á�ʵ��ǰӦ��������װ�õ������� ������
�� SO2�����������0��01/0��015=66��7������1������ͼ���Ӻ�װ�á�ʵ��ǰӦ��������װ�õ������� ������
��2�����ݿɻ��SO2����Ϊ��6�۵����п����ǿ����е��������ʲ���1����������SO2����H2O�У�������H2SO4��
��3����ͬѧ��Ϊ����1��ȷ������������װ��A�������ų����ŵ�̽��ʵ�顣
��4������������ԭ��Ӧԭ��������������������ǿ�������ܰѶ�������ת��Ϊ��������ӣ���װ��C�з�Ӧ�����ӷ���ʽ��SO2 + 2Fe3+ + Ba2+ + 2H2O=BaSO4��+ 2Fe2+ + 4H+ ��
��5��ֻҪ�����������Ӳ�Ҫ���������ͻ������ž��У��ʿ�ѡʵ���Լ���NaNO3��ҺBaCl2��Һ����ʵ�飬��װ��C�е���Һ��ΪNaNO3 ��BaCl2�Ļ����Һ��Ȼ���Һ©���������з�Ӧ����Ӧһ��ʱ�����C�г��ְ�ɫ��������֤������3��ȷ��
���㣺���⿼�������仯���������ʵ�飬�����صĻ�ѧ��Ӧԭ���ǽ��Ĺؼ��������Ѷ��еȡ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ԭ����ǻ�ѧ�������һ���ش��ף�
ԭ����ǻ�ѧ�������һ���ش��ף��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
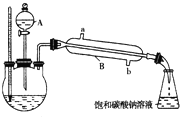 ��֪�����ʾ���ݣ�
��֪�����ʾ���ݣ�| ���� | �۵㣨�棩 | �е㣨�棩 | �ܶȣ�g?cm-3�� |
| �Ҵ� | -117.3 | 78.5 | 0.79 |
| ���� | 16.6 | 117.9 | 1.05 |
| �������� | -83.6 | 77.5 | 0.90 |
| Ũ���� | - | 338.0 | 1.84 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2011-2012ѧ�걱���г�������һ��ѧ����ĩͳһ���Ի�ѧ�Ծ����������� ���ͣ�ʵ����
��10�֣�ԭ����ǻ�ѧ�������һ���ش��ס�
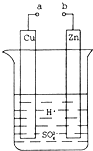
��1��ij��ȤС��Ϊ�о�ԭ���ԭ���������ͼװ�á�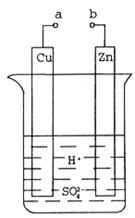
��a��b������ʱ���ձ��з�����Ӧ�����ӷ���ʽ��__________��
��a��b�õ������ӣ�Cu��Ϊԭ���__________������������������缫��Ӧʽ��__________��Zn������__________�����������ԭ������Ӧ����Һ��H������__________���Cu����Zn��������
������a��b�Ƿ����ӣ�ZnƬ������ʴ����ת����0.2mol���ӣ���������ZnƬ����������__________g��
��2����ͬѧ���Ba(OH)2?8H2O������NH4Cl����ķ�Ӧ��Ƴ�ԭ��أ�����Ϊ�Ƿ���У�________����ǡ�����������__________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014ѧ��㶫ʡ��ɽ�и���һģ���ۻ�ѧ�Ծ��������棩 ���ͣ������
����β����NOx�����������������������㷺��ע��
��1��ij��ȤС����������������Ϣ��
N2(g)+O2(g)=2NO(g) ��H=+180.5kJ/mol
2H2(g)+O2(g)=2H2O(g)) ��H=�D483.6kJ/mol
��Ӧ2H2(g)+2NO(g)=2H2O(g)+N2(g) ��H= ��
��2����С�����õ��ԭ���������ͼ1װ�ý���H2��ԭNO��ʵ��[�����ӵ����Ե�SCY�մ�(�ܴ���H+)Ϊ���ʣ������ٱ�Ĥ���缫]��
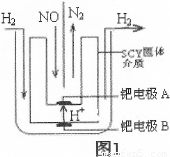
�ٵ缫AΪ �����缫��ӦʽΪ ��
��3����������ԭNOԭ�����£�
����Ӧ��4NO(g)+4NH3(g)+O2(g)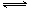 4N2(g)+6H2O(g)
(��H <0)
4N2(g)+6H2O(g)
(��H <0)
����Ӧ��4NH3(g)+3O2(g)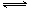 2N2(g)+6H2O(g)
2N2(g)+6H2O(g)
4NH3(g)+ 4O2(g)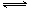 2N2O(g)+6H2O(g)
2N2O(g)+6H2O(g)
4NO(g)+4NH3(g)+3O2(g) 4N2O(g)+6H2O(g)
4N2O(g)+6H2O(g)
�й�ʵ�������ͼ2��ͼ3��ʾ���ݴ˻ش��������⣺

�ٴ���ԭNOӦ����n(NH3)/n(NO)�����ֵΪ �������� ��
������Ӧƽ�ⳣ������ʽ��K= �������¶ȵ����ӣ�K�� (ѡ����ӡ��� ����С�����䡱��
��Ӱ��N2O�����ʵ������� ������Ũ�Ⱥ� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014�챱���г�������һ��ѧ����ĩͳһ���Ի�ѧ�Ծ��������棩 ���ͣ�ʵ����
��10�֣�ԭ����ǻ�ѧ�������һ���ش��ס�
��1��ij��ȤС��Ϊ�о�ԭ���ԭ���������ͼװ�á�
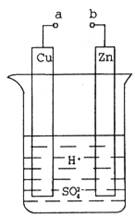
��a��b������ʱ���ձ��з�����Ӧ�����ӷ���ʽ��__________��
��a��b�õ������ӣ�Cu��Ϊԭ���__________������������������缫��Ӧʽ��__________��Zn������__________�����������ԭ������Ӧ����Һ��H������__________���Cu����Zn��������
������a��b�Ƿ����ӣ�ZnƬ������ʴ����ת����0.2mol���ӣ���������ZnƬ����������__________g��
��2����ͬѧ���Ba(OH)2•8H2O������NH4Cl����ķ�Ӧ��Ƴ�ԭ��أ�����Ϊ�Ƿ���У�________����ǡ�����������__________��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com