
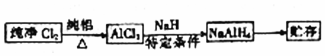
分析 (1)铝氢化钠遇水发生剧烈反应产生偏铝酸钠和氢气,根据反应放热和氢气爆炸分析;
(2)A装置制取氯气,B装置用饱和食盐水吸收氯化氢气体,C中装置有浓硫酸干燥氯气,D装置中是氯气与铝在加热条件下生成氯化铝,反应的尾气是氯气会污染空气,所以E装置中用碱石灰吸收氯气尾气,且吸收空气中的水蒸气,实验时应先在装置中通一会儿氯气,将装置中的空气排尽,以除去装置中的水分,
①氯化铝易遇水反应过量的氯气污染空气,据此分析;
②氯气充满装置即为排尽空气;
(3)①金属钠和氢气之间化合可以得NaH,但是氢气中的氯化氢要除去,选择氢氧化钠溶液;
②金属钠和氧气加热下会产生过氧化钠杂质;
(4)由反应原理得,测定铝氢化钠样品的纯度即通过测定铝氢化钠与水反应生成的氢气的量计算铝氢化钠的量,从而计算其纯度.
解答 解:(1)铝氢化钠遇水发生剧烈反应产生偏铝酸钠和氢气,其反应的化学方程式为NaAlH4+2H2O=NaAlO2+4H2↑,反应放出大量热量使生成的H2迅速膨胀而爆炸;
故答案为:反应放出大量热量使生成的H2迅速膨胀而爆炸;NaAlH4+2H2O=NaAlO2+4H2↑;
(2)①氯气污染空气,同时由题氯化铝易与水反应,E装置中的碱石灰吸收剩余的氯气并避免空气中的水蒸气进入D中;
故答案为:吸收剩余的氯气并避免空气中的水蒸气进入D中;
②点燃装置D处酒精灯之前,先将装置A中的分液漏斗打开,反应一段时间,使D中玻璃管充满黄绿色体,排尽装置内的空气;
故答案为:先将装置A中的分液漏斗打开,反应一段时间,使D中玻璃管充满黄绿色体;
(3)①金属钠和氢气之间化合可以得NaH,A中由金属与盐酸制备氢气,生成的氢气中氯化氢应用碱性试剂除去,如氢氧化钠,则B中试剂为NaOH溶液;
故答案为:NaOH溶液;
②金属钠和氧气加热下会产生过氧化钠杂质以及过量的Na;
故答案为:Na2O2(或Na等其他合理答案);
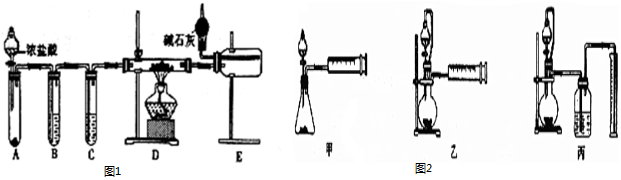
(4)由反应原理得,测定铝氢化钠样品的纯度即通过测定铝氢化钠与水反应生成的氢气的量计算铝氢化钠的量,从而计算其纯度,所以从简约性、准确性考虑,最甲没有使用恒压漏斗,测出的氢气有误差;C、D采用排水法收集氢气,由于导管中会有残留,导致测出的氢气有误差,适宜的方案是乙;通过连续两次读数的氢气体积相等,说明铝氢化钠与水完全反应,冷却至室温;
故答案为:乙;连续两次读数的氢气体积相等.
点评 本题考查知识点较多,涉及方程式的书写、装置图的选择、物质的制备和除杂等元素化合物的性质,属于拼合型题目,需要学生具备扎实的基础,难度中等.


 寒假乐园北京教育出版社系列答案
寒假乐园北京教育出版社系列答案科目:高中化学 来源: 题型:解答题
| 实验编号 | 操作 | 现象 | 实验结论 |
| 1 | 取少量黑色固体于试管,加入足量氨水,振荡 | 黑色固体不溶解 | 假设1成立 |
| 2 | 操作同实验1 | 黑色固体完全溶解 | 假设2成立 |
| 3 | ①取少量黑色固体于试管中,加入适量氨水,振荡,静置,取上层清液于洁净试管中,加入几滴乙醛,水浴加热②取少量黑色固体于试管中,加入足量稀硝酸,振荡 | ①试管内壁有银镜生成 ②固态完全溶解,并有气体产生 | 假设3成立 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 钠硫电池以熔融金属钠、熔融硫和多硫化钠(Na2Sx)分别作为两个电极的反应物,固体Al2O3陶瓷(可传导Na+)为电解质,电池反应为:2Na+xS═Na2Sx,电池结构如图所示.下列说法不正确的是( )
钠硫电池以熔融金属钠、熔融硫和多硫化钠(Na2Sx)分别作为两个电极的反应物,固体Al2O3陶瓷(可传导Na+)为电解质,电池反应为:2Na+xS═Na2Sx,电池结构如图所示.下列说法不正确的是( )| A. | 放电时,Na作负极,反应式为Na-e-=Na+ | |
| B. | 钠硫电池在常温下也能正常工作 | |
| C. | 放电时Na+向正极移动 | |
| D. | 当外电路通过0.25mol电子时消耗16g硫,则x=4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | A | B | C | D |
| 关系 |  包含关系 | 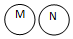 并列关系 | 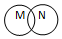 交集关系 | 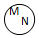 重叠关系 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 100g质量分数为46%的酒精水溶液中的氧原子数为4NA | |
| B. | 500mL 2mol/L碳酸钠溶液中的阴离子数小于NA | |
| C. | 合成氨反应中催化剂降低了反应的活化能,增大了反应的焓变 | |
| D. | 据“△H-T•△S<0”判断某反应能自发,可知该反应一定能发生 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
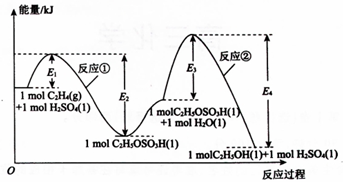 乙烯间接水合法合成乙醇分两步完成,反应过程中的能量变化如图所示,对于在密闭容器中进行的合成反应,下列说法不正确的是( )
乙烯间接水合法合成乙醇分两步完成,反应过程中的能量变化如图所示,对于在密闭容器中进行的合成反应,下列说法不正确的是( )| A. | H2SO4是乙烯间接水合法合成乙醇的催化剂 | |
| B. | 缩小容器容积,乙烯的转化率增大 | |
| C. | 反应①和反应②均为放热反应 | |
| D. | 反应②的反应热△H=-(E3-E4)kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
| 碳 | 氮 | Y | |
| X | 硫 | Z |
 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com