
【题目】回答问题
(1)电解池就是把能转化能的装置
(2)常温下KW数值= .
(3)常温下,某溶液中的c(H+)=5.0×10﹣7 molL﹣1 , 则此时c(OH﹣)=molL﹣1 .
【答案】
(1)电;化学
(2)1×10﹣14
(3)2.0×10﹣8
【解析】解:(1)电解池是将电能转化为化学能的装置;所以答案是:电能;化学能;(2)常温下水的离子积常数是一个定值,KW=1×10﹣14;所以答案是:1×10﹣14;(3)常温下,水的离子积常Kw=c(H+)c(OH﹣)=1×10﹣14;所以c(OH﹣)= ![]() =
= ![]() =2.0×10﹣8 , 所以答案是:2.0×10﹣8 .
=2.0×10﹣8 , 所以答案是:2.0×10﹣8 .
【考点精析】关于本题考查的离子积常数,需要了解水的离子积Kw=c(H+)·c(OH–)=10–14(25℃)①Kw只与温度有关,温度升高,Kw增大;如:100℃ Kw=10–12②Kw适用于纯水或稀酸、稀碱、稀盐水溶液中才能得出正确答案.


 百年学典课时学练测系列答案
百年学典课时学练测系列答案科目:高中化学 来源: 题型:
【题目】100mL 2.0 molL﹣1 的碳酸钠溶液和200mL盐酸,不管将前者滴加入后者,还是将后者滴加入前者,最终都有气体产生,但生成的气体体积不同,下列选项中盐酸的浓度合理的是( )
A.2.0 molL﹣1
B.1.5 molL﹣1
C.1 molL﹣1
D.0.5 molL﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】含有弱酸HA和其钠盐NaA的混合溶液,在化学上用作缓冲溶液.向其中加入少量酸或碱时,溶液的酸碱性变化不大.
(1)向该溶液中加入少量盐酸时,发生反应的离子方程式是 , 向其中加入少量KOH溶液时,发生反应的离子方程式是;
(2)现将0.04molL﹣1HA溶液和0.02molL﹣1NaOH溶液等体积混合,得到缓冲溶液.
①若HA为HCN,该溶液显碱性,则溶液中c(Na+)c(CN﹣)(填“<”、“=”或“>”),你得出该结论的依据是;该混合溶液的质子守恒式是 .
②若HA为CH3COOH,该溶液显酸性.溶液中所有的离子按浓度由大到小排列的顺序是 . 该混合溶液的物料守恒式是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CuSO4溶液与K2C2O4溶液混合反应,产物之一是某种只含一种阴离子的蓝色钾盐水合物.通过下述实验确定该晶体的组成.
步骤a:称取0.6720g样品,放入锥形瓶,加入适量2molL﹣1稀硫酸,微热使样品溶解.再加入30mL水加热,用0.2000molL﹣1 KMnO4溶液滴定至终点,消耗8.00mLKMnO4溶液.
步骤b:接着将溶液充分加热,使淡紫红色消失,溶液最终呈现蓝色.冷却后,调节pH并加入过量的KI固体,溶液变为棕色并产生白色沉淀CuI.用0.2500molL﹣1 Na2S2O3标准溶液滴定至终点,消耗8.00mLNa2S2O3溶液.
已知涉及的部分反应的离子方程式为:
步骤a:2MnO4﹣+5C2O42﹣+16H+=2Mn2++8H2O+10CO2↑
步骤b:2Cu2++4I﹣=2CuI↓+I2 I2+2S2O32﹣=2I﹣+S4O62﹣
(1)已知室温下CuI的Ksp=1.27×10﹣12 , 欲使溶液中c(Cu+)≤1.0×10﹣6molL﹣1 , 应保持溶液中c(I﹣)≥molL﹣1 .
(2)MnO4﹣在酸性条件下,加热能分解为O2 , 同时生成Mn2+ .
写出该反应的离子方程式为 .
若无此加热操作,则测定的Cu2+的含量将会(填“偏高”、“偏低”或“不变”).
(3)步骤b用淀粉溶液做指示剂,则滴定终点观察到的现象为 .
(4)通过计算确定样品晶体的组成.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中,氧化剂与还原剂物质的量之比为1:2的是( )
A.3S+6NaOH═2Na2S+Na2SO3+3H2O
B.2CH3COOH+Ca(ClO)2═2HClO+Ca(CH3COO)2
C.I2+2NaClO3═2NaIO3+Cl2
D.4HCl(浓)+MnO2 ![]() MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示的原电池装置,X,Y为两个电极,电解质溶液为稀硫酸,外电路中的电子流向如图所示,对此装置的下列叙述正确的是( ) 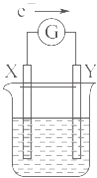
A.外电路中的电流方向为:X→外电路→Y
B.若两个电极分别为Zn和碳棒,则X为碳棒,Y为Zn
C.若两个电极都是金属,则它们的活动性为X>Y
D.X极上发生的是还原反应,Y极上发生的是氧化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲、乙、丙三位同学分别做了以下三个实验.
实验一:草酸晶体(H2C2O4)和浓硫酸混合缓慢加热时,可发生如下反应:H2C2O4=CO2↑+CO↑+H2O.甲同学设计了如图1实验装置,用来制取干燥纯净的CO气体,并用生成的CO气体还原FexOy , 制取铁粉.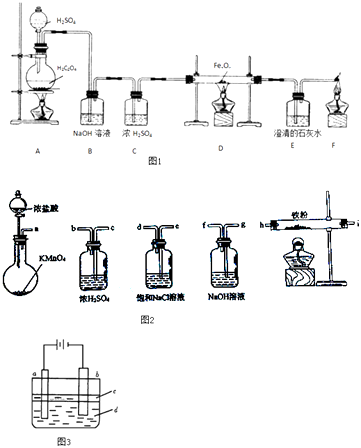
(1)装置B的作用是 . 装置E中的现象是 . 装置F的作用是 .
(2)若FexOy为0.4g,生成的气体与过量澄清石灰水反应生成0.75g白色沉淀,则FexOy的化学式为 .
实验二:乙同学用如图2所示仪器在实验室制备少量无水FeCl3 , 按气流由左到右顺序,仪器连接顺序的是 .
实验三:丙同学用如图3实验装置可制得纯净的Fe(OH)2沉淀.两极材料分别为石墨和铁.
①a电极材料为 , 其电极反应式为 .
②液体c为苯,其作用是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据题意解答
(1)某容器中发生了一个化学反应,反应过程中存在H2O、ClO﹣、CN﹣、HCO3﹣、N2、Cl﹣六种粒子,在反应过程中测得ClO﹣和N2的物质的量随时间变化的曲线如图所示. 
该反应的离子方程式是 .
(2)氮氧化合物是大气污染的重要盐因素,将NOx转化为无害物质是当前研究的重要课题.
①下式中X必须为无污染的物质,系数n可以为0.
NO2+G ![]() N2+H2O+nX(未配平的反应式).
N2+H2O+nX(未配平的反应式).
下列化合物中,满足上述反应式中的G是(填写字母).
a.NH3 b.CO2 c.SO2 d.CH3CH2OH
②若G为天然气的主要成分,则X为 , n= .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com