
| A、C2H2 |
| B、CO2 |
| C、NH3 |
| D、BF3 |
 课堂练加测系列答案
课堂练加测系列答案 轻松课堂单元测试AB卷系列答案
轻松课堂单元测试AB卷系列答案科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氯气通入水中H2O+Cl2═2H++Cl-+ClO- |
| B、氯化铁溶液中加入铁粉2Fe3++Fe═3Fe2+ |
| C、碳酸钙加入盐酸中 C032-+2H+=CO2↑+H2O |
| D、铜片加入稀硝酸中Cu+2 H+=Cu2++H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:
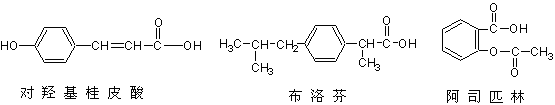
 )和阿司匹林有相似的结构,它的一种制备方法如下
)和阿司匹林有相似的结构,它的一种制备方法如下
 与足量的氢溴酸在加热条件下反应的化学方程式为
与足量的氢溴酸在加热条件下反应的化学方程式为查看答案和解析>>
科目:高中化学 来源: 题型:



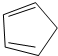 与CH≡CH(乙炔)也能发生Diels-Alder反应,请写出该反应产物的结构简式
与CH≡CH(乙炔)也能发生Diels-Alder反应,请写出该反应产物的结构简式查看答案和解析>>
科目:高中化学 来源: 题型:

| 氢氧化物 | Fe(OH)3 | Al(OH)3 | Mg(OH)2 |
| 开始沉淀的PH值 | 1.5 | 3.3 | 9.4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com