
等物质的量的下列物质①甲醇(CH3OH) ②乙醇(CH3CH2OH) ③乙二醇(![]() ) ④丙三醇(
) ④丙三醇(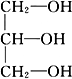 ),用物质的编号填空:
),用物质的编号填空:
(1)在空气中完全燃烧时,消耗氧气的质量由多到少的顺序________,反应中生成CO2的体积(相同状况)由小到大的顺序________.
(2)分别与足量的金属钠反应,放出H2的体积(相同状况)由少到多的顺序是________.
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
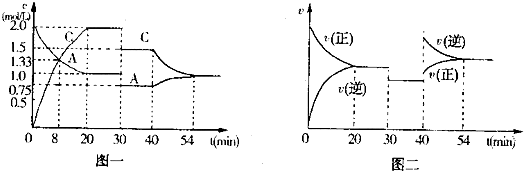
查看答案和解析>>
科目:高中化学 来源: 题型:
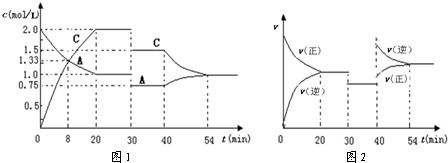
| A、0~20min用A物质表示反应的平均速率为0.05mol?L-1?min-1 | B、该反应的正反应为吸热反应 | C、x=1,且30min时改变的反应条件是减压 | D、在25min、35min、55min时化学平衡常数分别为K1、K2、K3,则K3>K2>K1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com