
海水中有取之不尽的化学资源,从海水中可提取多种化工原料,下图是某工厂对海水资源的综合利用的示意图:
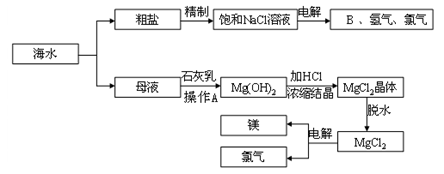
回答下列问题:
(1)操作A的实验名称为: ,B的化学式为
(2)镁是活泼的金属,能在二氧化碳中燃烧,反应方程式为:
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
下列有关实验操作、现象和解释或结论都正确的是( )
| 选项 | 操 作 | 现 象 | 解释或结论 |
| A | 过量的Fe粉中加入稀HNO3,充分反应后,滴加KSCN溶液 | 溶液呈红色 | 稀HNO3将Fe氧化为Fe3+ |
| B | Al箔插入稀HNO3中 | 无现象 | Al箔表面被稀HNO3氧化,形成致密的氧化膜 |
| C | 向某溶液中滴加浓NaOH溶液,将湿润红色石蕊试纸置于试管口 | 试纸变蓝 | 该溶液中存在NH4+ |
| D | 向紫色石蕊试液中通入SO2 | 溶液褪色 | SO2有漂白性 |
查看答案和解析>>
科目:高中化学 来源: 题型:
氯气是一种重要的化工原料。某学习小组在实验室中利用下图所示装置制取氯气并探究其性质。
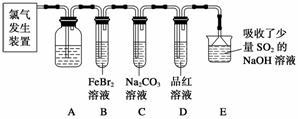
(1)实验室用二氧化锰和浓盐酸加热制取氯气,该反应的离子方程式为____________________________________________________________。
(2)装置A中盛有的试剂是饱和NaCl溶液,作用是_______________________________。
(3)若D中品红溶液褪色,则B装置中发生反应的离子方程式是_____________________________________________________________。
某研究性学习小组用刚吸收过少量SO2的NaOH溶液吸收处理上述实验后的尾气。经分析吸收尾气一段时间后,吸收液(呈强碱性)中肯定存在Cl-、OH-、CO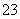 和SO
和SO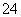 ,对于可能存在的其他阴离子,研究小组提出以下3种假设。
,对于可能存在的其他阴离子,研究小组提出以下3种假设。
假设1:只存在SO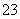 ; 假设2:只存在ClO-;假设3:既不存在SO
; 假设2:只存在ClO-;假设3:既不存在SO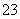 ,也不存在ClO-。
,也不存在ClO-。
(4)学习小组判断同时存在SO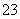 和ClO-是不可能的理由是_____________________。
和ClO-是不可能的理由是_____________________。
(5)现限选以下试剂,设计实验方案,进行实验,请写出实验步骤以及预期现象和结论。
a.3 mol·L-1 H2SO4 b.酸性KMnO4溶液 c.1 mol·L-1 BaCl2溶液
d.FeCl2溶液 e.酚酞试液
步骤一:取少量吸收液于试管中,滴加3 mol·L-1 H2SO4至溶液呈中性,然后将所得溶液分装于F、G两试管中。
步骤二:向F试管中滴加少量__________(填序号),若溶液____________________(填现象),则假设1成立。
步骤三:向G试管中滴加少量d溶液,生成红褐色沉淀,假设2成立,则反应的离子方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
关于Na2CO3和NaHCO3性质的说法不正确的是
A.热稳定性:NaHCO3<Na2CO3
B.与同浓度盐酸反应的剧烈程度:NaHCO3<Na2CO3
C. 相同温度时,在水中的溶解性:NaHCO3<Na2CO3
D. 等物质的量的Na2CO3、NaHCO3分别与足量盐酸反应产生的CO2质量相同
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子方程式的书写正确的是
A.金属铁溶于盐酸中:2Fe+6H+=2Fe3++3H2↑
B.实验室用大理石和稀盐酸制取CO2:2H++CO32- = CO2↑+H2O
C.向AlCl3溶液中加入过量的氨水:Al3++3OH-= Al(OH)3↓
D.MnO2固体和浓盐酸反应制氯气:MnO2+4H++2Cl- 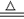 Mn2++Cl2↑+2H2O
Mn2++Cl2↑+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)矿泉水中往往含多种有益于人体健康的成分。右图是某品牌矿泉水中标签上的部分内容,则这瓶矿泉水中含Ca2+的物质的量≥ mol。
(2)现代生活离不开铝,工业上以铝土矿为原料生产铝。
现将一定量某铝土矿样品(主要成分Al2O3)溶于过量稀盐酸并制成500 mL溶液。取
100 mL该溶液,测得其中含有H+、Cl-、Mg2+、Al3+、Fe3+五种离子(不考虑其它离子)。
已知部分离子的物质的量浓度为:
c(H+) = 0.02 mol·L-1 c(Mg2+) = 0.01 mol·L-1 2-1-c-n-j-y
c(Fe3+)= 0.02 mol·L-1 c(Cl-) = 0.52 mol·L-1 21*cnjy*com
①溶液中Al3+物质的量浓度为 mol·L-1
②则该铝土矿样品中Al2O3的质量为 g(精确至0.01 g)。

查看答案和解析>>
科目:高中化学 来源: 题型:
己烯是乙烯的同系物,常温下是无色的液体,难溶于水,比水轻。鉴别己烯、乙酸、苯四种无色溶液或液体,可用的一种试剂是
A.盐酸 B.食盐 C.新制的氢氧化铜 D.溴水
查看答案和解析>>
科目:高中化学 来源: 题型:
现取有机物A 3.00g与4.48L(标准状况)氧气在密闭容器中燃烧,燃烧后产物只有二氧化碳、—氧化碳和水蒸气(没有反应物剩余)。将反应生成的气体依次通过浓硫酸和碱石灰,浓硫酸增重3.60g,碱石灰增重4.40g。回答下列问题:
(1)3.00gA中所含氢原子为 mol、碳原子为 mol。
(2)该有机物的分子式为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com