
| A. | I的原子半径大于Br,HI比HBr的热稳定性强 | |
| B. | P的非金属性强于Si,H3PO4比H2SiO3的酸性强 | |
| C. | 锂所在周期元素最高价氧化物对应的水化物中,酸性最强的是HNO3 | |
| D. | 常压下,0℃时冰的密度比水的密度小,水在4℃时密度最大,这些都与氢键有关 |
分析 A.元素的非金属性越强,其简单氢化物的稳定性越强;
B.元素的非金属性越强,其最高价氧化物的水化物酸性越强;
C.元素的非金属性越强,其最高价氧化物的水化物酸性越强,同一周期元素,元素的非金属性随着原子序数增大而增强;
D.冰中存在氢键,具有方向性和饱和性,其体积变大.
解答 解:A.元素的非金属性越强,其简单氢化物的稳定性越强,非金属性Br>I,所以氢化物的稳定性HBr>HI,与非金属原子半径大小无关,故A错误;
B.元素的非金属性越强,其最高价氧化物的水化物酸性越强,非金属性P>Si,所以H3PO4比H2SiO3的酸性强,故B正确;
C.元素的非金属性越强,其最高价氧化物的水化物酸性越强,同一周期元素,元素的非金属性随着原子序数增大而增强,第二周期元素非金属性最强的是F元素,但F、O元素没有最高价氧化物的水化物,所以其最高价氧化物的水化物酸性最强的是硝酸,故C正确;
D.冰中存在氢键,具有方向性和饱和性,其体积变大,则相同质量时冰的密度比液态水的密度小,故D正确;
故选A.
点评 本题考查元素周期律和氢键,为高频考点,侧重考查学生比较判断及知识综合应用能力,明确元素周期律内涵是解本题关键,注意规律中的反常现象,易错选项是C.


科目:高中化学 来源: 题型:选择题
| A. | 40K和40Ca原子中的质子数和中子数都相等 | |
| B. | 任何元素的原子都是由核外电子和核内中子、质子组成的 | |
| C. | 具有相同核电荷数的粒子,一定是同种原子的微粒 | |
| D. | 同种元素的不同核素之间互为同位素 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
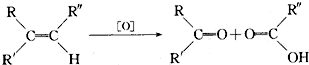 ,现有二烯烃C10H18与KMnO4溶液作用后可得到三种有机物:( CH3)2CO、CH3COOH、CH3CO(CH2)2COOH,由此推断二烯烃可能的结构简式为(CH3)2C═CHCH2CH2C(CH3)═CHCH3.
,现有二烯烃C10H18与KMnO4溶液作用后可得到三种有机物:( CH3)2CO、CH3COOH、CH3CO(CH2)2COOH,由此推断二烯烃可能的结构简式为(CH3)2C═CHCH2CH2C(CH3)═CHCH3.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 除零族元素外,短周期元素原子的最外层电子数等于该元素所属的族序数 | |
| B. | 除短周期外,其他周期均有18种元素 | |
| C. | 副族元素中有非金属元素 | |
| D. | 碱金属元素是指ⅠA族的所有元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用浸泡过高锰酸钾溶液的硅土吸收水果释放的乙烯,可达到水果保鲜的目的 | |
| B. | 在结冰的路面上撒盐,是利用盐与水发生化学反应放出大量热量,促使冰雪融化 | |
| C. | 食盐是咸味剂,工业上常用电解饱和食盐水制备氯气和钠 | |
| D. | 太阳能电池板中的硅是二氧化硅,光导纤维的主要成分是硅单质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 医院里可以用75%的乙醇溶液杀菌消毒 | |
| B. | 甲烷在空气中燃烧产生淡蓝色火焰,同时放出大量的热 | |
| C. | 乙酸乙酯是具有特殊香味、难溶于水的油状液体 | |
| D. | 无论乙烯还是甲苯,都能使酸性高锰酸钾溶液褪色,这与它们分子内含有碳碳双键有关 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
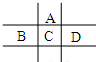 有A、B、C、D、E五种短周期元素,已知相邻的A、B、C、D四种元素原子核外共有56个电子,在周期表中的位置如图所示.E的单质可与酸反应,1molE单质与足量酸作用,在标准状况下能产生33.6LH2;E的阳离子与A的阴离子核外电子层结构完全相同,回答下列问题:
有A、B、C、D、E五种短周期元素,已知相邻的A、B、C、D四种元素原子核外共有56个电子,在周期表中的位置如图所示.E的单质可与酸反应,1molE单质与足量酸作用,在标准状况下能产生33.6LH2;E的阳离子与A的阴离子核外电子层结构完全相同,回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
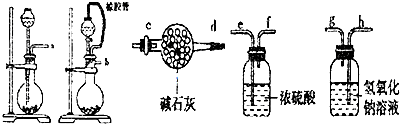
| 滴定次数 | 滴定前读数(mL) | 滴定后读数(mL) |
| 1 | 1.20 | 16.21 |
| 2 | 3.00 | 18.90 |
| 3 | 4.50 | 19.49 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com