
| A.1:10 | B.1:1 | C.1:2 | D.1:20 |
科目:高中化学 来源:不详 题型:问答题
| 1 |
| 2 |
| 1 |
| 2 |
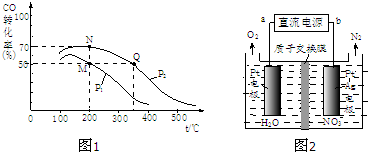
| ||
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.pH=6的某溶液 | B.加酚酞后显无色的溶液 |
| C.能与金属Al反应放出H2的溶液 | D.c(H+)>c(OH—)的任意水溶液 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.1.7 | B.12.3 | C.12 | D.2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.c(H+)等于l×l0-7mol/L的溶液一定是中性溶液 |
| B.无论是纯水,还是酸性、碱性或中性稀溶液,在常温下,其Kw= l×l0-14 |
| C.将水加热,Kw增大,pH不变 |
| D.任何浓度的溶液都可以用pH来表示其酸性的强弱 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.CH3COONa溶液中加入少量KNO3固体后的碱性溶液一定有: C(Na+)-c(CH3COO-)=c(OH-)-c(H+) |
| B.向ZnS白色悬浊液中加入CuSO4溶液,有黑色沉淀产生,是因为Ksp (ZnS)<Ksp (CuS) |
| C.向沸腾的NaOH溶液中滴加FeCl3饱和溶液,可以制备Fe(OH)3胶体 |
| D.热水中加入NaCl溶解至饱和后溶液的pH等于7 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.V一定等于0.2 |
| B.V大于或等于0.2 |
C.混合溶液中离子浓度一定满足:c(Cl-)>c(NH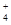 )> c(H+)>c(OH-) )> c(H+)>c(OH-) |
D.混合溶液中离子浓度一定满足:c(NH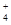 )+c(H+)= c(Cl-)+c(OH-) )+c(H+)= c(Cl-)+c(OH-) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com