
下列物质按只有氧化性、只有还原性、既有氧化性又有还原性的顺序排列的是
A.O2、K、Cl2 B.Cl2、Al、H2
C.NO2、SO2、H2O D.HNO3、HCl、Fe2+
科目:高中化学 来源:2017届内蒙古高三上模拟三化学试卷(解析版) 题型:推断题
已知A为一种盐,C、D、F、N、O为无色气体,E常温常压下为无色无味的液体,N、H、L为高中常见的单质,I为常见无氧强酸,M的焰色反应为紫色,反应①常用于气体F的检验。
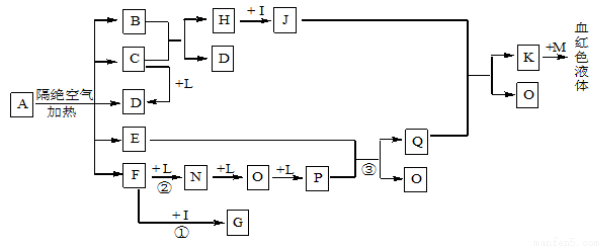
(1)写出D的电子式为_______________;
(2)写出反应①的化学方程式: ;写出反应②的化学方程式: ;反应③中氧化剂和还原剂的物质的量之比为_________________;
(3)将等体积、等浓度的G和F的溶液混合,溶液显碱性,则溶液中离子浓度从大到小的顺序为 ______________________;
(4)检验J中阳离子的实验方法为 ;
(5)已知B中氧元 素的质量分数为22.2﹪,且A分解产生的各物质的物质的量之比为n(B):n(C): n(D):n(E):n(F)=1:2:2:1:2,则A的化学式为_________________________
素的质量分数为22.2﹪,且A分解产生的各物质的物质的量之比为n(B):n(C): n(D):n(E):n(F)=1:2:2:1:2,则A的化学式为_________________________
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山东省高二12月月考化学卷(解析版) 题型:填空题
将1mol/L的FeCl3溶液逐滴滴入沸水中,液体变为___________色,得到的是___________;反应的化学方程式为________。向其中逐滴加入稀硫酸至过量,现象是___________,原因是__________________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山东省高二12月月考化学卷(解析版) 题型:选择题
设NA为阿伏加德罗常数的值。下列说法正确的是( )
A.0.1mol/LNaF溶液中所含F-数小于0.1NA
B.标准状况下,2.24L乙醇中含有的C—H键数为0.5 NA
C.0.1molNa完全被氧化生成Na2O2时,转移的电子数为0.1 NA
D.0.1mol臭氧中所含氧原子数为0.2 NA
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江大庆实验中学高一12月月考化学卷(解析版) 题型:选择题
关于反应3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O下列说法不正确的是
A.HNO3在反应中既表现氧化性也表现出酸性
B.每生成22.4L NO(标准状况)有3mol电子转移
C.HNO3中N元素得电子,化合价升高
D.氧化剂和还原剂物质的量之比为2:3
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江大庆实验中学高一12月月考化学卷(解析版) 题型:选择题
关于钠的用途叙述不正确的是
A.钠用于电光源上
B.钠是一种强还原剂,可以把钛、锆、铌、钽从其熔融盐中置换出来
C.钠和钾的合金常温下为液体,可作原子反应堆的导热剂
D.工业上可用于生产纯碱和大量制备氢氧化钠
查看答案和解析>>
科目:高中化学 来源:2016-2017学年广东省高一上大考二化学卷(解析版) 题型:填空题
无水AlC l3易升华,可用作有机合成的催化剂等。工业上以铝土矿(Al2O3、Fe2O3)为原料制备无水AlCl3的工艺流程如下。
l3易升华,可用作有机合成的催化剂等。工业上以铝土矿(Al2O3、Fe2O3)为原料制备无水AlCl3的工艺流程如下。

提示:2Fe(OH)3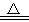 Fe2O3 + 3H2O
Fe2O3 + 3H2O
(1)铝在空气中有强的抗腐蚀性,原因是 。
(2)氯化炉中Al2O3、Cl2和C反应的化学方程式为 ________________________。
(3)用Na2SO3溶液可除去冷却器排出的尾气中的Cl2,反应完后溶液呈碱性,此反应的离子方程式为
_____________________。
(4)为测定制得的无水AlCl3产品(含杂质FeCl3)的纯度,称取16.25 g无水AlCl3样品,溶于过量的NaOH溶液中,过滤出沉淀物,沉淀物经洗涤、灼烧、冷却、称重,得其质量为0.32 g。
①写出上述除杂过程中涉及的离子方程式: 、 。
②产品中AlCl3的质量分数为(只列出计算式,不计算结果) 。
查看答案和解析>>
科目:高中化学 来源:2017届河北省高三上调研四化学试卷(解析版) 题型:填空题
欧盟原定于2012年1月1日起征收航空碳排税以应对冰川融化和全球变暖,使得对如何降低大气中CO2的含量及有效地开发利用碳资源显得更加紧迫。请运用化学反应原理的相关知识研究碳及其化合物的性质。
(1)用电弧法合成的储氢纳米碳管常伴有大量的碳纳米颗粒(杂质),这种颗粒可用如下氧化法提纯, 请完成该反应的化学方程式
_____C+____ KMnO4+____H2SO4→____CO2↑+_____MnSO4+ ______K2SO4+_____H2O
(2)焦炭可用于制取水煤气,测得12g碳与水蒸气完全反应生成水煤气时,吸收了131.6kJ热量。
反应的热化学方程式为_________________。
(3)工业上在恒容密闭容器中用下列反应合成甲醇:CO(g)+2H2(g)  CH3OH(g) △H=akJ/mol 如表所列数据是反应在不同温度下的化学平衡常数(K)。
CH3OH(g) △H=akJ/mol 如表所列数据是反应在不同温度下的化学平衡常数(K)。

① 判断反应达到平衡状态的依据是___________。(填序号)
A.生成CH3OH的速率与消耗CO的速率相等
B.混合气体的平均相对分子质量不变
C.混合气体的密度不变
D.CH3OH、CO、H2的浓度都不再发生变化
②某温度下,将2molCO和一定量的H2充入2L的密闭容器中,充分反应l0min后,达到平衡时测得c(CO)=0.2 mol/L,则以H2表示的反应速率v(H2)=________。
(4)CO还可以用做燃料电池的燃料,某熔融盐燃料电池具有高的发电效率,因而受到重视,该电池用Li2CO3和Na2CO3的熔融盐混合物作电解质,CO为负极燃气,空气与CO2的混和气为正极助燃气,制得在650℃下的燃料电池,其正极反应式:O2+2CO2+4e-=2CO32-,则负极反应式为___________________。
(5)向BaSO4沉淀中加入饱和碳酸钠溶液,充分搅拌,弃去上层淸液,如此处理多次,可使BaSO4 全部转化为BaCO3发生反应:BaSO4(s) + CO32-(aq)=BaCO3(s) +SO42-(aq)。己知某温度下该 反应的平衡常数 K=4.0×10-2,BaSO4的Ksp=1.0×10-10,则 BaCO3的溶度积 Ksp=______。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江省高一12月月考化学试卷(解析版) 题型:选择题
下列关于氯气的叙述,不正确的是( )
A.氯气是一种有毒的气体 B.氯气、氯水、液氯是同一种物质
C.氯气能与水发生反应 D.氯气是一种黄绿色,有刺激性气味的气体
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com