
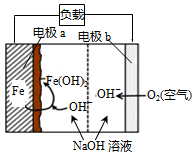
 美国NASA曾开发一种铁-空气二次电池.该电池放电时,其原理如图所示,电池反应为:2Fe+O2+2H2O═2Fe(OH)2.有关该电池放电时的说法正确的是( )
美国NASA曾开发一种铁-空气二次电池.该电池放电时,其原理如图所示,电池反应为:2Fe+O2+2H2O═2Fe(OH)2.有关该电池放电时的说法正确的是( )| A. | a 极质量不变 | B. | b极为电池负极 | ||
| C. | 电子由a极经负载流向b极 | D. | 由电能转变为化学能 |
分析 一种铁-空气二次电池,该电池放电时,是将化学能转化为电能的装置,根据总反应,则铁的一极为电源的负极,发生氧化反应,通入氧气的一极为原电池的正极,电子由负极经外电路流向正极,据此分析解答.
解答 解:A.根据总反应,则铁的一极为电源的负极,并且a极铁变成Fe(OH)2,质量增加,故A错误;
B.通入氧气的一极为原电池的正极,所以b极为电池正极,故B错误;
C.通入氧气的电极是正极,所以a是负极、b是正极,电子从a极经负载流向b极,故C正确;
D.一种铁-空气二次电池,该电池放电时,是将化学能转化为电能的装置,故D错误;
故选C.
点评 本题考查化学电源新型电池,侧重考查基本概念、电池反应式的书写,注意电子流向、电解质溶液中离子流向,为易错点.


科目:高中化学 来源: 题型:选择题
| A. | 向稀盐酸中加入少量金属钠:2Na+2H2O═2Na++2OH-+H2↑ | |
| B. | 向氯化铁溶液中滴加碳酸氢钠溶液:2Fe3++3CO32-+3H2O═2Fe(OH)3↓+3CO2↑ | |
| C. | NH4HCO3溶液与过量KOH浓溶液共热:NH4++OH-$\frac{\underline{\;\;△\;\;}}{\;}$ NH3↑+H2O | |
| D. | 将过量的SO2通入漂白粉溶液中:Ca2++2ClO-+2SO2+2H2O═CaSO4↓+2Cl-+4H++SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 大理石溶于醋酸中:CaCO3+2CH3COOH═Ca2++2CH3COO-+CO2↑+H2O | |
| B. | H2SO4溶液与Ba(OH)2溶液反应:Ba2++OH-+H++SO42-═BaSO4↓+H2O | |
| C. | 将Na投入到CuSO4溶液中:2Na+Cu2+═2Na++Cu↓ | |
| D. | 将Cl2通入水中:Cl2+H2O═2H-+Cl-+ClO- |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
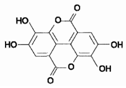 紫薯中的鞣花酸(结构如图)具有防癌和抗癌作用.
紫薯中的鞣花酸(结构如图)具有防癌和抗癌作用.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在0.1mol/lHNO3溶液中加入FeCO3粉末,发生反应的离子方程式为:2FeCO3+2H+═2Fe2++CO2↑+H2O | |
| B. | 在$\frac{c(O{H}^{-})}{c({H}^{+})}$=1010的溶液中NO3-、I-、Na+、SO42-不能大量共存 | |
| C. | 25℃时pH=13的NaOH溶液中含有OH-的数目为0.1 NA | |
| D. | 闭容器中2molNO与1molO2充分反应,产物的分子数小于2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

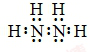 ;N2H4在水中的第一步电离方程式为N2H4+H2O?N2H5++OH-
;N2H4在水中的第一步电离方程式为N2H4+H2O?N2H5++OH-查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 盛放NaOH溶液的试剂瓶不能用玻璃塞:SiO2+2OH-═SiO32-+H2O | |
| B. | 用食醋检验牙膏中的摩擦剂碳酸钙:CaCO3+2H+═Ca2++H2O+CO2↑ | |
| C. | 用氯化铁溶液腐蚀铜线路板:Cu+Fe3+═Fe2++Cu2+ | |
| D. | 用氢氧化钠溶液去除铝表面的氧化膜:Al2O3+2OH-═2AlO2-+H2↑ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com