
反应A(g)+B(g)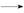 C(g) ΔH,分两步进行:①A(g)+B(g)
C(g) ΔH,分两步进行:①A(g)+B(g)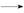 X(g) ΔH1
X(g) ΔH1
②X(g)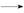 C(g) ΔH2,反应过程中能量变化如图所示,E1表示A(g)+B(g)
C(g) ΔH2,反应过程中能量变化如图所示,E1表示A(g)+B(g)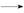 X(g)的活化能,下列说法正确的是( )
X(g)的活化能,下列说法正确的是( )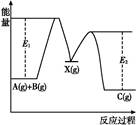
| A.ΔH1=ΔH-ΔH2>0 |
B.X(g)是反应A(g)+B(g)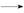 C(g)的催化剂 C(g)的催化剂 |
| C.E2是反应②的活化能 |
| D.ΔH=E1-E2 |
 开心蛙状元作业系列答案
开心蛙状元作业系列答案 课时掌控随堂练习系列答案
课时掌控随堂练习系列答案 一课一练一本通系列答案
一课一练一本通系列答案 浙江之星学业水平测试系列答案
浙江之星学业水平测试系列答案科目:高中化学 来源: 题型:单选题
下列说法中正确的是( )。
| A.物质发生化学反应时都伴随着能量变化,伴随能量变化的物质变化一定是化学变化 |
| B.需要加热的化学反应一定是吸热反应,不需要加热就能进行的反应一定是放热反应 |
| C.吸热反应就是反应物的总能量比生成物的总能量高;也可以理解为化学键断裂时吸收的能量比化学键形成时放出的能量多 |
| D.因为3O2===2O3是吸热反应,所以臭氧比氧气的化学性质更活泼 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
化学反应中的能量变化是由化学反应中旧化学键断裂时吸收的能量与新化学键形成时放出的能量不同引起的。如图为N2(g)和O2(g)反应生成NO(g)过程中的能量变化,下列说法正确的是( )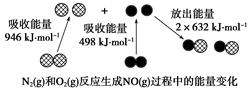
| A.1 mol N2(g)和NA个O2(g)反应放出的能量为180 kJ |
| B.1 mol N2(g)和1 mol O2(g)具有总能量小于2 mol NO(g)具有的总能量 |
| C.通常情况下,N2(g)和O2(g)混合能直接生成NO |
| D.NO是一种酸性氧化物,能与NaOH溶液反应生成盐和水 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列各组热化学方程式中,Q1<Q2的是( )
| A.CH4(g)+2O2(g)=CO2(g)+2H2O(g) ΔH=-Q1 kJ·mol-1 CH4(g)+3/2O2(g)=CO(g)+2H2O(g) ΔH=-Q2 kJ·mol-1 |
| B.S(g)+O2(g)=SO2(g) ΔH=-Q1 kJ·mol-1 S(s)+O2(g)=SO2(g) ΔH=-Q2 kJ·mol-1 |
| C.H2(g)+Br2(g)=2HBr(g) ΔH=-Q1 kJ·mol-1 H2(g)+Cl2(g)=2HCl(g) ΔH=-Q2 kJ·mol-1 |
| D.HCl(aq)+NaOH(aq)=NaCl(aq)+H2O(l) ΔH=-Q1 kJ·mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
甲醛是一种重要的化工产品,可以利用甲醇脱氢制备,反应式如下:
①CH3OH(g) CH2O(g)+H2(g) ΔH1="+84.2" kJ·mol-1
CH2O(g)+H2(g) ΔH1="+84.2" kJ·mol-1
向反应体系中通入氧气,通过反应②2H2(g)+O2(g) 2H2O(g) ΔH2="-483.6" kJ·mol-1提供反应①所需热量,要使反应温度维持在700 ℃,则进料中甲醇与氧气的物质的量之比约为( )
2H2O(g) ΔH2="-483.6" kJ·mol-1提供反应①所需热量,要使反应温度维持在700 ℃,则进料中甲醇与氧气的物质的量之比约为( )
| A.5.74∶1 | B.11.48∶1 | C.1∶1 | D.2∶1 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
将盛有NH4HCO3粉末的小烧杯放入盛有少量醋酸的大烧杯中。然后向小烧杯中加入盐酸,反应剧烈,醋酸逐渐凝固。由此可见( )
| A.NH4HCO3和盐酸的反应是放热反应 |
| B.该反应中,热能转化为产物内部的能量 |
| C.反应物的总能量高于生成物的总能量 |
| D.反应的热化学方程式为:NH4HCO3+HCl=NH4Cl+CO2↑+H2O ΔH=+Q |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
某反应的ΔH=+100 kJ·mol-1,下列有关该反应的叙述正确的是( )
| A.正反应活化能小于100 kJ·mol-1 |
| B.逆反应活化能一定小于100 kJ·mol-1 |
| C.正反应活化能不小于100 kJ·mol-1 |
| D.正反应活化能比逆反应活化能大100 kJ·mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是
①CH3OH(g)+H2O(g)=CO2(g)+3H2(g)
ΔH1=+49.0 kJ/mol;
②CH3OH(g)+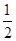 O2(g)=CO2(g)+2H2(g)
O2(g)=CO2(g)+2H2(g)
ΔH2=-192.9 kJ/mol。
根据上述反应,下列说法正确的是( )
| A.反应①中的能量变化如上图所示 |
| B.CH3OH转变成H2的过程一定要吸收能量 |
| C.1 mol CH3OH充分燃烧放出的热量为192.9 kJ |
| D.可推知2H2(g)+O2(g)=2H2O(g) ΔH=-483.8 kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
已知乙炔与苯蒸气完全燃烧的热化学方程式如下:
①C2H2(g)+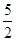 O2(g)―→2CO2(g)+H2O(l) ΔH=-1 300 kJ·mol-1
O2(g)―→2CO2(g)+H2O(l) ΔH=-1 300 kJ·mol-1
②C6H6(g)+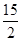 O2(g)―→6CO2(g)+3H2O(l) ΔH=-3 295 kJ·mol-1
O2(g)―→6CO2(g)+3H2O(l) ΔH=-3 295 kJ·mol-1
下列说法正确的是 ( )。
| A.1 mol C2H2(g)完全燃烧生成气态水时放热大于1 300 kJ |
| B.1 mol C6H6(l)完全燃烧生成液态水时放热大于3 295 kJ |
| C.相同条件下,等质量的C2H2(g)与C6H6(g)完全燃烧,C6H6(g)放热更多 |
| D.C2H2(g)三聚生成C6H6(g)的过程属于放热反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com