
【题目】一定温度下,将![]() 加入1L
加入1L![]() 溶液中,充分搅拌
溶液中,充分搅拌![]() 不考虑液体体积变化
不考虑液体体积变化![]() ,已知:
,已知:![]() ;
;![]() ,下列有关说法正确的是
,下列有关说法正确的是
A.相同温度下,AgCl的溶解性比![]() 弱
弱
B.沉淀转化反应![]() 的平衡常数为
的平衡常数为![]()
C.混合后溶液中的:![]()
![]()
![]()
![]()
D.混合后溶液中的:![]()
![]()
【答案】A
【解析】
A.氯化银和碳酸银阴阳离子之比不同,不能用直接用溶度积常数比较溶解性;
B.![]() ,平衡常数
,平衡常数![]() 计算;
计算;
C.![]() ,
,![]() ;
;
D.据溶液中的电荷守恒分析。
A.设Ag2CO3饱和溶液的物质的量浓度为x,则c(Ag+)=2x,c(CO32-)=x,则有![]() =1×10-11,x=1.26×10-4mol/L;设AgCl饱和溶液的物质的量浓度为y,则c(Ag+)=c(Cl-)=y,
=1×10-11,x=1.26×10-4mol/L;设AgCl饱和溶液的物质的量浓度为y,则c(Ag+)=c(Cl-)=y,![]() =2×10-10,y=1.41×10-5mol/L,相同温度下AgCl的溶解性比Ag2CO3弱,故A正确;
=2×10-10,y=1.41×10-5mol/L,相同温度下AgCl的溶解性比Ag2CO3弱,故A正确;
B.![]() ,平衡常数
,平衡常数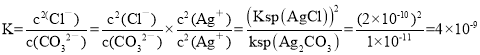 故B错误;
故B错误;
C.![]() ,
,![]() ,所以c(CO32-)>c(Cl-),故C错误;
,所以c(CO32-)>c(Cl-),故C错误;
D. 据电荷守恒,![]() ,故D错误;
,故D错误;
故选A。


 数学奥赛暑假天天练南京大学出版社系列答案
数学奥赛暑假天天练南京大学出版社系列答案 南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案科目:高中化学 来源: 题型:
【题目】在密闭容器中,对于反应2NO2(g)![]() N2O4(g) △H<0,增大压强(体积迅速减小),下列说法正确的是( )
N2O4(g) △H<0,增大压强(体积迅速减小),下列说法正确的是( )
A.平衡逆向移动
B.混合气体颜色比原来深
C.混合气体颜色比原来浅
D.混合气体的平均相对分子质量变小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下反应:A2(g)+3 B2(g)![]() 2 AB3(g) (每生成2 mol AB3放出92.4 kJ的热量),在恒温恒压的密闭容器中进行如下实验:①通入1 mol A2和3 mol B2,达平衡时放出热量为Q1,②通入2 mol A2和6 mol B2,达平衡时放出热量为Q2,则下列关系正确的是
2 AB3(g) (每生成2 mol AB3放出92.4 kJ的热量),在恒温恒压的密闭容器中进行如下实验:①通入1 mol A2和3 mol B2,达平衡时放出热量为Q1,②通入2 mol A2和6 mol B2,达平衡时放出热量为Q2,则下列关系正确的是
A.Q2 = 2 Q1 B.2Q1 < Q2
C.Q1 < Q2 < 92.4 kJ D.Q1 = Q2 < 92.4 kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从500mL1mol·L-1的CuSO4溶液中取出100mL,下列关于100mL溶液的叙述错误的是()
A.CuSO4的物质的量浓度为1mol·L-1
B.SO42-的物质的量浓度为1mol·L-1
C.含Cu2+的物质的量为0.1mol
D.含CuSO4的质量为80.0g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】准确称取6.0g铝土矿样品(含Fe2O3),加入100mL稀硫酸中,充分反应后向滤液中加入10mol·L-1NaOH溶液,产生沉淀的质量和加入NaOH溶液体积之间的关系如图所示。则所用硫酸物质的量浓度为( )
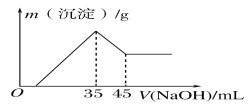
A.1.75mol·L-1B.3.50mol·L-1
C.0.85mol·L-1D.无法确定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是![]()
![]() 常温下,强酸溶液的
常温下,强酸溶液的![]() ,将溶液的体积稀释到原来的
,将溶液的体积稀释到原来的![]() 倍,则
倍,则![]()
![]() 已知
已知![]() 的
的![]() ,所以在
,所以在![]() 溶液中有
溶液中有![]()
![]() 将
将![]() 的NaHS和
的NaHS和![]() 的
的![]() 溶液等体积混合,所得溶液中有
溶液等体积混合,所得溶液中有![]()
![]() 在
在![]() 氨水中滴加
氨水中滴加![]() 盐酸,刚好完全中和时
盐酸,刚好完全中和时![]() ,由水电离产生的
,由水电离产生的![]() .
.
A.![]() B.
B.![]() C.
C.![]() D.
D.![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以高硫铝土矿(主要成分为Al2O3、Fe2O3、SiO2,少量FeS2和金属硫酸盐)为原料,生产氧化铝并获得Fe3O4的部分工艺流程如下:
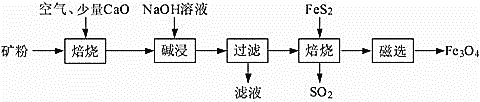
(1)焙烧过程均会产生SO2,用NaOH溶液吸收过量SO2的离子方程式为___________。利用喷雾干燥法脱硫工艺也是除去SO2的常见方法,先将含SO2的废气溶于水,再用饱和石灰浆吸收。该温度下吸收液中c(Ca2+)一直保持为0.50 mol·L-1,已知KSP(CaSO3)=1.4×10-7,则吸收后溶液中![]() 的浓度______________________。
的浓度______________________。
(2)添加1%CaO和不添加CaO的矿粉焙烧,其硫去除率随温度变化曲线如图所示:
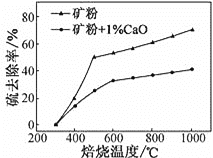
已知:多数金属硫酸盐的分解温度都高于600℃;硫去除率=(1![]() )×100%
)×100%
①不添加CaO的矿粉在低于500 ℃焙烧时,去除的硫元素主要来源于____________。
②700℃焙烧时,添加1%CaO的矿粉硫去除率比不添加CaO的矿粉硫去除率低,其主要原因是________________。
(3)向“过滤”得到的滤液中通入过量CO2,含铝粒子反应的离子方程式_________
(4) “过滤”得到的滤渣中含大量的Fe2O3。Fe2O3与FeS2混合后在缺氧条件下焙烧生成Fe3O4和SO2,理论上完全反应消耗的n(FeS2)∶n(Fe2O3)=__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】借助太阳能将光解水制H2与脱硫结合起来,既能大幅度提高光解水制H2的效率,又能脱除SO2,工作原理如下图所示。下列说法不正确的是

A. 该装置可将太阳能转化为化学能
B. 催化剂b附近的溶液pH增大
C. 吸收1mol SO2,理论上能产生1mol H2
D. 催化剂a表面发生的反应为:2H2O+2e-=H2↑+2OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W 均为常见的短周期主族元素,常温下,其最高价氧化物对应的水化物溶液(浓度均为0.01mol/L)的pH 和原子半径的关系如图所示,其中Y为碳元素。下列说法正确的是
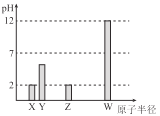
A.X是硫元素
B.Y的最高价氧化物的电子式为![]()
C.W 的最高价氧化物对应的水化物中仅含离子键
D.Z的最高价氧化物对应水化物的化学式为HZO4
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com