
| 浓度 时间/min 物质 | 0 | 1 | 2 | 3 | 4 |
| CH4 | 0.2mol?L-1 | 0.13mol?L-1 | 0.1mol?L-1 | 0.1mol?L-1 | 0.09moˉL-1 |
| H2 | 0mol?L-1 | 0.2mol?L-1 | 0.3mol?L-1 | 0.3mol?L-1 | 0.33mol?L-1 |
| n(CH4) |
| n(H2O) |

| 1 |
| 2 |
| 1 |
| 2 |
| 1000L |
| 22.4L/mol |
| c(CO)?c3(H2) |
| c(CH4)?c(H2O) |
| 0.1×0.33 |
| 0.1×0.2 |
| 8.96L |
| 22.4L/mol |
| 0.4mol×4 |
| 8 |


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
| A、用FeCl3溶液腐蚀铜线路板:Cu+2Fe3+=Cu2++2Fe2+ |
| B、Na2O2与H2O反应制备O2:Na2O2+H2O=2Na++2OH-+O2↑ |
| C、将氯气溶于水制备次氯酸:Cl2+H2O=2H++Cl-+ClO- |
| D、将磁性氧化铁溶于盐酸:Fe3O4+8H+═3Fe3++4H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
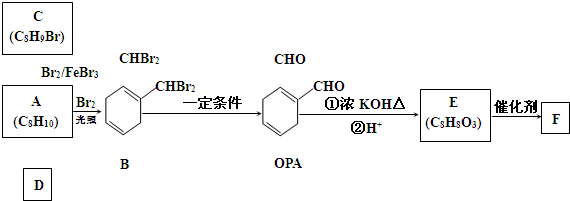

| 浓硫酸 |
| 170℃ |
| Br2 |

查看答案和解析>>
科目:高中化学 来源: 题型:
| X | A | ||
| Y | C | B |
| A、原子半径大小:Y>C>X>A |
| B、Y和B形成的化合物中Y和B的原子个数比为2:3 |
| C、X、C、A中最高价氧化物对应的水化物的酸性最强的是A |
| D、A、B均为非金属元素,所以两者的氢化物相遇不发生反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 离子半径 | 酸性 | 还原性 | 得电子能力 |
| N3- | H2SO4 | O2- | 35Cl |

查看答案和解析>>
科目:高中化学 来源: 题型:
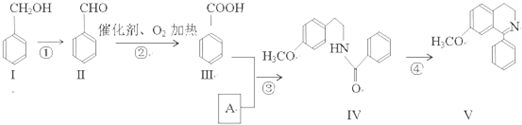
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、6种 | B、7种 | C、8种 | D、9种 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 在25mL 0.1mol/L NaOH溶液中逐滴加入0.2mol/L CH3COOH溶液,曲线如图所示,有关粒子浓度关系比较正确的( )
在25mL 0.1mol/L NaOH溶液中逐滴加入0.2mol/L CH3COOH溶液,曲线如图所示,有关粒子浓度关系比较正确的( )| A、在A、B间任意一点,溶液中一定都有c(Na+)>cCH3COO-)>c(OH-)>c(H+) |
| B、在B点,a>12.5,且有c(Na+)=c(CH3COO-)>c(OH-)=c(H+) |
| C、在C点:c(Na+)>c(CH3COO-)>c(H+)>c(OH-) |
| D、在D点:c(CH3COO-)+c(CH3COOH)=2 c(Na+) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氟利昂和NOX都能破坏臭氧层,从而导致“温室效应” |
| B、针对H7N9禽流感的扩散情况,要加强环境、个人等的消毒预防,可选用含氯消毒剂、活性银离子、酒精、双氧水等作为消毒剂,这种处理方法符合绿色化学核心 |
| C、光缆在信息产业中有广泛应用,制造光缆的主要材料是单质硅 |
| D、肌红蛋白、蚕丝、过氧化氢酶、鱼油充分水解后不能全部都得到氨基酸 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com