
【题目】下列离子反应方程式正确的是
A.金属钠投入蒸馏水2 Na+2H2O=2 Na+ +2OH- +H2↑
B.向亚硫酸钠溶液中加入足量硝酸SO3 2- +2 H+ =SO2↑+ H2O
C.用浓盐酸与MnO2反应制取少量氯气MnO2+4H++2C1- = Mn2+ + 2H2O+Cl2↑
D.硫酸亚铁溶液中加入酸化的双氧水Fe2++2H++H2O2 = Fe3++2H2O
 愉快的寒假南京出版社系列答案
愉快的寒假南京出版社系列答案科目:高中化学 来源: 题型:
【题目】关于Na2CO3和NaHCO3性质的说法正确的是
A. 在水中的溶解性: NaHCO3>Na2CO3
B. 热稳定性:NaHCO3<Na2CO3
C. 与酸反应的剧烈程度: NaHCO3<Na2CO3,
D. 只能让NaHCO3转化成Na2CO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物A是一元羧酸,由C,H,O元素组成,质量分数:C%40%;H 6.67%;取0.60g A配成溶液,用含0.01mol NaOH 的溶液能恰好完全中和.
(1)A的最简式为;最简式量为 .
(2)A的相对分子质量为;分子式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将14g铜银合金与足量的HNO3反应,放出的气体与标准状况下体积为1.12L的O2 混合后再通入水中,恰好全部吸收,则合金中铜的质量为
A. 4.8g B. 3.2g C. 6.4g D. 10.8g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】同温度下,体积均为1L的两个恒容密闭容器中发生可逆反应:N2(g)+3H2(g)![]() 2NH3(g) △H=-92.6kJ/mol.测得数据如表
2NH3(g) △H=-92.6kJ/mol.测得数据如表
容器编号 | 起始时各物质物质的量/mol | 达到平衡时体系能量的变化 | ||
N2 | H2 | NH3 | ||
(1) | 2 | 3 | 0 | 27.78kJ |
(2) | 1.6 | 1.8 | 0.8 | Q |
下列叙述不正确的是
A.容器(1)(2)反应达平衡时压强相等
B.容器(2)中反应开始时v(正)>v(逆)
C.容器(2)中反应达平衡时,吸收的热量Q为9.26kJ
D.若条件为“绝热恒容”,容器(1)中反应达平衡时n(NH3)<0.6mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关氧化还原反应的叙述错误的是
A.复分解反应一定不是氧化还原反应
B.氧化还原反应一定有元素化合价的升降
C.氧化还原反应中氧化剂和还原剂可能是同一种物质
D.氧化剂失电子,被还原
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】霉酚酸酯(MMF)是器官移植中抑制细胞增殖最常用的药物.下列说法正确的是( ) 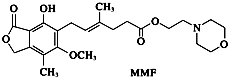
A.MMF能溶于水
B.1 mol MMF能与含3 mol NaOH的水溶液完全反应
C.1 mol MMF能与6 mol氢气发生加成反应
D.MMF能发生取代反应和消去反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,H2(g)+CO2(g)H2O(g)+CO(g)的平衡常数K= ![]() .该温度下在甲、乙、丙三个恒容密闭容器中,投入H2(g)和CO2(g),其起始浓度如表所示.下列判断不正确的是( )
.该温度下在甲、乙、丙三个恒容密闭容器中,投入H2(g)和CO2(g),其起始浓度如表所示.下列判断不正确的是( )
起始浓度 | 甲 | 乙 | 丙 |
c(H2)/mol/L | 0.010 | 0.020 | 0.020 |
c(CO2)/mol/L | 0.010 | 0.010 | 0.020 |
A.平衡时,乙中CO2的转化率大于60%
B.平衡时,甲中和丙中H2的转化率均是60%
C.平衡时,丙中c(CO2)是甲中的2倍,是0.012mol/L
D.反应开始时,丙中的反应速率最快,甲中的反应速率最慢
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com