
| A. | 用激光笔光束鉴别氯化铁溶液和氢氧化铁胶体 | |
| B. | 用KSCN溶液鉴别Fe3+和Fe2+ | |
| C. | 用NaOH溶液和红色石蕊试纸鉴别溶液是否含NH4+ | |
| D. | 在氢氧化钠溶液中滴入氯化铁饱和溶液可以制得氢氧化铁胶体 |
分析 A.丁达尔现象为胶体特有的性质;
B.KSCN溶液鉴别Fe3+时溶液为血红色;
C.铵根离子与碱加热生成氨气,氨气可使红色石蕊试纸变蓝;
D.氢氧化钠溶液中滴入氯化铁饱和溶液,反应生成红褐色沉淀.
解答 解:A.丁达尔现象为胶体特有的性质,则用激光笔光束可鉴别氯化铁溶液和氢氧化铁胶体,故A正确;
B.KSCN溶液鉴别Fe3+时溶液为血红色,不能与亚铁离子反应,现象不同,可鉴别,故B正确;
C.铵根离子与碱加热生成氨气,氨气可使红色石蕊试纸变蓝,则试剂可鉴别铵根离子,故C正确;
D.氢氧化钠溶液中滴入氯化铁饱和溶液,反应生成红褐色沉淀,不能制备胶体,应向沸水中滴入氯化铁饱和溶液可以制得氢氧化铁胶体,故D错误;
故选D.
点评 本题考查化学实验方案的评价,为高频考点,把握物质的性质、常见离子的检验、胶体制备为解答的关键,侧重分析与实验能力的考查,注意元素化合物与实验的结合及实验评价性分析,题目难度不大.


科目:高中化学 来源: 题型:实验题
| 化合物 | 甲 | 乙 | 丙 |
| 组成元素 | B、C | A、C | C、D |
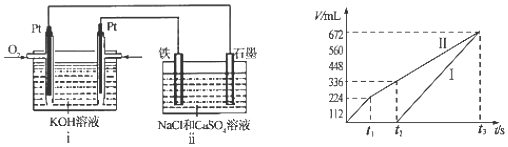
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 目前工业上主要采用接触法制硫酸,并使用热交换器充分利用反应中放出的热量 | |
| B. | 从海水中提取溴,是将提取粗盐后的母液浓缩、氧化,使溶液中的溴离子发生氧化反应转化成溴单质,就得到粗溴 | |
| C. | 工业上合成氨没有采用更大的压强是从设备和动力要求方面考虑的 | |
| D. | 离子交换膜在工业生产中广泛应用,如氯碱工业使用了阳离子交换膜 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验操作 | 预期现象及结论 |
| 步骤1:取少量样品b于烧杯中,加足量蒸馏水,并用玻璃棒搅拌 | 样品溶解,形成无色溶液. |
| 步骤2:取少量步骤1形成的溶液于试管中,再滴加少量NaOH溶液,振荡 | 有白色沉淀生成,说明样品b中添加了镁盐 |
| 步骤3:取少量步骤1形成的溶液于试管中,再滴加少量的BaCl2溶液振荡 | 若有白色沉淀产生,则添加的是MgSO4.若无明显现象,则添加的是MgCl2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
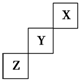
| A. | X、Y、Z三种元素中,与H2化合最容易的是X元素 | |
| B. | 最高价氧化物对应的水化物的酸性:Y>Z | |
| C. | Y的最高正化合价为+7价 | |
| D. | X单质的熔点比Z的低 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
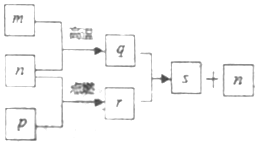 短周期元素X、Y、Z、W的原子序数依次增加,其中一种为金属元素.Y元素在大气中存在两种常见单质,Z与X处于同一主族,q、r、s是由这些元素组成的二元化合物,m、n、p分别是元素Z、X、W的单质,p通常为黄绿色气体.上述物质的转化关系如图所示.下列说法正确的是( )
短周期元素X、Y、Z、W的原子序数依次增加,其中一种为金属元素.Y元素在大气中存在两种常见单质,Z与X处于同一主族,q、r、s是由这些元素组成的二元化合物,m、n、p分别是元素Z、X、W的单质,p通常为黄绿色气体.上述物质的转化关系如图所示.下列说法正确的是( )| A. | 化合物Z2Y2与X2Y2中化学键完全相同 | |
| B. | 最简单氢化物的沸点:Y>W | |
| C. | 36g物质q与过量的物质r反应则有2mol电子发生转移 | |
| D. | 由Y、Z、W三种元素组成的化合物的水溶液一定显中性 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com