
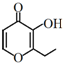
 俗称“一滴香”的有毒物质被人食用后会损伤肝脏,还能致癌.“一滴香”的分子结构如图所示,下列说法正确的是( )
俗称“一滴香”的有毒物质被人食用后会损伤肝脏,还能致癌.“一滴香”的分子结构如图所示,下列说法正确的是( )| A. | lmol该有机物最多能与2molH2发生加成反应 | |
| B. | 该有机物的分子式为C7H8O3 | |
| C. | 该有机物能发生取代反应、加成反应、消去反应和氧化反应 | |
| D. | 该有机物的一种芳香族同分异构体能发生银镜反应 |
分析 由结构可知,分子中含碳碳双键、-OH、羰基、醚键,结合烯烃、醇的性质来解答.
解答 解:A.碳碳双键、羰基均与氢气发生加成反应,则lmol该有机物最多能与3molH2发生加成反应,故A错误;
B.由结构可知,分子式为C7H8O3,故B正确;
D.与-OH相连C的邻位C上没有H,不能发生消去反应,故C错误;
D.该有机物含有三个双键,其芳香族同分异构体含有苯环,所以苯环的支链上不可能含有醛基,导致其芳香族同分异构体不能发生银镜反应,故D错误;
故选B.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系为解答的关键,侧重分析与应用能力的考查,注意选项D为解答的难点,题目难度不大.


科目:高中化学 来源: 题型:选择题
 有机充电电池具有不含重金属,受资源限制少等优点而备受瞩目.某PYT-锂电池总反应如图,下列叙述不正确的是( )
有机充电电池具有不含重金属,受资源限制少等优点而备受瞩目.某PYT-锂电池总反应如图,下列叙述不正确的是( )| A. | PYT分子式为C16H6O4 | B. | 不能采用水溶液作为电解质溶液 | ||
| C. | 充电时,负极反应为Li-e-=Li+ | D. | 放电时,Li+向正极移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 150ml 1mol/LNaCl溶液 | B. | 100ml 3mol/L KClO3溶液 | ||
| C. | 75ml 2mol/L MgCl2溶液 | D. | 50ml 1mol/L FeCl3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分别加热,观察有无气体生成 | |
| B. | 制成稀溶液,再分别滴加同浓度的稀盐酸 | |
| C. | 制成稀溶液,分别加入CaCl2溶液 | |
| D. | 制成溶液,分别加入少量澄清的石灰水 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c(Na+)═c(HCO3-)+c(CO32-)+c(H2CO3) | |
| B. | c (Na+)+c (H+)═c (HCO3-)+c (CO32-)+c (OH-) | |
| C. | HCO3- 的电离程度大于HCO3-的水解程度 | |
| D. | c(Na+)>c(HCO3-)>c(OH-)>c(CO32-)>c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 Q、R、X、Y、Z、W为周期表中原子序数依次递增的前四周期元素.
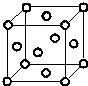
Q、R、X、Y、Z、W为周期表中原子序数依次递增的前四周期元素.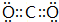 ,分子的空间构型是直线形;Z3+的原子结构示意图为
,分子的空间构型是直线形;Z3+的原子结构示意图为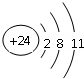 ;X2Q4分子中X原子的杂化方式为sp3杂化.
;X2Q4分子中X原子的杂化方式为sp3杂化.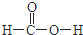 ,m g该物质完全燃烧后通过足量Na2O2固体充分吸收,Na2O2固体增重的质量为$\frac{15m}{23}$g
,m g该物质完全燃烧后通过足量Na2O2固体充分吸收,Na2O2固体增重的质量为$\frac{15m}{23}$g查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 酒精的燃烧热△H=(Q2-Q3-3Q1)kJ/mol | |
| B. | 由③可知1molC2H5OH(g)的能量大于2molCO2(g)和3molH2O(g)的总能量 | |
| C. | H2O(g)→H2O(l)释放出了热量,所以该过程为放热反应 | |
| D. | 23g液态酒精完全燃烧生成CO2(g)和H2O(l),放出的热量为(0.5Q2-0.5Q3-1.5Q1)kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径比较:X<Y<Z<W | |
| B. | Y的氢化物沸点高于W的氢化物 | |
| C. | Y的氢化物稳定性一定弱于W的氢化物 | |
| D. | 短周期所有元素中,w的最高价氧化物的水化物酸性最强 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com