
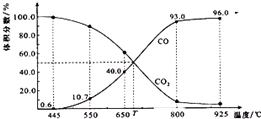
 һ������CO2��������̼������ɱ�ĺ�ѹ�ܱ������з�Ӧ��C��s��+CO2��g��?2CO��g����ƽ��ʱ����ϵ����������������¶ȵĹ�ϵ��ͼ��ʾ����֪�������ѹ��p����=������ѹ��p�������������������˵����ȷ���ǣ�������
һ������CO2��������̼������ɱ�ĺ�ѹ�ܱ������з�Ӧ��C��s��+CO2��g��?2CO��g����ƽ��ʱ����ϵ����������������¶ȵĹ�ϵ��ͼ��ʾ����֪�������ѹ��p����=������ѹ��p�������������������˵����ȷ���ǣ�������| A�� | 550��ʱ��������������壬v����v�� ����С��ƽ�ⲻ�ƶ� | |
| B�� | 650��ʱ����Ӧ��ƽ���CO2��ת����Ϊ25.0% | |
| C�� | T��ʱ��������������CO2��CO��ƽ�ⲻ�ƶ� | |
| D�� | 925��ʱ����ƽ���ѹ����ƽ��Ũ�ȱ�ʾ�Ļ�ѧƽ�ⳣ��Kp=24��p�� |
���� A���ɱ�ĺ�ѹ�ܱ������з�Ӧ��550��ʱ������������壬�൱�ڼ�Сѹǿ����v����v������С���ָķ�Ӧ�������������ķ�Ӧ����ƽ�������ƶ���
B����ͼ��֪��650��ʱ����Ӧ��ƽ���CO���������Ϊ40%���迪ʼ����Ķ�����̼Ϊ1mol����������ʽ���м��㣻
C����ͼ��֪��T��ʱ����Ӧ��ƽ���CO��CO2�����������Ϊ50%��Ϊƽ��״̬��
D.925��ʱ����ƽ���ѹ����ƽ��Ũ�ȱ�ʾ�Ļ�ѧƽ�ⳣ��Kp=$\frac{{p}^{2}��CO��}{P��C{O}_{2}��}$���ݴ˼��㣮
��� �⣺A���ɱ�ĺ�ѹ�ܱ������з�Ӧ��550��ʱ������������壬�൱�ڼ�Сѹǿ��ƽ�����������ƶ���v����v������С����A����
B����ͼ��֪��650��ʱ����Ӧ��ƽ���CO���������Ϊ40%���迪ʼ����Ķ�����̼Ϊ1mol��ת����xmol��
����C��s��+CO2��g��?2CO��g��
��ʼ 1 0
ת�� x 2x
ƽ�⣻ 1-x 2x
����$\frac{2x}{1-x+2x}$��100%=40%�����x=0.25mol����CO2��ת����Ϊ��$\frac{0.25}{1}$��100%=25.0%����B��ȷ��
C����ͼ��֪��T��ʱ����Ӧ��ƽ���CO��CO2�����������Ϊ50%��Ϊƽ��״̬������ƽ�ⲻ�ƶ�����C��ȷ��
D.925��ʱ��CO���������Ϊ96%����CO2�����������Ϊ4%��������ƽ���ѹ����ƽ��Ũ�ȱ�ʾ�Ļ�ѧƽ�ⳣ��Kp=$\frac{{p}^{2}��CO��}{P��C{O}_{2}��}$=$\frac{��0.96p��^{2}}{0.04p}$=23.04P����D����
��ѡBC��
���� ���⿼���˻�ѧƽ��ļ��㣬��Ŀ�Ѷ��еȣ���ȷͼ�����߱仯�ĺ���Ϊ���ؼ���ע�����ջ�ѧƽ�⼰��Ӱ�����أ�����������ѧ���ķ������������Ӧ��������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2017�콭��ʡ����и�����ѧ����������һ��ѧ�Ծ��������棩 ���ͣ�ѡ����
�����й����ʵ�������Ӧ�����Ӧ����
A��̼������Һ�ʼ��ԣ�������ϴȥ��м���������
B���������ۻ������������ɻ�������Ľṹ����
C��̿���л�ԭ�ԣ�������ұ���ơ�þ�����Ƚ���
D��Ũ�������ǿ�����ԣ������ڸ��������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����

| A�� | ����Һ��pH=7ʱ����Һ�������Ϊ20mL����������Һ��Ϻ�����ı仯�� | |
| B�� | ��0.1mol/L ��Na2CO3��Һ�У�c��Na+��+c��H+���Tc��CO32-��+c��OH-��+c��HCO3-�� | |
| C�� | ��A����ʾ����Һ�У�c��CO32-���Tc��HCO3-����c��H+����c��OH-�� | |
| D�� | ��B����ʾ����Һ�У�Ũ��������������Na+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������Ϊ94��������Ϊ144���У�Pu��ԭ�ӣ�14494Pu | |
| B�� | H2O2�ĵ���ʽ��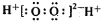 | |
| C�� | S2-���ӽṹʾ��ͼ�� | |
| D�� |  ������2-��-4-���� ������2-��-4-���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
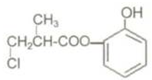
| A�� | �л���A��Ũ�����ϼ��ȣ����Է�����ȥ��Ӧ | |
| B�� | 1molA��������H2�����ӳɷ�Ӧ������������4molH2 | |
| C�� | 1molA������NaOH��Һ������Ӧ������������ 4molNaOH | |
| D�� | �л���A��ͬ���칹��������ϡ������ˮ�����ɶ����ӵ���6�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��

| A�� | �絼�ʴ������������ж�����к͵ζ����յ� | |
| B�� | �ù����У�a����ʾ��Һ�ĵ�������ǿ | |
| C�� | c��絼����С����Ϊ��ʱ��Һ�е�������Ŀ���� | |
| D�� | d����ʾ��Һ�д��ڣ�c��Cl-��+c��OH-��=c��H+��+c��Na+�� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com