
【题目】“春蚕到死丝方尽,蜡炬成灰泪始干”是唐代诗人李商隐的著名诗句,下列关于该诗句中所涉及物质的说法错误的是
A. 蚕丝的主要成分是蛋白质
B. 蚕丝属于天然高分子材料
C. “蜡炬成灰”过程中发生了氧化反应
D. 古代的蜡是高级脂肪酸酯,属于高分子聚合物
 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案科目:高中化学 来源: 题型:
【题目】等质量镁铝合金分别与下列四种过量的溶液充分反应,放出H2最多的是( )
A. H2SO4溶液 B. NaOH溶液 C. 蔗糖溶液 D. NaCl溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是:
①CH3OH(g)+H2O(g)=CO2(g)+3H2(g); △H= +49.0 kJ·mol-1
②CH3OH(g)+1/2O2(g)=CO2(g)+2H2(g);△H= -192.9 kJ·mol-1
下列说法正确的是
A. CH3OH的燃烧热为192.9 kJ·mol-1
B. 反应①中的能量变化如图所示

C. CO2和H2转变成CH3OH的过程不一定要吸收能量
D. 根据②推知反应:CH3OH(l)+1/2O2(g)=CO2(g)+2H2(g)的△H<-192.9kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A. 液氯可以储存在钢瓶中
B. 天然气的主要成分是甲烷的水合物
C. 天然石英和水晶的主要成分都是二氧化硅
D. 硫元素在自然界的存在形式有硫单质、硫化物和硫酸盐等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NH3是一种重要的化工原料,可用来制备肼、硝酸、硝酸铵和氯胺等。
(1)N2和H2以物质的量之比为1∶3在不同温度和压强下发生反应:N2+3H2![]() 2NH3,测得平衡体系中NH3的物质的量分数如图。
2NH3,测得平衡体系中NH3的物质的量分数如图。
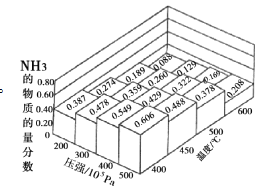
①下列途径可提高氨气产率的是_____(填序号)。
a.采用常温条件 b.采用适当的催化剂 c.将原料气加压 d.将氨液化,不断移去液氨
②上图中所示的平衡体系中NH3的物质的量分数为0.549和0.478时,该反应的平衡常数分别为K1、K2,则K1___(选填“>”或“<”或“=”)K2。
(2)肼(N2H4)是一种火箭燃料。已知:N2(g)+2O2(g)=2NO2(g)H=+67.7kJ·mol-1
N2H4(g)+O2g)=N2(g)+2H2O(g)H=-534.0kJ·mol-1
NO2(g)=1/2N2O4(g)H=-28.0 kJ·mol-1
①反应2N2H4(g)+N2O4(g)=3N2(g)+4H2O(g)的H=_____ kJ·mol-1。
②氨气与次氯酸钠溶液反应生成肼的离子方程式为_________。
(3)电解硝酸工业的尾气NO可制备NH4NO3,其工作原理如图。
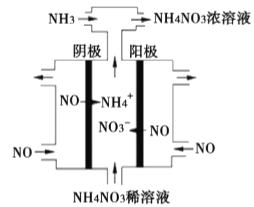
①阴极的电极反应式为__________。
②将电解生成的HNO3全部转化为NH4NO3,则通入的NH3与实际参加反应的NO的物质的量之比至少为_________。
(4)饮用水消毒时,氯胺(NH2Cl等)在酸性条件下具有良好的效果,其原因是_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】20世纪30年代,Eyring和Pelzer在碰撞理论的基础上提出化学反应的过渡态理论:化学反应并不是通过简单的碰撞就能完成的,而是在反应物到生成物的过程中经过一个高能量过渡态。分析图中信息,回答下列问题:
(1)图一是NO2和CO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式:___________________________________。在反应体系中加入催化剂,E1和E2的变化是:E1_________,E2________(填“增大”、“减小”或“不变”),对反应热是有无影响?_______________,原因是_______________________________________________。
(2)图二是红磷P(s)和Cl2(g)发生反应生成PCl3(g)和PCl5(g)的反应过程与能量关系图(图中的△H表示生成1mol产物的数据)。根据图二回答下列问题:
① P(s)和Cl2(g)反应生成PCl3(g)的热化学方程式__________________________________。
PCl5(g)分解成PCl3(g)和Cl2(g)的热化学方程式____________________________________。
② P(s)和Cl2(g)分两步反应生成1molPCl5(g)的△H1与P(s)和Cl2(g)一步反应生成1molPCl5(g)的△H2关系是:△H2____________△H1(填“大于”、“小于”或“等于”),原因是_______________________。
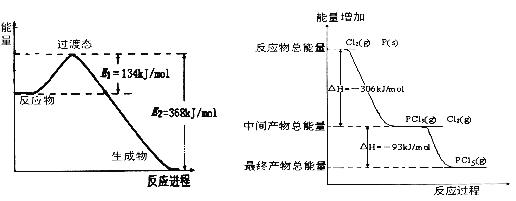
图一 图二
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关电池叙述正确的是( )
A.水果电池是高效环保的家用电池B.锌锰干电池是一种常用的二次电池
C.锌锰干电池碳棒是负极,锌片是正极D.锌锰干电池工作一段时间后锌外壳逐渐变薄
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究小组用黄铁矿(FeS2)、氯酸钠和硫酸溶液混合反应制备C1O2气体,再用水吸收该气体可得C1O2溶液。在此过程中需要控制适宜的温度,若温度不当,副反应增加,影响生成C1O2气体的纯度,且会影响C1O2的吸收率,具体情况如图所示。
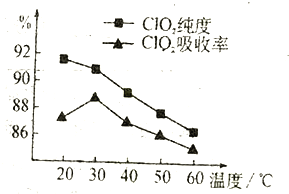
(1)据图可知,反应时需要控制的适宜温度是________℃,要达到此要求需要采取的措施是________。
(2)已知:黄铁矿中的硫元素在酸性条件下可被ClO3-氧化成SO42-,请写出FeS2、氯酸钠和硫酸溶液混合反应生成二氧化氯(C1O2)的离子方程式:_____________________。
(3)该小组拟以“m (C1O2) /m (NaC1O3) ”作为衡量C1O2产率的指标。若取NaC1O3样品6.0g,通过反应和吸收获得400mL C1O2溶液,取此溶液20mL与37.00mL0.500 mol·L-1 (NH4)2Fe (SO4)2溶液充分反应后,过量的Fe2+再用0.0500 mol·L-1 K2Cr2O7标准溶液滴定至终点,消耗K2Cr2O7标准溶液20.00mL。反应原理为:
4H++ C1O2+5Fe2+=Cl-+5Fe3++2H2O
14H++ Cr2O72-+6Fe2+=2Cr3++6Fe3++7H2O
试计算C1O2的“产率”_______________(写出计算过程)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com