
【题目】一定温度下,向恒容容器中充入amolH2和amolI2蒸气,发生反应H2(g)+I2(g)![]() 2HI(g).下列能判断该反应达到平衡状态的是
2HI(g).下列能判断该反应达到平衡状态的是
A. 混合气体的平均分子质量不再发生改变
B. 每断裂1molH-H键的同时就生成2molI-H键
C. 容器中混合气体的颜色不变
D. H2和I2的体积分数相等
科目:高中化学 来源: 题型:
【题目】分类法是学习和研究化学的一种重要方法。下列分类不合理的是( )
A.CaO和SO3都属于氧化物
B.K2SO4和KHCO3都属于盐
C.KOH和Na2CO3都属于碱
D.H2SO4和H3PO4都属于酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知NA为阿伏加德罗常数的数值,下列说法正确的是( )
A. 27g Al与NaOH完全反应,转移的电子数为0.1NA
B. 1L 1mol/L CaC12溶液中含有的Cl-离子数目为NA
C. 标准状况下,22.4L水含有1mol水分子
D. 2mol钠与过量稀盐酸反应生成NA个氢气分子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,在没有氧气存在时,铁粉与水几乎不反应,但在高温下,铁粉能与水蒸气反应。
(1)铁粉与水蒸气反应的化学方程式是________________________________。
(2)停止反应,待装置冷却后,取出反应后的混合物,加入过量的稀硫酸充分反应,过滤。简述检验所得滤液中含有Fe3+的操作方法:______________________________。
(3)经检验上述滤液中不含Fe3+,这不能说明铁粉与水蒸气反应所得的产物中不含+3价的铁,原因是(结合化学方程式说明)___________________。
(4)向上述滤液中加入NaOH 溶液后,观察到的现象为_______________________。沉淀由白色变为红褐色的原因是______________________________________(用化学方程式表示)
(5)为了得到白色的Fe(OH)2沉淀,并尽可能可能较长时间保持白色沉淀,该同学设计了如图所示的装置,请简述实验操作:______________________________________________________。
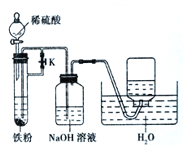
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室欲测定铁铝合金的组成,将铁铝合金溶解后,取试样25.00mL,分离并测定Fe3+的浓度,实验方案设计如下:

已知:乙醚易挥发,易燃烧。
回答下列问题:
(1)常温下,将铁铝合金溶解的试剂是_________(填字母)。
a.稀盐酸 b.稀硫酸 c.稀硝酸 d.浓硝酸
(2)已知氢氧化铁实际上是三氧化二铁的水合物,则通过称量氢氧化铁固体质量的方法来确定c(Fe3+)时,该方案理论上的主要缺点是________________________。
(3)操作X是___________________________,操作X后检验溶液中是否有Fe3+残留的方法是_______________________________。
(4)蒸馏装置如图所示,装置中存在的错误是___________________________。
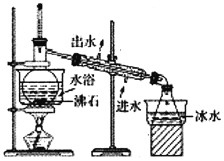
(5)将含Fe3+的溶液定容至100mL需要的仪器是___________________________。
(6)已知滴定反应为Ce4++Fe2+=Ce3++Fe3+,当滴定达到终点时,消耗0.1000 mol·L-1Ce(SO4)2溶液15.00 mL,则开始试样中c(Fe3+)=_____________。若改用稀硫酸酸化的K2Cr2O7溶液滴定含Fe2+的待测液,则该过程的离子反应方程式为_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,分别向两杯100mL的水中逐渐加入少量NH4Cl和NaOH固体,溶液的pH变化如图所示。下列判断正确的是

A. X代表NaOH,Y代表NH4Cl
B. pH变化相同时,n(NH4Cl)<n(NaOH)
C. 两份溶液的Kw均大于1.0×10-14
D. 若两杯溶液混合后呈中性,则加入的n(NH4Cl)和n(NaOH)不相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】超氧化钾KO2也和过氧化钠一样,吸收CO2变成碳酸盐并放出O2 . 若有0.5molKO2与过量CO2反应,则产生O2的物质的量为( )
A.0.125mol
B.0.375mol
C.0.5mol
D.0.75mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示是高炉炼铁的示意图。已知反应:
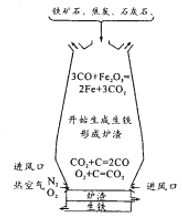
①2Fe2O3(s)+3C(s)![]() 4Fe(s)+3CO2(g) ΔH1=+468kJ/mol
4Fe(s)+3CO2(g) ΔH1=+468kJ/mol
②C(s)+CO2(g)![]() 2CO(g) ΔH2=+172.7 kJ/mol
2CO(g) ΔH2=+172.7 kJ/mol
(1)反应 ③Fe2O3(s)+3CO(g)![]() 2Fe(s)+3CO2(g) ΔH3=_________
2Fe(s)+3CO2(g) ΔH3=_________
(2)高炉炼铁中,存在可逆反应,增大高炉高度,能否减少尾气中CO排放比例?____(填“能”或“否”);能够减小高炉尾气中CO排放比例的措施是_______(举出一条)。
(3)一定温度下,某容器中加人足量的Fe2O3和C,发生反应:2Fe2O3(s)+3C(s)![]() 4Fe(s)+3CO2(g),达到平衡,下列说法错误的是_________(填序号)。
4Fe(s)+3CO2(g),达到平衡,下列说法错误的是_________(填序号)。
A.将容积压缩为原来的一半,再次达平衡时,CO2的浓度为原来的2倍
B. 向容器中再加Fe2O3,可以提高反应的速率
C.将体积变为原来的2倍,再次达平衡时,气体的密度不变
D.保持容器体积不变,充入He,平衡逆向移动
(4)为了消除CO对空气的污染,常温下将CO通入PdCl2的水溶液中,将其转化为无毒的气体并得到Pd单质。反应的化学方程式为____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验现象描述正确的是( )
A.二氧化碳气体通入无色酚酞溶液,溶液变红色
B.细铁丝在氧气里剧烈燃烧,火星四射
C.点燃棉线闻到一股烧焦的羽毛味
D.打开浓盐酸试剂瓶的瓶塞,瓶口上方出现大量白烟
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com