
【题目】化学反应过程中发生物质变化的同时,常常伴有能量的变化.这种能量的变化常以热能的形式表现出来,叫做反应热.由于反应的情况不同,反应热可以分为许多种,如燃烧热和中和热等.
(1)下列△H表示物质燃烧热的是;表示物质中和热的是 .
A.2H2(g)+O2(g)=2H2O(l);△H1
B.C(s)+ ![]() O2(g)=CO(g);△H2
O2(g)=CO(g);△H2
C.CH4(g)+2O2(g)=CO2(g)+2H2O(g);△H3
D.C(s)+O2(g)=CO2(g);△H4
E.C6H12O6(s)+12O2(g)=6CO2 (g)+6H2O (l);△H5
F.NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l);△H6
G.2NaOH(aq)+H2SO4(aq)=Na2SO4(aq)+2H2O(l);△H7
H.CH3COOH(aq)+NaOH(aq)=CH3COONa(aq)+H2O(l);△H8
(2)甲硅烷(SiH4)是一种无色液体,遇到空气能发生爆炸性自燃,生成SiO2和水.已知室温下10g甲硅烷自燃放出热量446kJ,表示其燃烧热的热化学方程式为 .
(3)使Cl2和H2O(g)通过灼热的炭层,生成HCl和CO2是放热反应,当1molCl2参与反应时释放145kJ的热量,写出这个热化学方程式: .
【答案】
(1)△H4、△H5;△H6
(2)SiH4(g)+O2(g)=SiO2(g)+2H2O(l)△H=﹣1427.2kJ/mol
(3)2Cl2(g)+2H2O(g)+C(s)═4HCl(g)+CO2(g)△H=﹣290kJ?mol﹣1
【解析】(1)A.氢气的物质的量为2mol,反应热△H1不能表示燃烧热,
B.碳燃烧的生成物为CO,表示温度的氧化物CO2 , 反应热△H2不能表示燃烧热,
C.1mol甲烷完全燃烧,生成的水是气态,不是稳定的状态,应为液态水,故反应热△H3不能表示燃烧热,
D.C(s)+O2(g)═CO2(g)△H4中1molC完全燃烧生成二氧化碳,符合燃烧热概念,反应热△H4能表示燃烧热,
E.C6H12O6(s)+6O2(g)═6CO2(g)+6H2O(l)△H5中1molC6H12O6完全燃烧生成二氧化碳与液态水,符合燃烧热概念,反应热△H5能表示燃烧热,
F.NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(l)△H6中实质是1mol氢离子与1mol氢氧根离子反应生成1molH2O,符合中和热概念,反应热△H6能表示中和热,
G.反应生成的水为2mol,反应热△H7不能表示中和热,
H.CH3COOH(aq)+NaOH(aq)=CH3COONa(aq)+H2O(l)中,醋酸是弱酸,不能表示中和热.
所以答案是:△H4、△H5;△H6;(2)n(SiH4)=![]() , 则1molSiH4燃烧放出的热量为:446kJ×
, 则1molSiH4燃烧放出的热量为:446kJ× ![]() =1427.2kJ,
=1427.2kJ,
反应的化学方程式为:SiH4+O2=SiO2+2H2O,则热化学方程式为:SiH4(g)+O2(g)=SiO2(g)+2H2O(l)△H=﹣1427.2kJ/mol,
所以答案是:SiH4(g)+O2(g)=SiO2(g)+2H2O(l)△H=﹣1427.2kJ/mol;(3)使Cl2和H2O(g)通过灼热的炭层,生成HCl和CO2是放热反应,当1mol Cl2参与反应时释放145kJ的热量,2mol氯气完全反应放热290 kJ,热化学方程式为2Cl2(g)+2H2O(g)+C(s)═4HCl(g)+CO2(g)△H=﹣290 kJmol﹣1 ,
所以答案是:2Cl2(g)+2H2O(g)+C(s)═4HCl(g)+CO2(g)△H=﹣290 kJmol﹣1 .
【考点精析】关于本题考查的燃烧热和中和热,需要了解在101kPa时1mol H2物质完全燃烧生成稳定的氧化物时所放出的能量,叫该物质的燃烧热;在稀溶液中,酸和碱发生中和反应而生成1mol H2O,这时的反应热叫做中和热才能得出正确答案.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】羟氨苄青霉素是高效、广谱和低毒的抗生素,其结构简式如图所示.下列说法不正确的是( ) 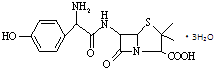
A.羟氨苄青霉素在空气中不能稳定存在
B.每个羟氨苄青霉素分子中含有3个手性碳原子
C.羟氨苄青霉素既能与盐酸反应,又能与碳酸氢钠溶液反应
D.1mol羟氨苄青霉素与氢氧化钠溶液反应时,最多消耗4molNaOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中W原子的最外层电子数是最内层电子数的3倍.下列判断正确的是( ) 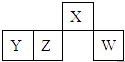
A.原子半径:W>Z>Y>X
B.含Y元素的盐溶液一定显酸性
C.最简单气态氢化物的热稳定性:Z>W
D.X与氢元素组成的化合物XH5与水反应可产生两种气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有下列九种物质:①盐酸 ②石墨 ③蔗糖 ④CO2 ⑤熔融NaHSO4 ⑥Ba(OH)2固体 ⑦氨水 ⑧硫酸 ⑨明矾
(1)属于电解质的有;属于非电解质的有;能导电的物质有 .
(2)②和SiO2在高温下可发生如下反应:3C+SiO2 ![]() SiC+2CO,上述反应中还原产物是;氧化剂与还原剂物质的量之比为 .
SiC+2CO,上述反应中还原产物是;氧化剂与还原剂物质的量之比为 .
(3)上述九种物质中有两种物质之间可发生离子反应:H++OH﹣═H2O,该离子反应对应的化学方程式为
(4)⑤的电离方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据如图,可判断出下列离子方程式中错误的是( )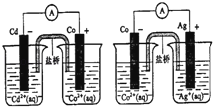
A.2Ag+(aq)+Cd(s)=2Ag(s)+Cd 2+(aq)
B.Co2+(aq)+Cd(s)=Co(s)+Cd2+(aq)
C.2Ag(s)+Cd2+(aq)=2Ag+(aq)+Cd(s)
D.2Ag+(aq)+Co(s)=2Ag(s)+Co2+(aq)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有m g某气体,它由四原子分子构成,它的摩尔质量为M gmol﹣1 , 则:
(1)该气体的物质的量为mol.
(2)该气体中所含的原子总数为个.
(3)该气体在标准状况下的体积为L.
(4)该气体溶于1L水中(不考虑反应),其溶液中溶质的质量分数为 .
(5)该气体溶于水后形成V L溶液,其溶液的物质的量浓度为molL﹣1 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图,水槽中试管内有一枚铁钉,放置数天观察,铁钉有明显生锈的迹象: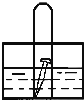
(1)若试管内液面上升,则溶液呈性,电极反应式为:正极
(2)若试管内液面下降,则溶液呈性,电极反应式为:正极 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com