
【题目】某有机物其结构简式如图,关于该有机物,下列叙述不正确的是( )
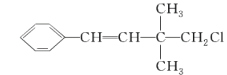
A.该物质分子中含有氯原子,不属于烃类
B.1 mol 该有机物能与溴的四氯化碳溶液发生加成反应反应,消耗 1 mol Br2
C.该物质与苯互为同系物
D.该物质在一定条件下,能发生加聚反应
科目:高中化学 来源: 题型:
【题目】实验室按如下装置测定纯碱(含少量NaC1)的纯度。下列说法不正确的是
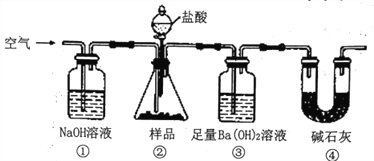
A. 滴入盐酸前,应将装置中含有CO2的空气排尽
B. 装置①、④的作用是防止空气中的CO2进入装置③
C. 必须在装置②、③间添加盛有饱和 NaHCO3溶液的洗气瓶
D. 反应结束时,应再通入空气将装置②中CO2转移到装置③中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】归纳法是高中化学学习常用的方法之一,某化学研究性学习小组在学习了《化学反应原理》后作出了如下的归纳总结:归纳正确的是
①对已建立化学平衡的某可逆反应,当改变条件使化学平衡向正反应方向移动时,生成物的产量一定增加
②常温下,pH=3的醋酸溶液与pH=11的NaOH溶液等体积混合后形成溶液a,等浓度的盐酸与NaOH溶液等体积混合后形成溶液b,水的电离程度a>b。
③常温下,AgCl在同物质的量浓度的氨水和NaCl溶液中的溶解度比较,前者大。
④若将适量CO2通入0.1 mol/LNa2CO3溶液中至溶液恰好呈中性,则溶液中(不考虑溶液体积变化) 2c(CO32-)+ c(HCO3ˉ)= 0.1 mol/L
⑤常温下,已知醋酸电离平衡常数为Ka;醋酸根水解平衡常数为Kh;水的离子积为Kw;则有:Ka·Kh=Kw
A.①②④⑤B.②④⑤C.②⑤D.①③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A.破坏乙烯分子里![]() 所需吸收的能量是破坏乙烷分子里 C—C 能量的两倍
所需吸收的能量是破坏乙烷分子里 C—C 能量的两倍
B.乙烯分子和苯分子都能使溴水褪色,两者褪色原理相同
C.因为甲烷和苯都不能被酸性 KMnO4 溶液氧化,所以两者都不能发生氧化反应
D.甲烷和苯都能和氯气发生取代反应,但是两者发生反应时需要的条件不同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】砷化镓(GaAs)灯泡寿命是普通灯泡的100倍,而耗能即为10%,推广砷化镓(GaAs)、 氮化镓(GaN)等发光二极管(LED)照明,是节能减排的有效举措。请回答下列问题:
(1)基态N原子核外电子排布图为 _____________________ ;Ga与Al同主族,且位于Al的下一周期,则基态Ga原子的价电子排布式为 ________________。
(2)Ga的电负性比As______(填“大”或“小”);Ga逐级失去电子的电离能 (单位:kJ·mol-1)的数值依次为577、1985、2962、6192,由此可推知Ga的主要化合价为__和+3。
(3)比较下列Ga的卤化物的熔点和沸点, GaCl3、GaBr3、GaI3的熔、沸点依次升高, 分析其变化的原因是:_____________________________________________________。
镓的卤化物 | GaCl3 | GaBr3 | GaI3 |
熔点/℃ | 77.75 | 122.3 | 211.5 |
沸点/℃ | 201.2 | 279 | 346 |
GaF3的熔点超过1000℃,可能的原因是____________________________。
(4)GaAs是将(CH3)3Ga和AsH3用金属有机物化学气相淀积方法制备得到,该反应在700℃下进行
①则该反应的化学方程式为:____________________________________________。
②反应物AsH3分子的几何构型为________________,(CH3)3Ga中镓原子杂化方式为____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将 A、B 置于固定容积为 1L 的密闭容器中,发生反应:3A(g)+B(g)2C(g)+2D(g),反应进行到 10 s 末,测得 A 的物质的量为 1.8 mol,B 的物质的量为 0.6 mol,C 的物质的量为 0.8 mol,下列说法错误的是( )
A.用 C 表示 10 s 内反应的平均反应速率为 0.8 molL-1s-1
B.反应前 A 的物质的量浓度是 3 molL-1
C.10 s 末,生成物 D 的物质的量为 0.8 mol
D.保持其他条件不变,适当升高温度,正逆反应速率都加快
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】燃烧法是测定有机物分子式的一种重要方法。完全燃烧 0.1mol 某烃后,测得生成的二氧化碳为 11.2 L(标准状况),生成的水为 10.8g。请完成下面的填空:
(1)该烃的分子式为_________。
(2)写出它可能存在的全部物质的的结构简式 :_________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝元素在自然界中主要存在于铝土矿(主要成分为Al2O3,还含有Fe2O3、FeO、SiO2)中。工业上用铝土矿制备铝的某种化合物的工艺流程如下。
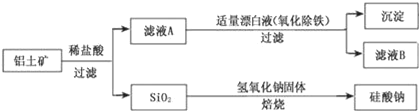
(1)在滤液A中加入漂白液,目的是氧化除铁,所得滤液B显酸性。
①该过程中涉及某氧化还原反应如下,请完成:__Fe2+___ClO-+( )___=____Fe(OH)3↓+__C1﹣+( )。
②检验滤液B中是否还含有铁元素的方法为:________(注明试剂、现象)。
③将滤液B中的铝元素以沉淀形式析出,可选用的最好试剂为___(填代号)。
a.氢氧化钠溶液 b.硫酸溶液 c.氨水 d.二氧化碳
④由滤液B制备氯化铝晶体涉及的操作为:边滴加浓盐酸边蒸发浓缩、冷却结晶、____(填操作名称)、洗涤。
(2)SiO2和NaOH焙烧制备硅酸钠,可采用的装置为___(填代号)。
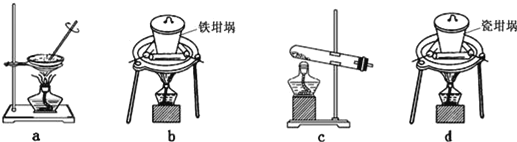
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】聚合物L具有特殊的光学性质,可用于光电材料,其合成路线如下:
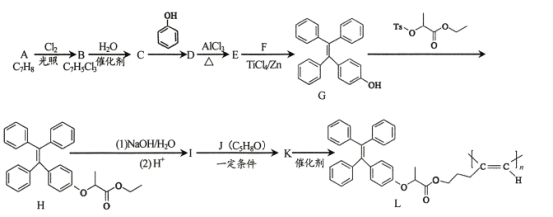
已知:
i.有机物可用键线式表示,如![]() 可表示为
可表示为
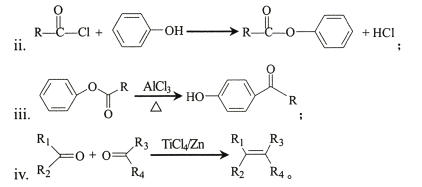
(1) A—B的化学方程式为____。
(2)D的结构简式为____。
(3)E中含有的含氧官能团为____ 。
(4) G—H的反应类型为____。
(5)I—K的化学方程式为____。
(6)下列说法正确的是______填字母序号)。
a.A分子中所有碳原子均在同一平面 b.C的结构简式为![]()
c.F+F—G的副产物中有2种互为顺反异构体 d.1 mol H最多能与2 molNaOH反应
(7)乳酸乙酯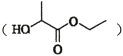 是合成
是合成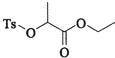 的中间体。下图是某同学设计的合成乳酸乙酯的流程。
的中间体。下图是某同学设计的合成乳酸乙酯的流程。
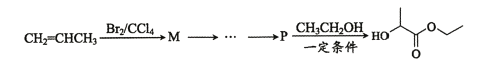
请写出M-P的合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com