
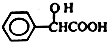 .工业上扁桃酸可以由烃A经过以下步骤合成得到:
.工业上扁桃酸可以由烃A经过以下步骤合成得到: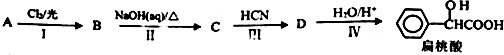
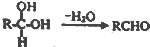
 ;扁桃酸中含氧官能团名称羟基、羧基.
;扁桃酸中含氧官能团名称羟基、羧基. .
. )在浓硫酸作用下反应生成,请写出反应的化学方程式
)在浓硫酸作用下反应生成,请写出反应的化学方程式
 .
.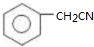 )为原料合成扁桃酸的同分异构体-对羟基苯乙酸(
)为原料合成扁桃酸的同分异构体-对羟基苯乙酸(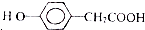 )的合理路线.
)的合理路线.分析 D发生水解反应生成扁桃酸,根据信息③知,D结构简式为 ,C和HCN发生加成反应生成D,C结构简式为
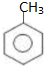
,C和HCN发生加成反应生成D,C结构简式为 ,A为烃且碳氢的质量比为21:2,A中C、H原子原子之比=$\frac{21}{12}$:$\frac{2}{1}$=7:8,A为苯的同系物,则A为甲苯,A结构简式为
,A为烃且碳氢的质量比为21:2,A中C、H原子原子之比=$\frac{21}{12}$:$\frac{2}{1}$=7:8,A为苯的同系物,则A为甲苯,A结构简式为 ,A和氯气发生取代反应生成B,B发生取代反应生成苯甲醛,根据信息②知,B结构简式为
,A和氯气发生取代反应生成B,B发生取代反应生成苯甲醛,根据信息②知,B结构简式为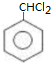 ,结合题目分析解答.
,结合题目分析解答.
解答 解:D发生水解反应生成扁桃酸,根据信息③知,D结构简式为 ,C和HCN发生加成反应生成D,C结构简式为
,C和HCN发生加成反应生成D,C结构简式为 ,A为烃且碳氢的质量比为21:2,A中C、H原子原子之比=$\frac{21}{12}$:$\frac{2}{1}$=7:8,A为苯的同系物,则A为甲苯,A结构简式为
,A为烃且碳氢的质量比为21:2,A中C、H原子原子之比=$\frac{21}{12}$:$\frac{2}{1}$=7:8,A为苯的同系物,则A为甲苯,A结构简式为 ,A和氯气发生取代反应生成B,B发生取代反应生成苯甲醛,根据信息②知,B结构简式为
,A和氯气发生取代反应生成B,B发生取代反应生成苯甲醛,根据信息②知,B结构简式为 ,
,
(1)通过以上分析知,A的结构简式为 ;扁桃酸中含氧官能团名称为羟基、羧基,故答案为:
;扁桃酸中含氧官能团名称为羟基、羧基,故答案为: ;羟基、羧基;
;羟基、羧基;
(2)通过以上分析知,Ⅰ、Ⅲ的反应类型分别是取代反应、加成反应,故答案为:取代反应;加成反应;
(3)C结构简式为 ,C与新制的氢氧化铜悬浊液发生氧化反应,该反应的化学方程式为
,C与新制的氢氧化铜悬浊液发生氧化反应,该反应的化学方程式为 ,
,
故答案为: ;
;
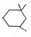
(4)环扁桃酸酯可由扁桃酸和3,3,5-三甲基环乙醇(HO- )在浓硫酸作用下发生酯化反应生成,该反应的化学方程式为
)在浓硫酸作用下发生酯化反应生成,该反应的化学方程式为 ,
,
故答案为: ;
;
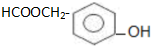
(5)扁桃酸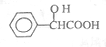 ,扁桃酸的同分异构体符合下列条件:①溶液遇到Fe3+显紫色说明含有酚羟基,②能发生银镜反应说明含有醛基,③能在NaOH溶液中发生水解反应说明含有酯基,④核磁共振氢谱有5个吸收峰,说明含有5种氢原子,符合条件的同分异构体结构简式为
,扁桃酸的同分异构体符合下列条件:①溶液遇到Fe3+显紫色说明含有酚羟基,②能发生银镜反应说明含有醛基,③能在NaOH溶液中发生水解反应说明含有酯基,④核磁共振氢谱有5个吸收峰,说明含有5种氢原子,符合条件的同分异构体结构简式为 ,
,
故答案为: ;
;
(6)苯乙氰和浓硝酸发生取代反应生成对硝基苯乙氰,对硝基苯乙氰和浓盐酸反应生成对硝基苯乙酸,对硝基苯乙酸和Fe、浓盐酸反应生成对氨基苯乙酸,对氨基苯乙酸亚硝酸钠、硫酸反应生成对羟基苯乙酸,其流程图为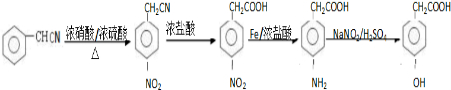 ,
,
故答案为: .
.
点评 本题考查有机合成,为高考高频点,侧重考查学生分析推断、知识迁移及知识综合应用能力,根据流程图中物质结构变化及反应条件进行推断,熟悉常见有机反应类型及反应条件,难点是合成路线的设计,题目难度中等.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
 .
. 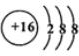 ;D与E能形成一种所有原子最外层均满足8电子的分子,该分子的结构式为S=C=S;D所在族元素的氢化物中,沸点最低的是H2S.
;D与E能形成一种所有原子最外层均满足8电子的分子,该分子的结构式为S=C=S;D所在族元素的氢化物中,沸点最低的是H2S.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
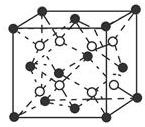 有A、B、C、D、E五种原子序数依次增大的元素(原子序数均小于30).A的基态原子2p能级有3个单电子;C的基态原子2p能级有1个单电子;E原子最外层有1个单电子,其次外层有3个能级且均排满电子;D与E同周期,价电子数为2.则:
有A、B、C、D、E五种原子序数依次增大的元素(原子序数均小于30).A的基态原子2p能级有3个单电子;C的基态原子2p能级有1个单电子;E原子最外层有1个单电子,其次外层有3个能级且均排满电子;D与E同周期,价电子数为2.则:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
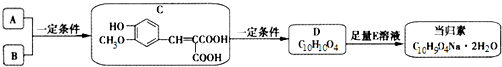
 .
. .
.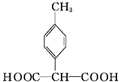 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | m=1,n=5 | B. | m=3,n=4 | C. | m=5,n=1 | D. | m=3,n=3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 配制CuCl2溶液时,将CuCl2(s)溶于浓HCl后再加水冲稀,浓盐酸作用:有利于抑制CuCl2水解,可防止Cu(OH)2的形成 | |
| B. | 加热MnO2的浓HCl溶液制取氯气.浓盐酸作用:有利于减少氯气的溶解损失 | |
| C. | 浓硝酸不能溶解金,需用浓HCl溶液配制王水才能溶解金.浓盐酸作用:有利于增强Au的还原性,并且提高硝酸的氧化性 | |
| D. | 将浓硫酸滴入浓盐酸中制备HCl气体.浓盐酸作用:增大溶质的浓度,有利于促进平衡向气体溶解的逆方向移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
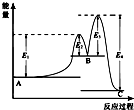 某反应由两步反应A═B═C构成,它的反应能量曲线如图所示(E1、E2、E3、E4表示活化能).下列有关叙述正确的是( )
某反应由两步反应A═B═C构成,它的反应能量曲线如图所示(E1、E2、E3、E4表示活化能).下列有关叙述正确的是( )| A. | A═B的反应热△H=+(E2-E1)KJ/mol | B. | 三种化合物中C最稳定 | ||
| C. | C═B 是放热反应 | D. | 整个反应中△H=E1-E4 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
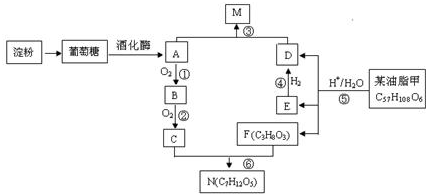
 ;C与F按不同的比例,还可以生成另外两种物质X、Y,且相对分子量X<N<Y,则Y的分子式C9H14O6.
;C与F按不同的比例,还可以生成另外两种物质X、Y,且相对分子量X<N<Y,则Y的分子式C9H14O6. C17H35COOCH2CH3+H2O.
C17H35COOCH2CH3+H2O.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com