
| A. | S2-和HS- | B. | H3O+和OH- | C. | Na+和NH${\;}_{4}^{+}$ | D. | K+和Ne |
分析 利用阳离子中的核外电子数为质子数之和减去电荷数,阴离子中的核外电子数为质子数之和加上微粒的电荷数,分子中的核外电子数之和=质子数之和来解答.
解答 解:A、S2-的质子数为16,核外电子总数为18,HS-的质子数为17,核外电子总数为18,故A错误;
B、H3O+的质子数为19,核外电子总数为18,OH-的质子数为17,核外电子总数为18,故B错误;
C、Na+的质子数为11,核外电子总数为10,NH4+的质子数为11,核外电子总数为10,故C正确;
D、K+的质子数为19,核外电子总数为18,Ne的质子数为10,核外电子总数为10,故D错误;
故选:C.
点评 本题主要考查了微粒中质子数和电子数的计算,根据微粒的构成情况确定质子数和电子数,题目难度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | 可加入硫酸以提高电解质的导电性 | |
| B. | 放电时电池内部Li+向负极移动 | |
| C. | 充电过程中,电池正极材料的质量增加 | |
| D. | 放电时电池正极反应为:FePO4+Li++e-═LiFePO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,40 g SO3所含的氧原子的数目为1.5 NA | |
| B. | 5.6 g铁与足量氯气或硫蒸气反应转移的电子数均为0.3 NA | |
| C. | 12.5 mL 16 mol•L-1浓硫酸与足量铜反应,生成SO2的分子数为0.1 NA | |
| D. | 常温下5.6 g铁投入到足量浓硝酸中反应,转移电子数为0.3 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 mol•L-1甲酸溶液的pH约为2 | |
| B. | 甲酸能与水以任意比例互溶 | |
| C. | 10 mL 1 mol•L-1甲酸恰好与10 mL 1 mol•L-1 NaOH溶液完全反应 | |
| D. | 甲酸溶液的导电性比强酸溶液弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ;DB2有多种重要的用途,请你写出其中的一种:制玻璃、制光导纤维、制粗硅(其中一种).
;DB2有多种重要的用途,请你写出其中的一种:制玻璃、制光导纤维、制粗硅(其中一种).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| D | ||
| A | B | C |
| E |
| A. | 5Z | B. | 5Z+8 | C. | 5Z+10 | D. | 5Z+18 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 元素 | X | Y | Z | W |
| 相关信息 | 短周期p区元素,有种单质常作电极材料 | 基态原子2p能级上各轨道中均有电子且电子的自旋方向相同 | 基态原子的核外电子共有17种运动状态 | 位于第四周期第VA族 |
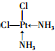 (YH3作为一个整体写)
(YH3作为一个整体写)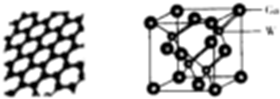
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com