
 ��Ȼ���д��ڴ����Ľ���Ԫ�أ��� ���ơ�þ����������ͭ���ڹ�ũҵ���������Ź㷺��Ӧ�ã�
��Ȼ���д��ڴ����Ľ���Ԫ�أ��� ���ơ�þ����������ͭ���ڹ�ũҵ���������Ź㷺��Ӧ�ã�| �����ܣ�kJ/mol�� | I1 | I2 | I3 | I4 |
| A | 932 | 1821 | 15390 | 21771 |
���� ��1������26��Ԫ�أ����ݺ�������Ų����ɣ�����д�����̬ԭ�Ӻ�������Ų�ʽ��
��2���ӱ���ԭ�ӵĵ�һ�����ĵ����ܿ��Կ�����A�ĵڶ�������С��
��3����ͬһ����Ԫ�صĵ�һ����������ԭ�����������������������ƣ�����IIA��͵�VA��Ԫ�صĵ�һ�����ܴ�������Ԫ�أ�
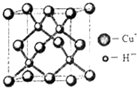
�ڸ��ݻ�����Ļ�ѧʽ�жϣ�һ��ͭ�������������������һ���ʻ����壬��4�����壻
�ۼ����ӻ�����ʱ���ݵ��Ӷ������жϣ�����ԭ�ӵļ۵�����������������ĺͳ���2�͵õ����Ӷ��������ݵ��Ӷ���������ȷ���ӻ����ͣ�
��4�����ӻ������о�����Խ�������������Խ�࣬�۷е�Խ�ߣ��ȵ�������ָ������ͬ�۵���������ԭ�������ķ��ӻ����ӣ�
��5�����ݼ۲���ӶԻ�������ȷ��Nԭ�ӵļ۲���Ӷ�������ȷ���ӻ����͡����ӿռ乹�ͣ�
��6�����ݾ�̯������һ�������и�ԭ�ӵ���Ŀ�����ݾ����ܶ�$��=\frac{m}{V}$���㣮
��� �⣺��1������26��Ԫ�أ����ݺ�������Ų����ɣ�����д�����̬ԭ�Ӻ�������Ų�ʽ��1s22s22p63s23p63d64s2��[Ar]3d64s2��
�ʴ�Ϊ��1s22s22p63s23p63d64s2��[Ar]3d64s2��
��2���ӱ���ԭ�ӵĵ�һ�����ĵ����ܿ��Կ�����A�ĵڶ�������С�����������ܽϴ�˵����ʧȥ2�����ӣ���A�Ļ��ϼ�Ϊ+2�ۣ�ӦΪMgԪ�أ��۵����Ų�Ϊ3s2���ʴ�Ϊ��3s2��
��3����ͬһ����Ԫ�صĵ�һ����������ԭ�����������������������ƣ�����IIA��͵�VA��Ԫ�صĵ�һ�����ܴ�������Ԫ�أ�����C��N��O����Ԫ�صĵ�һ��������С�����˳��Ϊ��C��O��N���ʴ�Ϊ��C��O��N��
��һ��ͭ�������������������һ���ʻ����壬��4�����壬�ʴ�Ϊ��4��
������ԭ��Ϊ̼���۵�����Ϊ4������Ϊ����ԭ�ӣ����ṩ���ӣ�ÿ���ǰ����ṩһ�����ӣ����Ӷ���Ϊ��4+1��2����2=3�����ӻ����Ϊsp2����ԭ���γ���3���Ҽ���ͬʱ����һ�Թµ��ӣ����Ӷ���Ϊ3+1=4�����ӻ����Ϊsp3���Ҽ�����ĿΪ3��ÿ���ǰ����ЦҼ�����Ŀ2��һ���������к��Ҽ�����ĿΪ3+2��2=7����ÿĦ�������к��ЦҼ�����ĿΪ7NA��
�ʴ�Ϊ��sp2��sp3��7��
��4��MgO�����Ӷ���2����λ��ɣ�NaCl�����Ӷ���1����λ��ɣ����Ӱ뾶Cl-��O2-��Mg2+��Na+���ۻ�����ľ�����Զ���ڵͼ����ӻ�����ľ�������MgO��NaCl�����۵�MgO��NaCl���ʴ�Ϊ��MgO�����������Ӱ뾶С��������࣬�����ܴ�
��5��NH4+��Nԭ�ӵļ۲���Ӷ���Ϊ4+$\frac{1}{2}$��5-1-4��1��=4������û�йµ��Ӷԣ��������ӵĿռ乹��Ϊ�������壻NO3-ԭ����Ϊ4���۵�����Ϊ24������ȵ�����Ϊ��SO3����BF3��
�ʴ�Ϊ���������壻SO3����BF3��
��6��һ��������Cuԭ����ĿΪ$8��\frac{1}{8}$+6��$\frac{1}{2}$=4��Hԭ����ĿΪ4�������ܶ�$��=\frac{m}{V}$=$\frac{\frac{65��4}{{N}_{A}}}{{a}^{3}}$=$\frac{260}{{a}^{3}•{N}_{A}}$g/cm3���ʴ�Ϊ��$\frac{260}{{a}^{3}•{N}_{A}}$��
���� ���⿼����ԭ�ӵ��ӻ���ʽ����������Ų�ʽ����д�������۷е���жϵ�֪ʶ�㡢�������㣬���е����Ų�ʽ��ԭ�ӵ��ӻ���ʽ�Ǹ߿����ȵ㣬��ѧϰ���ص㣮



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1�� | B�� | 2�� | C�� | 3�� | D�� | 4�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���Ȼ�����Һ��ʴͭ�壺Cu+Fe3+�TCu2++Fe2+ | |
| B�� | ��ˮ��ͨ��������SO2��I2+SO2+2H2O�T2I-+SO42-+4H+ | |
| C�� | ��������Һ�еμӹ�����ˮ��Ag++NH3•H2O�TAgOH��+NH4+ | |
| D�� | 0.5mol/LNaHSO4��0.5mol/LBa��OH��2�������Һ�����ԣ�Ba2++OH-+SO42-+H+�TBaSO4��+H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Cl•�ڷ�Ӧ���Ǵ��� | |
| B�� | Cl•��Cl2������ | |
| C�� | ��Ҳ������Cl•��g��+CH4��g����CH3Cl��g��+H•��g�� | |
| D�� | �ɢۿ�֪C-Cl�ļ��ܱ�Cl-Cl�ļ���С |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 50��ʱ���ⶨijNaNO2��Һ��pH=8������Һ��c��Na+��-c��NO2-��=9.9��10-7mol•L-1 | |||||||||
| B�� | NaHSO3ˮ��Һ�д��ڹ�ϵ��c��H2SO3��+c��H+��=c��OH-��+c��SO32-��+c��HSO3-�� | |||||||||
| C�� | һ���¶��£�����pH�Ʋⶨ��ͬŨ�ȴ�����Һ��pHֵ���õ��������ݣ�
| |||||||||
| D�� | ��֪25��ʱ���й�������ʵĵ���ƽ�ⳣ����HCN��Ka=4.9��10-10��H2CO3��Ka1=4.3��10-7Ka2=5.6��10-11����CO2ͨ��NaCN��Һ�з�Ӧ�Ļ�ѧ����ʽΪ��2NaCN+H2O+CO2=2HCN+Na2CO3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��
��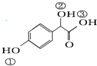 ���Т١��ڡ��ۣ������ұ�ţ�3��-OH������������ǿ��˳���ǣ��ۣ��٣��ڣ�
���Т١��ڡ��ۣ������ұ�ţ�3��-OH������������ǿ��˳���ǣ��ۣ��٣��ڣ��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
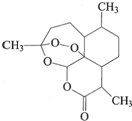 �й�ҩѧ�������ϻ��2015��ŵ��������ҽѧ������������������--һ����������ű����ҩ������ȫ���������˵������������صĽṹ��ͼ��ʾ�������й������ص�˵������ȷ���ǣ�������
�й�ҩѧ�������ϻ��2015��ŵ��������ҽѧ������������������--һ����������ű����ҩ������ȫ���������˵������������صĽṹ��ͼ��ʾ�������й������ص�˵������ȷ���ǣ�������| A�� | ����ʽΪC15H22O5 | |
| B�� | ���������ѵ��л��ܼ� | |
| C�� | �ɷ���ȡ����Ӧ�����ܷ���������Ӧ | |
| D�� | ��ǿ���ǿ������Һ�в����ȶ����� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com