
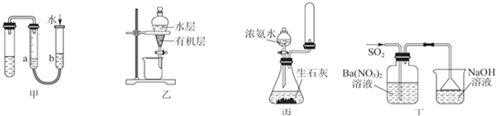
| A. | 用图甲的方法不能检查此装置的气密性 | |
| B. | 图乙可以作为CCl4萃取溴水后的分液装置 | |
| C. | 实验室用图丙所示装置制取少量氨气 | |
| D. | 图丁洗气瓶中的白色沉淀为BaSO3 |
分析 A.能产生压强差的装置能检验装置气密性;
B.四氯化碳能作溴水的萃取剂且密度大于水;
C.收集氨气时应该采用向下排空法,且收集时不能将试管口塞塞子;
D.二氧化硫能被硝酸钡氧化生成硫酸钡.
解答 解:A.能产生压强差的装置能检验装置气密性,该装置调节b装置时能产生压强差,所以可以来检验装置气密性,故A错误;
B.四氯化碳能作溴水的萃取剂且密度大于水,所以图乙可以作为CCl4萃取溴水后的分液装置,故B正确;
C.收集氨气时应该采用向下排空法,且收集时不能将试管口塞塞子,否则收集气体的试管中压强过大易产生安全事故,且导气管深入试管底部,故C错误;
D.二氧化硫能被硝酸钡氧化生成硫酸钡,所以生成的白色沉淀是硫酸钡而不是亚硫酸钡,故D错误;
故选B.
点评 本题考查化学实验方案评价,为高频考点,涉及气密性检验、萃取、气体的收集、氧化还原反应等知识点,明确实验原理、物质性质、实验操作是解本题关键,易错选项是C.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
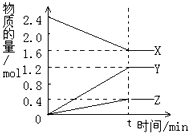 在2L容器中3种物质间进行反应,X、Y、Z的物质的量随时间的变化曲线如图.依图所示:
在2L容器中3种物质间进行反应,X、Y、Z的物质的量随时间的变化曲线如图.依图所示:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 由mXa+与nYb-得,m+a=n-b | |
| B. | 由mXa+与nYb-得X和Y不同周期 | |
| C. | X、Y一定不是同周期元素 | |
| D. | 若X离子是阴离子,则Y离子一定是阳离子 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
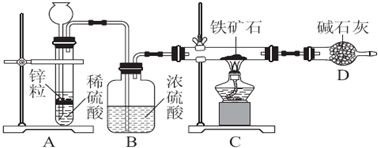
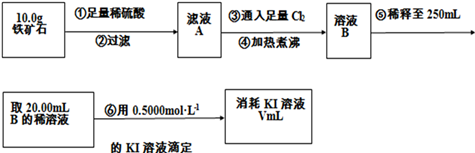
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 水属于氧化物 | B. | 水分子中含有非极性键 | ||
| C. | 冰与可燃冰的化学成分完全相同 | D. | 氟气与水的反应中,水作氧化剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Y位于元素周期表的第2周期第IVA族 | |
| B. | X、Y、Z、W、M的原子半径由大到小的顺序为M>Y>Z>W>X | |
| C. | X、Z、W形成的盐中只含有离子键 | |
| D. | 产生刺激性气味气体的反应离子方程式为H++HSO3-=H2O+SO2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,11.2L的CHCl3含有的分子数为0.5NA | |
| B. | 28gSi晶体中含有Si-Si键的个数为4NA | |
| C. | 常温下,78g某浓度的乙炔的苯溶液中含碳原子数为6NA | |
| D. | 0.1 molCnH2n+2中含有的碳碳单键数为0.1nNA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com