
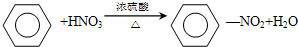
 ,该反应的类型是取代反应.
,该反应的类型是取代反应. 分析 (1)硫酸铜和氢氧化钠的混合液可反应生成氢氧化铜悬浊液,与尿液混合,加热后,若产生红色沉淀,说明含有醛基,进而说明含有葡萄糖;
(2)检验淀粉完全水解成葡萄糖,须证明无淀粉存在,碘水遇到淀粉会变蓝,如果淀粉溶液中加入碘水没有变化 则说明水解完全,无淀粉;
(3)①有机物分子中双键(或三键)两端的碳原子与其他原子或原子团直接结合生成新的化合物的反应为加成反应,根据烯烃与卤化氢发生加成反应得到卤代烃分析解答;
②有机物中的原子或原子团被其他的原子或原子团所代替生成新的化合物的反应叫取代反应,苯与浓硝酸在浓硫酸催化作用下发生取代反应生成硝基苯和水.
解答 解:(1)NaOH溶液和CuSO4溶液生成硫酸钠和氢氧化铜沉淀,溶液呈碱性,醛基能被氢氧化铜氧化生成羧酸,同时生成砖红色氧化铜沉淀,将NaOH溶液与CuSO4溶液加入某病人的尿液中,微热时如果观察到红色沉淀,则说明该病人的尿液含有醛基的物质葡萄糖,
故答案为:葡萄糖;
(2)淀粉遇碘变蓝色,在已经水解的淀粉溶液中滴加几滴碘液,溶液显蓝色,则证明淀粉没有完全水解;溶液若不显色,则证明淀粉完全水解.
故答案为:碘水;
(3)①乙烯和氯化氢反应生成氯乙烷,反应方程式为CH2=CH2+HCl→CH3CH2Cl,该反应中乙烯的双键两端的碳原子与氢原子和氯原子结合生成氯乙烷,所以属于加成反应,
故答案为:CH2=CH2+HCl→CH3CH2Cl;加成反应;
②在浓硫酸作催化剂、加热条件下,苯中的氢原子被硝基取代生成硝基苯,所以该反应属于取代反应,反应方程式为: ,
,
故答案为: ;取代反应.
;取代反应.
点评 本题考查了葡萄糖的性质、淀粉的水解程度的判断,反应方程式的书写及取代反应和加成反应的判断,明确新制氢氧化铜悬浊液可以检验醛基的存在,抓住若证明完全水解,加入碘水不变蓝,注意取代反应和加成反应的区别,题目难度不大.


 轻松课堂标准练系列答案
轻松课堂标准练系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ag乙烯和丙烯混合物中所含碳氢键数目为$\frac{a{N}_{A}}{7}$ | |
| B. | 常温常压下,18g重水中含有的中子数为8NA | |
| C. | 标准状况下,2.24LCl2与足量的铁反应转移的电子数目是0.3NA | |
| D. | 7.8gNa2O2中含有的阴离子数为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用水稀释0.1 mol/L的氨水,则溶液中$\frac{c(C{H}_{3}.{H}_{2}O)}{c(O{H}^{-})}$增大 | |
| B. | 在等体积等pH 的盐酸和醋酸两溶液中分别加入等质量的相同锌粒,若只有一种溶液中的锌粒有剩余,则该溶液一定是盐酸 | |
| C. | pH=3的盐酸和醋酸分别升高相同的温度,pH均不变 | |
| D. | 两种氨水溶液的物质的量浓度分别为C1和C2,pH分别为a和a+1,则C2=10C1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 物质 | Cu(OH)2 | Fe(OH)2 | Fe(OH)3 |
| 开始沉淀pH | 6.0 | 7.5 | 1.4 |
| 沉淀完全pH | 13 | 14 | 3.7 |

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | K+、Mn${O}_{4}^{-}$、Cl-、${SO}_{4}^{2-}$ | B. | Na+、${CO}_{3}^{2-}$、${SO}_{4}^{2-}$、Cl- | ||
| C. | ${NO}_{3}^{-}$、Na+、${HCO}_{3}^{-}$、Mg2+ | D. | Na+、${NO}_{3}^{-}$、H+、${SO}_{4}^{2-}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硅相对于氢气便于运输、贮存,从安全角度考虑,硅是有开发价值的燃料 | |
| B. | 硅在地壳中含量居第二位,在地球上有丰富的硅资源,如石英、水晶、玛瑙的主要成分都是单质硅 | |
| C. | 存放NaOH溶液的试剂瓶应用玻璃塞 | |
| D. | 二氧化硅是一种良好的半导体材料 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com