
 将一定质量的Mg和Al混合物投入到200mL稀硫酸中,固体全部溶解后,向所得溶液中滴加NaOH溶液至过量,生成沉淀的物质的量与加入NaOH溶液的体积关系如图所示.则下列说法不正确的是( )
将一定质量的Mg和Al混合物投入到200mL稀硫酸中,固体全部溶解后,向所得溶液中滴加NaOH溶液至过量,生成沉淀的物质的量与加入NaOH溶液的体积关系如图所示.则下列说法不正确的是( )| A、Mg和Al的总质量为9g |
| B、最初20mLNaOH溶液用于中和过量的稀硫酸 |
| C、NaOH溶液物质的量浓度为5mol?L-1 |
| D、生成的氢气在标准状况下的体积为11.2L |
| 1 |
| 2 |
| 0.2mol |
| 0.24L-0.20L |
| 1 |
| 2 |
| 0.2mol |
| 0.24L-0.20L |
| 0.2mol×3+0.15mol×2 |
| 2 |


 开心试卷期末冲刺100分系列答案
开心试卷期末冲刺100分系列答案 双基同步导航训练系列答案
双基同步导航训练系列答案 黄冈小状元同步计算天天练系列答案
黄冈小状元同步计算天天练系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、制取NaHCO3的反应是利用其溶解度小于NaCl |
| B、用澄清的石灰水可鉴别NaHCO3溶液和Na2CO3溶液 |
| C、在第③、④、⑤步骤中,溴元素均被氧化 |
| D、加热MgCl2溶液制取无水氯化镁 |
查看答案和解析>>
科目:高中化学 来源: 题型:
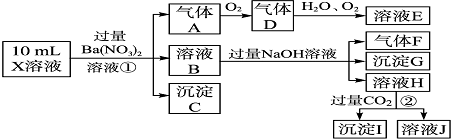
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、单质的熔点和沸点随核电荷数的增加逐渐升高 |
| B、单质的氧化性随核电荷数的增加逐渐减弱 |
| C、氢化物的稳定性随核电荷数的增加逐渐增强 |
| D、卤素阴离子的还原性随核电荷数的增加逐渐增强 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1:9 | B、1:1 |
| C、1:2 | D、1:4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、钠是电和热的良导体 |
| B、在水中的溶解性:NaHCO3大于Na2CO3 |
| C、明矾净水是由于明矾在水中形成Al(OH)3胶体具有吸附作用 |
| D、某溶液焰色反应时,火焰呈黄色就说明该溶液一定有钠元素,一定没有钾元素 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com