
【题目】重金属离子具有毒性.实验室中有甲、乙两种重金属离子的废液,甲废液经化验呈碱性,主要有毒离子为Ba2+ , 如将甲、乙两废液按一定比例混合,毒性明显降低.则乙废液中可能含有的离子是( )
A.Cu2+和SO ![]() ?
?
B.Cu2+和Cl﹣
C.K+和SO ![]()
D.Ag+和NO ![]()
【答案】A
【解析】解:甲废液经化验呈碱性,则溶液中含有OH﹣ , 主要为有毒离子为Ba2+ , 将甲、乙两废液按一定比例混合,毒性明显降低,则甲乙发生反应使重金属离子生成沉淀,
则乙中应含有SO ![]() ,发生反应Ba2++SO
,发生反应Ba2++SO ![]() =BaSO4↓,
=BaSO4↓,
乙中的重金属离子与甲中的OH﹣反应生成沉淀,根据选项中离子的性质可知,只有A符合,
发生反应为2OH﹣+Cu2+=Cu(OH)2↓,
故选A.
常见的重金属离子:Cu2+、Ag+、Hg2+、Ba2+、Pb2+ , 甲中有OH﹣、Ba2+ , 乙中有Cu2+、SO ![]() ,它们发生如下反应:2OH﹣+Cu2+=Cu(OH)2↓,Ba2++SO
,它们发生如下反应:2OH﹣+Cu2+=Cu(OH)2↓,Ba2++SO ![]() =BaSO4↓,将甲、乙两废液按一定比例混合,毒性明显降低,以此解答该题.
=BaSO4↓,将甲、乙两废液按一定比例混合,毒性明显降低,以此解答该题.


科目:高中化学 来源: 题型:
【题目】锰锂电池的体积小、性能优良,是常用的一次电池.该电池反应原理如图所示,其中电解质LiClO4溶于混合有机溶剂中,Li+通过电解质迁移入MnO2晶格中,生成LiMnO2 . 回答下列问题: 
(1)外电路的电流方向是由极流向极(填字母).
(2)电池正极反应式 .
(3)是否可用水代替电池中的混合有机溶剂?(填“是”或“否”),原因是 .
(4)MnO2可与KOH和KClO3在高温下反应,生成K2MnO4 , 反应的化学方程式为 . K2MnO4在酸性溶液中歧化,生成KMnO4和MnO2的物质的量之比为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】五种短周期元素的部分性质数据如下:
元素 | T | X | Y | Z | W |
原子半径(nm) | 0.037 | 0.075 | 0.099 | 0.102 | 0.143 |
最高或最低化合价 | +1 | +5﹣3 | +7﹣1 | +6﹣2 | +3 |
(1)Z离子的结构示意图为 .
(2)关于Y、Z两种元素,下列叙述正确的是(填序号). a.简单离子的半径 Y>Z
b.气态氢化物的稳定性Y比 Z强
c.最高价氧化物对应水化物的酸性Z比Y强
(3)甲是由T、X两种元素形成的10e﹣分子,乙是由Y、W两种元素形成的化合物.某同学设计了如图所示装置(夹持仪器省略)进行实验,将甲的浓溶液逐滴加入到NaOH固体中,烧瓶中即有甲放出,原因是 . 一段时间后,观察到试管中的现象是 , 发生反应的离子方程式是 . 
(4)T,X两种元素形成XT5固体,它的所有原子的最外层都符合相应稀有气体原子的最外层结构,则其电子式为 .
(5)XO2是导致光化学烟雾的“罪魁祸首”之一.它被氢氧化钠溶液吸收的化学方程式是:2XO2+2NaOH═M+NaXO3+H2O(已配平),产物M中元素X的化合价为 .
(6)常温下,Z2Y2是一种橙黄色液体,广泛用于橡胶工业的硫化机,其分子结构与双氧水分子相似.试写出其结构式
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值,下列说法正确的是( )
A.在20℃,1.01×105Pa时,22.4L甲烷(CH4)所含的原子数为5NA
B.常温常压下,28g氮气所含的原子数为2NA
C.标准状况下,22.4L水所含有的分子数目为NA
D.0.5mol H2O所含的电子数目为9 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A~H是中学化学中的常见物质,A、C、G是金属,E、F是氧化物,B溶于水得蓝色溶液,它们有如图所示的关系(反应中生成的水已略去).试回答下列问题. 
(1)推断填写物质化学式:A是 , D是 , H是
(2)反应④的化学方程式为 .
(3)用金属C制备另一种金属单质是工业上较常用的方法.如:2C+4BaO ![]() 3Ba↑+BaOC2O3
3Ba↑+BaOC2O3
①常温下C的金属性比Ba的金属性(选填“强”“弱”).
②利用上述方法可制取Ba的主要原因是 .
a、高温时C的活泼性大于Ba
b、高温有利于BaO分解
c、高温时BaOC2O3比C2O3稳定
d、金属Ba的沸点比金属C的低
(4)H水溶液与氢碘酸反应时可生成棕色物质,该反应的离子方程式为
(5)将51.2克的A投入200毫升的硝酸溶液中恰好反应完全,产生标准状况下的NO2、NO共31.36L,求硝酸的浓度molL﹣1 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2H、13C、15N、18O、34S等常用作环境分析指示物,下列对它们的说法正确的是( )
A. 34S原子核内的中子数为16B. 13C和15N原子核内的质子数相差2
C. 16O与18O互称同位素D. 2H的核外电子数比1H多一个
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯碱厂电解饱和食盐水制取NaOH溶液的工艺流程示意图如图1,完成下列填空: 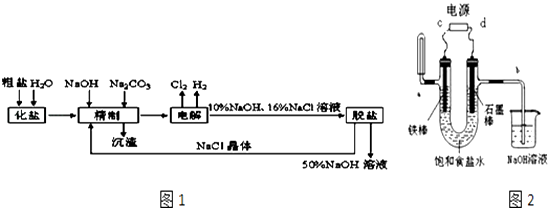
(1)在电解过程中,与电源负极相连的电极上电极反应为 , 与电源正极相连的电极附近,溶液pH(选填“不变”、“升高”或“下降”).
(2)工业食盐含Ca2+、Mg2+等杂质,精制过程发生反应的离子方程式为 , .
(3)如果粗盐中SO42﹣含量较高,必须添加钡试剂除去SO42﹣ , 该钡试剂可以是 .
A.BaCl2
B.Ba(NO3)2
C.BaCO3
(4)用以如图2装置电解饱和食盐水时a处收集到的气体是U型管左边铁棒附近滴入紫色石蕊颜色变化为 , C为电源的极.B处导气管中产生的气体可用检验.
(5)电解足够长时间后发现相同条件下a出和b处产生的气体体积比接近2:1,此时将电源正负极互换则U型管内现象是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在配制一定物质的量浓度的盐酸时,下列错误操作可使所配制溶液浓度偏高的是
A.用量筒量取浓盐酸时仰视读数
B.溶解搅拌时有液体飞溅
C.定容时仰视容量瓶瓶颈刻度线
D.摇匀后见液面下降,再加水至刻度线
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室可用K2Cr2O7固体与浓盐酸混合加热制备氯气.发生的离子反应如下: ____Cr2O ![]() +____Cl﹣+____H+=____Cl2↑+____Cr3++____□,下列有关叙述不正确的是( )
+____Cl﹣+____H+=____Cl2↑+____Cr3++____□,下列有关叙述不正确的是( )
A.以上各物质对应的计量数依次为1、6、14、3、2、7
B.Cr2O72﹣发生了还原反应
C.□处对应的物质是H2O
D.若0.1mol Cr2O ![]() 参加反应,产生氯气物质的量是0.5mol
参加反应,产生氯气物质的量是0.5mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com