
| A. | 改燃煤为燃气,可以减少废气中SO2等有害物质的排放量天气的一种措施 | |
| B. | 84 消毒液的有效成分是 NaClO | |
| C. | 含有食品添加剂的食物对人体健康不一定有益 | |
| D. | 金属防护中:牺牲阳极的阴极保护法利用的是电解原理,外加电流的阴极保护法利用的 是原电池原理 |
分析 A.改燃煤为燃气,可减少二氧化硫的排放量,可减少PM2.5的排放;
B.氯气与氢氧化钠反应可得84消毒液;
C.食品添加剂中某些物质有毒,对人体有害;
D.利用原电池原理的牺牲阳极的阴极保护法,外加电流的阴极保护法利用的是电解原理.
解答 解:A.改燃煤为燃气,可减少废气中SO2等有害物质的量,减少环境污染物的排放,可有效减少雾霾发生,故A正确;
B.氯气与氢氧化钠反应可得84消毒液,有效成分为NaClO,故B正确;
C.食品添加剂中某些物质有毒,对人体有害,所以含有食品添加剂的食物对人体健康不一定有益,故C正确;
D.原电池的正极及电解池的阴极中的金属被保护,所以利用电化学原理保护金属主要有两种方法,分别是牺牲阳极的阴极保护法和外加电流的阴极保护法,故D错误;
故选:D.
点评 本题考查环境污染及保护以及生活中的材料等知识,熟悉相关物质的性质是解题关键,注意金属腐蚀的原理及防护措施,题目难度不大.


 小学教材全测系列答案
小学教材全测系列答案 小学数学口算题卡脱口而出系列答案
小学数学口算题卡脱口而出系列答案 优秀生应用题卡口算天天练系列答案
优秀生应用题卡口算天天练系列答案 浙江之星课时优化作业系列答案
浙江之星课时优化作业系列答案科目:高中化学 来源: 题型:解答题
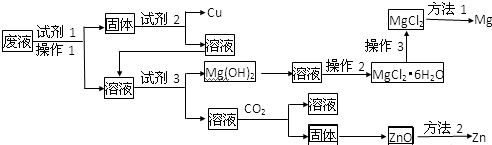
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3.2g氧气所含氧分子数为0.2NA | |
| B. | 1L0.1mol/L NaCl 溶液中所含的Na+为0.1NA | |
| C. | 0.012 kg 12C中含有碳原子数约为NA | |
| D. | 24g镁变成镁离子时失去的电子数为2N A |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ③④⑤ | B. | ②③④ | C. | ①③④⑥ | D. | ①②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

| 编号 | 实验目的 | 碳粉/g | 铁粉/g | 醋酸/% |
| ① | 为以下实验作参照 | 0.5 | 2.5 | 90.0 |
| ② | ? | 0.5 | 2.5 | 36.0 |
| ③ | 碳粉质量的影响 | 0.2 | ? | 90.0 |
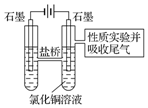
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | v正(H2)=2v逆(CO) | |
| B. | 平衡常数K不再随时间而变化 | |
| C. | 混合气体的密度保持不变 | |
| D. | 混合气体的平均相对分子质量不随时间而变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 物质类别 | 酸 | 碱 | 盐 | 氧化物 | 氢化物 |
| 化学式 | ①H2SO4 ②HNO3 | ③NaOH ④KOH | ⑤Na2SO4 ⑥K2SO4 | ⑦SO2 ⑧SO3 | ⑨NH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com