
”¾ĢāÄæ”湤ŅµÉĻÖʱøBaCl2µÄ¹¤ŅÕĮ÷³ĢĶ¼ČēĻĀ£ŗ 
Ä³ŃŠ¾æŠ”×éŌŚŹµŃéŹŅÓĆÖŲ¾§ŹÆ£ØÖ÷ŅŖ³É·ÖBaSO4£©¶Ō¹¤Ņµ¹ż³Ģ½ųŠŠÄ£ÄāŹµŃ飮²é±ķµĆ
BaSO4£Øs£©+4C£Øs£© ![]() 4CO£Øg£©+BaS£Øs£©”÷H1=+571.2kJmol©1¢Ł
4CO£Øg£©+BaS£Øs£©”÷H1=+571.2kJmol©1¢Ł
BaSO4£Øs£©+2C£Øs£© ![]() 2CO2£Øg£©+BaS£Øs£©”÷H2=+226.2kJmol©1¢Ś
2CO2£Øg£©+BaS£Øs£©”÷H2=+226.2kJmol©1¢Ś
£Ø1£©ĘųĢåÓĆ¹żĮæNaOHČÜŅŗĪüŹÕ£¬µĆµ½Įņ»ÆÄĘ£®Na2SĖ®½āµÄĄė×Ó·½³ĢŹ½ĪŖ £®
£Ø2£©ĻņBaCl2ČÜŅŗÖŠ¼ÓČėAgNO3ŗĶKBr£¬µ±Į½ÖÖ³Įµķ¹²“ꏱ£¬ ![]() = £® [Ksp£ØAgBr£©=5.4”Į10©13 £¬ Ksp£ØAgCl£©=2.0”Į10©10]
= £® [Ksp£ØAgBr£©=5.4”Į10©13 £¬ Ksp£ØAgCl£©=2.0”Į10©10]
£Ø3£©·“Ó¦C£Øs£©+CO2£Øg£© ![]() 2CO£Øg£©µÄ”÷H2=kJmol©1 £®
2CO£Øg£©µÄ”÷H2=kJmol©1 £®
£Ø4£©Źµ¼ŹÉś²śÖŠ±ŲŠė¼ÓČė¹żĮæµÄĢ棬Ķ¬Ź±»¹ŅŖĶØČėæÕĘų£¬ĘäÄæµÄŹĒ £®
”¾“š°ø”æ
£Ø1£©S2©+H2O?HS©+OH©”¢HS©+H2O?H2S+OH©
£Ø2£©2.7”Į10©3
£Ø3£©+172.5
£Ø4£©Ź¹BaSO4µĆµ½³ä·ÖµÄ»¹Ō£Ø»ņĢįøßBaSµÄ²śĮ棩,¢Ł¢ŚĪŖĪüČČ·“Ó¦,ĢæŗĶŃõĘų·“Ó¦·ÅČČĪ¬³Ö·“Ó¦ĖłŠčøßĪĀ
”¾½āĪö”æ½ā£ŗ£Ø1£©Na2SĖ®½ā³Ź¼īŠŌ£¬ĒŅÓŠĮ½²½Ė®½ā£¬ŅŌµŚŅ»²½Ė®½āĪŖÖ÷£¬µŚŅ»²½Ė®½āÉś³ÉĄė×ÓHS©£¬µŚ¶ž²½Ė®½āÉś³ÉH2S£¬Ė®½āµÄĄė×Ó·½³ĢŹ½·Ö±šĪŖS2©+H2OHS©+OH©”¢HS©+H2OH2S+OH©£¬
ĖłŅŌ“š°øŹĒ£ŗS2©+H2OHS©+OH©”¢HS©+H2OH2S+OH©£»£Ø2£©µ±Į½ÖÖ³Įµķ¹²“ꏱ£¬Ag+Ąė×ÓÅضČĻąĶ¬£¬øł¾ŻČܶȻż³£Źż¼ĘĖć£¬c£ØBr©£©= ![]() £¬c£ØCl©£©=
£¬c£ØCl©£©= ![]() £¬Ōņ
£¬Ōņ ![]() =
= ![]() =2.7”Į10©3£®
=2.7”Į10©3£®
ĖłŅŌ“š°øŹĒ£ŗ2.7”Į10©3£»£Ø3£©ĄūÓĆøĒĖ¹¶ØĀÉĒó½ā£ŗ
BaSO4£Øs£©+4C£Øs£© ![]() 4CO£Øg£©+BaS£Øs£©”÷H1=571.2kJmol©1¢Ł
4CO£Øg£©+BaS£Øs£©”÷H1=571.2kJmol©1¢Ł
BaSO4£Øs£©+2C£Øs£© ![]() 2CO2£Øg£©+BaS£Øs£©”÷H2=226.2kJmol©1¢Ś
2CO2£Øg£©+BaS£Øs£©”÷H2=226.2kJmol©1¢Ś
½«ŅŌÉĻĮ½øöČČ»Æѧ·½³ĢŹ½Ļą¼õ£¬Č»ŗó³żŅŌ2æÉµĆ£ŗ
C£Øs£©+CO2£Øg£© ![]() 2CO£Øg£©”÷H=
2CO£Øg£©”÷H= ![]() =+172.5kJmol©1£¬
=+172.5kJmol©1£¬
ĖłŅŌ“š°øŹĒ£ŗ+172.5£»£Ø4£©¼ÓČė¹żĮæCæÉĢįøßÖŲ¾§ŹÆµÄ×Ŗ»ÆĀŹ£¬ŅŌÉĻ·“Ó¦ĪŖĪüČČ·“Ó¦£¬ĢæŗĶŃõĘų·“Ó¦·ÅČČĪ¬³Ö·“Ó¦ĖłŠčøßĪĀ£¬
ĖłŅŌ“š°øŹĒ£ŗŹ¹BaSO4µĆµ½³ä·ÖµÄ»¹Ō£Ø»ņĢįøßBaSµÄ²śĮ棩£¬¢Ł¢ŚĪŖĪüČČ·“Ó¦£¬ĢæŗĶŃõĘų·“Ó¦·ÅČČĪ¬³Ö·“Ó¦ĖłŠčøßĪĀ£®


 ¾«Ó¢æŚĖćæØĻµĮŠ“š°ø
¾«Ó¢æŚĖćæØĻµĮŠ“š°ø Ó¦ÓĆĢāµć²¦ĻµĮŠ“š°ø
Ó¦ÓĆĢāµć²¦ĻµĮŠ“š°ø דŌŖ¼°µŚĻµĮŠ“š°ø
דŌŖ¼°µŚĻµĮŠ“š°ø Ķ¬²½°ĀŹżĻµĮŠ“š°ø
Ķ¬²½°ĀŹżĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŌŚ15mL0£®1molL©1KOHČÜŅŗÖŠÖšµĪ¼ÓČė0.2molL©1¼×ĖįČÜŅŗ£¬ČÜŅŗpHŗĶ¼ÓČė¼×Ėį£ØČõĖį£©µÄĢå»ż¹ŲĻµĒśĻßČēĶ¼ĖłŹ¾£¬ĻĀĮŠ¹ŲĻµÕżČ·µÄŹĒ£Ø””””£© 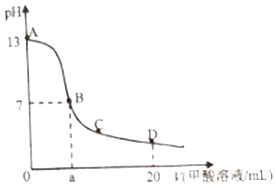
A.ŌŚBµć£ŗc£ØK+£©=c£ØHCOO©£©£¾c£ØOH©£©=c£ØH+£©£¬ĒŅa=7.5
B.ŌŚA£¬B¼äČĪŅāŅ»µć£¬c£ØHCOO©£©£¾c£ØK+£©£¾c£ØOH©£©£¾c£ØH+£©
C.ŌŚDµć£ŗc£ØHCOO©£©+c£ØHCOOH£©£¾2c£ØK+£©
D.B”śC¶Ī£ŗĖ®µÄµēĄė³Ģ¶ČĻČŌö“óŗó¼õŠ”
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀ±ķĪŖŌŖĖŲÖÜĘŚ±ķµÄŅ»²æ·Ö£¬Ēė²ĪÕÕŌŖĖŲ¢Ł”«¢ąŌŚ±ķÖŠµÄĪ»ÖĆ£¬»Ų“šĻĀĮŠĪŹĢā£ŗ

£Ø1£©Š“³ö¢ŽŌŖĖŲµÄĆū³Ę£ŗ______________”£
£Ø2£©ŌŚŅŌÉĻŌŖĖŲµÄŌ×ÓÖŠ£¬Ō×Ó°ė¾¶×ī“óµÄŹĒ___________________£ØĢīŌŖĖŲ·ūŗÅ£©”£
£Ø3£©µŲæĒÖŠŗ¬Įæ¾ÓÓŚµŚ¶žĪ»µÄŌŖĖŲĪ»ÓŚŌŖĖŲÖÜĘŚ±ķÖŠµÄµŚ___________ÖÜĘŚ£¬µŚ_________×唣
£Ø4£©¢ßŌŖĖŲµÄĘųĢ¬Ēā»ÆĪļ»ÆѧŹ½ĪŖ___________________”£
£Ø5£©¢ŻŌŖĖŲµÄ×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦µÄĖ®»ÆĪļ»ÆѧŹ½ĪŖ______________________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ0.2molijĢžAŌŚŃõĘųÖŠĶźČ«Č¼ÉÕŗó£¬Éś³ÉCO2ŗĶH2Oø÷1.2mol”£
(1)ĢžAµÄ·Ö×ÓŹ½ĪŖ_____£®
(2)ČōĢžA²»ÄÜŹ¹äåĖ®ĶŹÉ«£¬µ«ŌŚŅ»¶ØĢõ¼žĻĀÄÜÓėĀČĘų·¢ÉśČ”“ś·“Ó¦£¬ĘäŅ»ĀČČ”“śĪļÖ»ÓŠŅ»ÖÖ£¬ŌņĢžAµÄ½į¹¹¼ņŹ½ĪŖ_____£®
(3)ČōĢžAÄÜŹ¹äåĖ®ĶŹÉ«£¬ŌŚ“߻ƼĮ×÷ÓĆĻĀ£¬ÓėH2·¢Éś¼Ó³É·“Ó¦£¬Ęä¼Ó³É²śĪļB¾²ā¶Ø·Ö×ÓÖŠŗ¬ÓŠ4øö¼×»ł£¬ĒŅĘäŗĖ“Ź²ÕńĒāĘ×Ķ¼ÖŠÓŠĮ½×é·å£¬ŌņAæÉÄÜÓŠµÄ½į¹¹¼ņŹ½ĪŖ_____£®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠø÷×éĄė×ÓŌŚÖø¶ØµÄČÜŅŗÖŠÄÜ“óĮæ¹²“ęµÄŹĒ £Ø £©
¢ŁĪŽÉ«ČÜŅŗÖŠ£ŗK+”¢Cu2+”¢Na+”¢SO42-
¢ŚpH=11µÄČÜŅŗÖŠ£ŗK+”¢Ba2+”¢Cl-”¢HCO3-
¢ŪÄÜŹ¹·ÓĢŖŹŌ¼Į±äŗģµÄČÜŅŗÖŠ£ŗCl-”¢CO32-”¢NO3-”¢NH4+
A.¢ŁB.¢Ś
C.¢ŪD.Č«¶¼²»ŠŠ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æNAĪŖ°¢·ü¼ÓµĀĀŽ³£ŹżµÄÖµ£¬ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ
A. ±ź×¼×“æöĻĀ3.6 g H2Oŗ¬ÓŠµÄµē×ÓŹżĪŖ2NA
B. 2.8 gŅŅĻ©Óė¾ŪŅŅĻ©µÄ»ģŗĻĪļŗ¬ÓŠµÄ¼«ŠŌ¼üĪŖ0.4NA
C. 0.l moI Cl2Óė×ćĮæµÄĢś·Ū³ä·Ö·“Ó¦×ŖŅʵĵē×ÓŹżĪŖ0.2NA
D. 1 L 0.2 mol/lµÄK2Cr2O7ČÜŅŗÖŠ![]() µÄŹżÄæĪŖ0.2NA
µÄŹżÄæĪŖ0.2NA
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æµ±Ē°ŌŚČĖĄąŅŃÖŖµÄ»ÆŗĻĪļÖŠ£¬ÖÖĄą×ī¶ąµÄŹĒ£Ø £©
A. ¢ńA×åŌŖĖŲµÄ»ÆŗĻĪļ B. ¢ōA×åŌŖĖŲµÄ»ÆŗĻĪļ
C. ¢öA×åŌŖĖŲµÄ»ÆŗĻĪļ D. ¢öB×åŌŖĖŲµÄ»ÆŗĻĪļ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æijĪĀ¶ČĻĀ£¬ŌŚŅ»øö2LµÄĆܱÕČŻĘ÷ÖŠ¼ÓČė4mol AŗĶ2mol B½ųŠŠČēĻĀ·“Ó¦£ŗ3A£Øg£©+2B£Øg£©4C£Øs£©+D£Øg£©£¬·“Ó¦2minŗó“ļµ½Ę½ŗā£¬²āµĆÉś³É1.6mol C£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø””””£©
A.Ē°2 min DµÄĘ½¾ł·“Ó¦ĖŁĀŹĪŖ0.2 molL©1min©1
B.“ĖŹ±£¬BµÄĘ½ŗā×Ŗ»ÆĀŹŹĒ40%
C.Ōö“óøĆĢåĻµµÄŃ¹Ēæ£¬Ę½ŗā²»ŅʶÆ
D.Ōö¼ÓB£¬Ę½ŗāĻņÓŅŅĘ¶Æ£¬BµÄĘ½ŗā×Ŗ»ÆĀŹŌö“ó
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æNAĪŖ°¢·ü¼ÓµĀĀŽ³£Źż£¬ĻĀĮŠŠšŹöÖŠÕżČ·µÄŹĒ
A. ±ź×¼×“æöĻĀ,11.2 L CH3CH2OH ÖŠŗ¬ÓŠµÄ·Ö×ÓŹżÄæĪŖ0.5NA
B. ³£ĪĀ³£Ń¹ĻĀ,92 gµÄNO2ŗĶN2O4»ģŗĻĘųĢåŗ¬ÓŠµÄŌ×ÓŹżĪŖ6NA
C. ±ź×¼×“æöĻĀ,6. 72 L NO2ÓėĖ®³ä·Ö·“Ó¦×ŖŅʵĵē×ÓŹżÄæĪŖ0.1NA
D. 100g 46%µÄŅŅ“¼ČÜŅŗÖŠ£¬ŗ¬H£O¼üµÄŹżÄæĪŖNA
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com