
| A£® | S£Øs£©+O2£Øg£©ØTSO2£Øg£©£¬·“Ó¦·Å³öµÄČČĮæ“óÓŚ293.23 kJ•mol-1 | |
| B£® | S£Øg£©+O2£Øg£©ØTSO2£Øg£©£¬·“Ó¦·Å³öµÄČČĮæŠ”ÓŚ293.23 kJ•mol-1 | |
| C£® | 1 mol SO2µÄ¼üÄÜ×ÜŗĶ“óÓŚ1 molĮņŗĶ1 molŃõĘųµÄ¼üÄÜÖ®ŗĶ | |
| D£® | 1 mol SO2µÄ¼üÄÜ×ÜŗĶŠ”ÓŚ1 molĮņŗĶ1 molŃõĘųµÄ¼üÄÜÖ®ŗĶ |
·ÖĪö øł¾ŻĪļÖŹÓÉŅŗĢ¬×Ŗ±ä³É¹ĢĢ¬ŅŖ·Å³öČČĮ棬ÓÉŅŗĢ¬×Ŗ±ä³ÉĘųĢ¬ŅŖĪüŹÕČČĮæŅŌ¼°·ÅČČ·“Ó¦ÖŠ¾É¼ü¶ĻĮŃĪüŹÕµÄÄÜĮæŠ”ÓŚŠĀ¼üŠĪ³ÉĖł·Å³öµÄÄÜĮæĄ“·Ö·ÖĪö£®
½ā“š ½ā£ŗA”¢ŅņĪļÖŹÓÉŅŗĢ¬×Ŗ±ä³É¹ĢĢ¬ŅŖ·Å³öČČĮ棬ĖłŅŌ1mol¹ĢĢåSµ„ÖŹČ¼ÉշųöµÄČČĮæŠ”ÓŚ297.23kJ•mol-1£¬¹ŹA“ķĪó£»
B”¢ŅņĪļÖŹÓÉŅŗĢ¬×Ŗ±ä³ÉĘųĢ¬ŅŖĪüŹÕČČĮ棬ĖłŅŌ1molĘųĢåSµ„ÖŹČ¼ÉշųöµÄČČĮæ“óÓŚ297.23kJ•mol-1£¬¹ŹB“ķĪó£»
C”¢Ņņ·ÅČČ·“Ó¦ÖŠ¾É¼ü¶ĻĮŃĪüŹÕµÄÄÜĮæŠ”ÓŚŠĀ¼üŠĪ³ÉĖł·Å³öµÄÄÜĮ棬1molSO2µÄ¼üÄÜ×ÜŗĶ“óÓŚ1molSŗĶ1molO2µÄ¼üÄÜ×ÜŗĶ£¬¹ŹCÕżČ·£»
D”¢Ņņ·ÅČČ·“Ó¦ÖŠ¾É¼ü¶ĻĮŃĪüŹÕµÄÄÜĮæŠ”ÓŚŠĀ¼üŠĪ³ÉĖł·Å³öµÄÄÜĮ棬1molSO2µÄ¼üÄÜ×ÜŗĶ“óÓŚ1molSŗĶ1molO2µÄ¼üÄÜ×ÜŗĶ£¬¹ŹD“ķĪó£»
¹ŹŃ”C£®
µćĘĄ ±¾ĢāÖ÷ŅŖæ¼²éĮĖ»Æѧ·“Ó¦ÖŠ·“Ó¦ČČµÄ¼ĘĖć£¬ŠčŅŖ×¢ŅāµÄŹĒĪļÖŹČżĢ¬Ö®¼äµÄ×Ŗ±äŅ²“ęŌŚÄÜĮæµÄ±ä»Æ£®


 Ö„ĀéæŖ»ØæĪ³ĢŠĀĢåŃéĻµĮŠ“š°ø
Ö„ĀéæŖ»ØæĪ³ĢŠĀĢåŃéĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 £®
£® £¬A”śBµÄ·“Ó¦ĄąŠĶĪŖŃõ»Æ·“Ó¦£®
£¬A”śBµÄ·“Ó¦ĄąŠĶĪŖŃõ»Æ·“Ó¦£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĻąĶ¬Ģõ¼žĻĀ£¬2mol H2ĶźČ«Č¼ÉÕŹ±ŅŗĢ¬Ė®·ÅČČ572kJ | |
| B£® | ĻąĶ¬Ģõ¼žĻĀ£¬2mol H2OĶźČ«·Ö½āĪüŹÕČČĮæ572kJ | |
| C£® | ĻąĶ¬Ģõ¼žĻĀ£¬1mol H2³ä·ÖČ¼ÉÕÉś³ÉĘųĢ¬Ė®·ÅČČ“óÓŚ286kJ | |
| D£® | ŠĪ³É1mol H2OµÄ»Æѧ¼üĖłŹĶ·ÅµÄÄÜĮæ“óÓŚ¶ĻĮŃlmol H2ŗĶ0.5mol O2µÄ»Æѧ¼üĖłĪüŹÕµÄ×ÜÄÜĮæ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
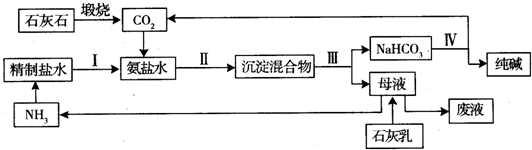
| A£® | ĒāŃõ»ÆÄĘČÜŅŗÖŠĶØČė¹żĮ涞Ńõ»ÆĢ¼£ŗOH-+CO2ØTHCO3- | |
| B£® | Ģ¼ĖįøĘČÜÓŚĻ”“×Ėį£ŗCaCO3+2H+ØTCa2++H2O+CO2”ü | |
| C£® | ĻņĢ¼ĖįĒāļ§Ļ”ČÜŅŗÖŠ¼ÓČė¹żĮæÉÕ¼īČÜŅŗ£ŗNH4++OH-ØTNH3H2O | |
| D£® | ÄĘÓėĖ®µÄ·“Ó¦£ŗNa+H2OØTNa++OH-+H2”ü |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com