
【题目】250C时纯水的电离度为a1,pH=2的醋酸溶液中水的电离度为a2,pH=12的氢氧化钠溶液中水的电离度为a3。若将上述醋酸与氢氧化钠溶液等体积混合,所得溶液中水的电离度为a4.下列关系式中正确的是( )
A. a2=a3<a4<a1 B. a3=a2<a1<a4 C. a2<a3<a1<a4 D. a1<a2<a3<a4
【答案】A
【解析】试题分析:在25 ℃时,纯水中![]() mol·L-1,纯水的电离度为α1;pH=2的醋酸溶液中c(H+)=10-2mol·L-1,水电离出来的氢离子的浓度与氢氧根的浓度相等,即
mol·L-1,纯水的电离度为α1;pH=2的醋酸溶液中c(H+)=10-2mol·L-1,水电离出来的氢离子的浓度与氢氧根的浓度相等,即![]() ,水的电离度为α2,醋酸电离出来的氢离子要抑制水的电离,α2<α1;同理可得pH=12的氢氧化钠溶液中c(OH-)=10-2mol·L-1,
,水的电离度为α2,醋酸电离出来的氢离子要抑制水的电离,α2<α1;同理可得pH=12的氢氧化钠溶液中c(OH-)=10-2mol·L-1,![]() ,水的电离度为α3=α2<α1;pH=2的醋酸溶液和pH=12的氢氧化钠溶液等体积混合,醋酸是弱电解质,所以有醋酸过量,溶液仍显酸性,溶液的pH<2,对水的电离抑制作用小于pH=2的醋酸溶液,
,水的电离度为α3=α2<α1;pH=2的醋酸溶液和pH=12的氢氧化钠溶液等体积混合,醋酸是弱电解质,所以有醋酸过量,溶液仍显酸性,溶液的pH<2,对水的电离抑制作用小于pH=2的醋酸溶液,![]() ,溶液中水的电离度为α4,所以有a2=a3<a4<a1;答案选A。
,溶液中水的电离度为α4,所以有a2=a3<a4<a1;答案选A。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】水是最宝贵的资源之一。下列表述正确的是( )
A.向水中加入盐,对水的电离没有影响
B.在盐酸稀释过程中水的电离程度没有发生变化
C.水的电离程度很小,纯水中主要存在形态是水分子
D.向水中加入酸或碱,都可抑制水的电离,使水的离子积减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“即食即热型快餐”适合外出旅行时使用.其内层是用铝箔包裹的并已加工好的真空包装食品,外层则是分别包装的两包化学物质,使用时拉动预留在外的拉线,使这两种化学物质反应,此时便可对食物进行加热,这两包化学物质最合适的选择是( ) 
A.氢氧化钡晶体和氯化铵晶体
B.生石灰与水
C.金属钠与水
D.氯化钠与水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中进行反应CH4(g)+H2O(g)![]() CO(g)+3H2(g)△H>0,测得c(CH4)随反应时间(t)的变化如图所示.下列判断正确的是( )
CO(g)+3H2(g)△H>0,测得c(CH4)随反应时间(t)的变化如图所示.下列判断正确的是( )
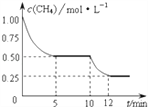
A. 恒温下,缩小容器体积,平衡后c(H2)减小
B. 0~5min内,v(H2)=0.1mol/(Lmin)
C. 10min时,改变的外界条件可能是升高温度
D. 12min时,反应达平衡的本质原因是气体总质量不再变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关金属元素特征的叙述正确的是( )
A.金属元素的原子只有还原性,离子只有氧化性
B.金属元素在一般化合物中只显正价
C.金属元素在不同的化合物中的化合价均不同
D.金属元素的单质在常温下均为金属晶体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】作为目前发现的最薄、强度最大、导电导热性能最强的一种新型纳米材料,石墨烯被称为“黑金”,是“新材料之王”,科学家甚至预言石墨烯将“彻底改变21世纪”。极有可能掀起一场席卷全球的颠覆性新技术新产业革命。石墨烯一层层叠起来就是石墨,厚1毫米的石墨大约包含300万层石墨烯。英国曼彻斯特大学的两位科学家安德烈·盖姆(AnD.re Geim)和克斯特亚·诺沃消洛夫(Konstantin Novoselov)从高定向热解石墨中剥离出石墨片,然后将薄片的两面粘在一种特殊的胶带上,撕开胶带,就能把石墨片一分为二。不断地这样操作,于是薄片越来越薄,最后,他们得到了仅由一层碳原子构成的薄片,这就是石墨烯(如图)。
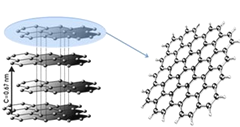
石墨 石墨稀
(1))石墨、金刚石、C60等互称为___________________;
(2)已知25℃,101KPa下,石墨、金刚石燃烧的热化学方程式分别为
C(石墨) + O2(g) = CO2(g);△H=-393.51kJ.mol-1
C(金刚石) + O2(g) = CO2(g);△H=-395.41kJ.mol-1
C(金刚石)=C(石墨);△H =________kJ/mol
(3)石墨和金刚石相比,更稳定的是:________________;
(4)请用化学知识解释科学家为什么可以用特殊的胶带将石墨不断地粘撕得到石墨烯: _______________。
(5)12g石墨烯中含有___________NA个如图所示的六元环。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表为元素周期表的一部分,表中列出了10种元素在周期表中的位置,按要求完成下列各小题.
主族 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
2 | ⑥ | ⑦ | ⑨ | ||||||
3 | ① | ③ | ⑤ | ⑧ | ⑩ | ||||
4 | ② | ④ |
(1)化学性质最不活泼的元素的原子结构示意图为 .
(2)元素⑧的名称为 , 其最高价氧化物的水化物的化学式为 .
(3)元素③与元素⑧形成的化合物的电子式为 .
(4)非金属性最强的元素是(填元素符号);除0族外原子半径最大的元素是(填元素符号);元素①单质与水反应的离子方程式是 .
(5)①、③、⑤三种元素的最高价氧化物为水化物中,碱性最强的化合物的化学式是 .
(6)能形成两性氢氧化物的元素是(用元素符号表示),写出该元素的单质与①的最高价氧化物的水化物反应的化学方程式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)990C时,Kw=1.0×10-12mol2·L-2,该温度下测得0.1 mol·L-1 Na2A溶液的pH=6。
①H2A在水溶液中的电离方程式为______________________.
②该温度下,将0.01 mol· L-1 H2A溶液稀释到20倍后,溶液的pH=________。
③体积相等、pH均为1的盐酸与H2A溶液分别与足量的Zn反应,产生的氢气______(填字母)
A.盐酸多 B.H2A多 C.一样多 D.无法确定
(2)最新研究发现,用隔膜电解法处理高浓度乙醛废水的工艺具有流程简单、能耗较低等优点,其原理是使乙醛分别在阴、阳极发生反应生成乙醇和乙酸,总反应式为2CH3CHO+H2O![]() CH3CH2OH +CH3COOH实验室中,以一定浓度的乙醛—Na2SO4溶液为电解质溶液,模拟乙醛废水的处理过程,其装置如图所示。
CH3CH2OH +CH3COOH实验室中,以一定浓度的乙醛—Na2SO4溶液为电解质溶液,模拟乙醛废水的处理过程,其装置如图所示。
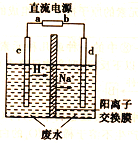
①若以甲烷碱性燃料电池为直流电源,则燃料电池中b极应通入_______(填化学式),电极反应式为_______。
②在实际工艺处理中,阴极区乙醛的去除率可达80%。若在两极区分别注入1m3乙醛含量为3000mg·L-1的废水,可得到乙醇_____kg(计算结果保留小数点后1位)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于氯气的叙述中,正确的是( )
A.氯气以液态形式存在时可称为氯水或液氯
B.红热的铜丝在氯气中燃烧,冒蓝色烟
C.有氯气参加的化学反应必须在溶液中进行
D.钠在氯气中燃烧生成白色固体氯化钠
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com