
 +2C2H5OH
+2C2H5OH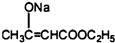 +CH3COOH→
+CH3COOH→ +CH3COONa
+CH3COONa
分析 ①催化剂参加反应,但反应前后质量和化学性质不变,根据反应原理,无水乙醇参与反应,但反应前后都有,为催化剂;
②空气中含有水蒸气,因此装置中加干燥管是为了防湿气进入反应体系中以保证反应体系干燥;
反应装置中冷凝管的作用是冷凝回流,挺高原料的利用率,减压装置中冷凝管的作用是冷却蒸发出的蒸汽便于得到产品;
为充分冷凝,使冷水充满冷凝器,因此冷却水采取逆流原理;
③由于产物中含有钠盐,因此产物处理后,滴加稀醋酸的目的是中和生成的钠盐,使之变成产物;分离互不相溶液体操作为分液;
酯类在碳酸钠溶液中的溶解度小,滴加碳酸钠溶液可以除去混有的乙酸;碳酸钾吸水,因此加碳酸钾的目的是干燥产品;
④3-丁酮酸乙酯沸点高,而受热温度超过95℃摄氏度时就会分解,所以需要减压蒸馏;
⑤根据反应物的用量可知钠不足,因此理论上生成产品的物质的量是0.07mol,根据m=nM计算理论上3-丁酮酸乙酯质量,进而计算其产率.
解答 解:①在反应原理中可以得到乙醇钠发生了反应生成了乙醇,在反应装置中加入的是乙醇,乙醇可以与金属钠反应生成乙醇钠,当乙醇钠反应后又生成了乙醇,故乙醇的作用是催化剂,
故答案为:催化剂;
②空气中含有水蒸气,因此装置中加干燥管是为了防止空气中的水蒸汽进入反应体系中以保证反应体系干燥;反应装置中冷凝管的作用是冷凝回流,提高原料的利用率,减压装置中冷凝管的作用是冷却蒸发出的蒸汽便于得到产品,为充分冷凝,故两个冷凝管的作用不同;左侧装置中冷凝水从b口进入,右侧冷凝管中的冷凝水应从d口进入,
故答案为:防湿气进入反应体系中以保证反应体系干燥;不相同;b、d;
③在第一步骤中生成的是产物的钠盐,加入稀醋酸使其变成产物;因产物易溶于水,当在其中加入的酸过多后会增加产物在水中的溶解度,醋酸不能滴加的过多;用分液漏斗分离出酯层的操作叫分液;碳酸钠溶液可以与加入的过量的醋酸反应,故洗涤的目的是中和醋酸;碳酸钾可以做干燥剂,对产物进行干燥,
故答案为:中和生成的钠盐,使之变成产物;酸多了会增加产物在水中的溶解度;分液;中和醋酸;干燥;
④因3-丁酮酸乙酯沸点181℃,在温度超过95℃摄氏度时就会分解,所以在进行蒸馏时的温度不能过高,需要减压蒸馏,
故答案为:3-丁酮酸乙酯沸点高,在沸点温度下还易分解;
⑤反应物中有0.32mol乙酸乙酯、0.07mol金属钠,乙酸乙酯过量,钠不足,因此理论上生成产品的物质的量是0.07mol,质量为0.07mol×130g/mol=9.1g,产率=$\frac{2.0g}{9.1g}$×100%=22%,
故选B.
点评 本题考查了物质制备方案的设计、对装置与操作的分析评价、物质的分离提纯、产率的计算,试题充分考查了学生的分析能力、理解能力及化学实验能力,题目难度中等.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 任何晶体中,若含有阳离子也一定含有阴离子 | |
| B. | 在电子云示意图中,小黑点密集表示电子在核外空间单位体积内电子出现的机会多 | |
| C. | 强电解质溶液一定比弱电解质溶液的导电能力强 | |
| D. | 常用原子光谱进行有机物相对分子质量的测定 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 物质 | CaCO3 | MgCO3 | Ca(OH)2 | Mg(OH)2 | Fe(OH)3 |
| Ksp | 4.96×10-9 | 6.82×10-6 | 4.68×10-6 | 5.61×10-12 | 2.64×10-39 |
| A. | 常温下,除去NaCl溶液中的MgCl2杂质,选用NaOH溶液比Na2CO3溶液效果好 | |
| B. | 常温下,除去NaCl溶液中的CaCl2杂质,选用Na2CO3溶液比NaOH溶液效果好 | |
| C. | 向含有Mg2+,Fe3+的溶液中滴加NaOH溶液,当两种沉淀共存且溶液的pH=8时,c(Mg2+):c(Fe3+)=2.125×1021 | |
| D. | 无法利用Ca(OH)2制备NaOH |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 高温结构陶瓷是新型无机非金属材料 | |
| B. | 钢是用量最大、用途最广的合金,分为碳素钢和合金钢 | |
| C. | 硅芯片是各种计算机、微电子产品的核心材料 | |
| D. | 单晶硅常用于制造光导纤维 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 滴定次数 | 待测溶液体积(mL) | 标准酸体积 | |
| 滴定前的刻度(mL) | 滴定后的刻度(mL) | ||
| 第一次 | 10.00 | 0.40 | 20.50 |
| 第二次 | 10.00 | 0.20 | 20.80 |
| 第三次 | 10.00 | 4.10 | 24.00 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
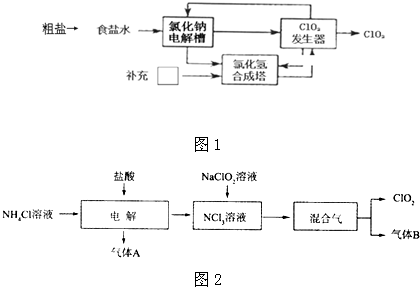
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
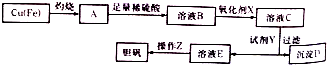
| 溶液中被沉淀离子 | Fe3+ | Fe2+ | Cu2+ |
| 完全生成氢氧化物沉淀时,溶液的pH | ≥3.7 | ≥6.4 | ≥4.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  铁钉易被腐蚀 | |
| B. |  滴加少量KSCN溶液,溶液变为血红色 | |
| C. |  燃气灶的中心部位容易生锈,主要是由于高温下铁发生化学腐蚀 | |
| D. | 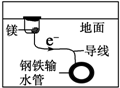 用牺牲镁块的方法来防止地下钢铁管道的腐蚀,镁块相当于原电池的正极 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验目的 | 主要玻璃仪器 | 试剂 |
| A | 鉴别Na2CO3和NaHCO3溶液 | 试管、胶头滴管 | 澄清石灰水 |
| B | 分离I2和CCl4的混合物 | 分液漏斗、烧杯 | 乙醇 |
| C | 实验室制取干燥的NH3 | 试管、酒精灯、带导管的橡皮塞 | NH4Cl、Ca(OH)2、碱石灰 |
| D | 测定NaOH溶液的浓度 | 滴定管、锥形瓶、烧杯 | NaOH溶液、酚酞试剂、0.1000mol•L-1盐酸 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com