
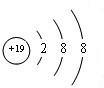
 ,C原子的结构示意图为
,C原子的结构示意图为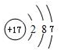 .
.分析 有A、B、C三种元素,已知A的气态氢化物的分子式为H2A,则A的最高价有机物为AO3,A是氢化物的式量与A的最高价氧化物的式量之比为1:2.35,设A的相对分子质量为x,则(x+2):(x+48)=1:2.35,解得x=32,A的原子核内的质子数与中子数相等,则A的质子数为16,故A为S元素;B与A可形成离子化合物B2A,B+与A2-的电子层结构相同,则B为K元素;C与A(硫)处于同一周期,C的单质为双原子分子,则C为Cl.
解答 解:有A、B、C三种元素,已知A的气态氢化物的分子式为H2A,则A的最高价有机物为AO3,A是氢化物的式量与A的最高价氧化物的式量之比为1:2.35,设A的相对分子质量为x,则(x+2):(x+48)=1:2.35,解得x=32,A的原子核内的质子数与中子数相等,则A的质子数为16,故A为S元素;B与A可形成离子化合物B2A,B+与A2-的电子层结构相同,则B为K元素;C与A(硫)处于同一周期,C的单质为双原子分子,则C为Cl.
(1)由上述分析可知,A的质子数为16,则A的原子序数为16,
故答案为:16;
(2)由上述分析可知,A为S,B为K,C为Cl,
故答案为:S;K;Cl;
(3)K+离子结构示意图为 ,Cl原子的结构示意图为
,Cl原子的结构示意图为 ,
,
故答案为: ;
; ;
;
(4)A、B、C三种元素最高价氧化物对应水化物的化学式为H2SO4、KOH、HClO4,它们酸性由强到弱的排列顺序是:HClO4、H2SO4、KOH,
故答案为:H2SO4、KOH、HClO4;HClO4、H2SO4、KOH;
点评 本题考查结构性质位置关系应用,关键是计算确定A,侧重对元素周期律与化学用语的考查,比较基础.


 阳光课堂同步练习系列答案
阳光课堂同步练习系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
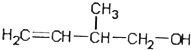 ,下列有关该物质叙述正确的是( )
,下列有关该物质叙述正确的是( )| A. | 不能与金属钠发生反应 | |
| B. | 不能使酸性高锰酸钾溶液褪色 | |
| C. | 在浓硫酸催化下.能与乙酸发生反应 | |
| D. | 常温下能与溴的四氯化碳溶液发生加成反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 元素编号 元素性质 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
| 原子半径(10-10m) | 0.74 | 1.60 | 1.52 | 1.10 | 0.99 | 1.86 | 0.75 | 1.43 |
| 最高或最低化合价 | +2 | +1 | +5 | +7 | +1 | +5 | +3 | |
| -2 | -3 | -1 | -3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
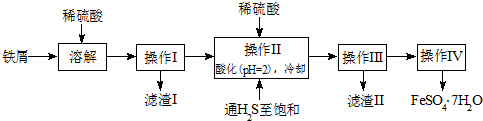
| 实验次数 | 初读数(mL) | 末读数(mL) |
| 1 | 0.20 | 21.40 |
| 2 | 0.00 | 21.00 |
| 3 | 1.60 | 26.60 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com