
| A. | O2,NO,HCl,NH3,CO2 | B. | O2,NO,NH3,HCl,SO2 | ||
| C. | NO,O2,NH3,HCl,SO2 | D. | HBr,Cl2,NH3,H2S,C2H4 |
分析 a,b相混合气体变成棕色,说明生成NO2,a、b为NO、O2中的一种,b,e分别通入氢硫酸中都产生淡黄色的沉淀,则b、e都具有氧化性,则b为O2,a为NO,c,d相混合生成白烟,应生成氯化铵,c、d为NH3、HCl中的一种,c,e分别通入少量溴水中,可知c为NH3,d为HCl,以此解答该题.
解答 解:a,b相混合气体变成棕色,说明生成NO2,a、b为NO、O2中的一种,b,e分别通入氢硫酸中都产生淡黄色的沉淀,则b、e都具有氧化性,则b为O2,a为NO,c,d相混合生成白烟,应生成氯化铵,c、d为NH3、HCl中的一种,c,e分别通入少量溴水中,可知c为NH3,d为HCl,e与硫化氢反应生成硫,可为SO2,
则a,b,c,d,e可能依次是NO,O2,NH3,HCl,SO2,
故选C.
点评 本题考查无机物的推断,侧重于元素化合物知识的综合理解和运用的考查,为高频考点,有助于培养学生的分析能力和双基,注意把握常见气体的性质以及反应现象,难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
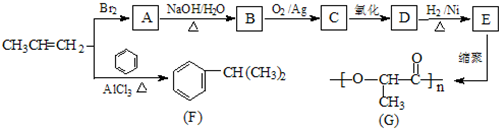
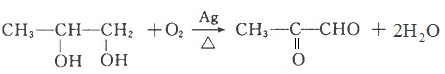 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 10g CO和10g N2 | B. | 10g C2H4和10g C3H6 | ||
| C. | 5.6L O2(标准状况)和0.5mol H2O | D. | 224mL He(标准状况)和1.6g CH4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加热 | B. | 加HCl | C. | 加NaOH | D. | 加AlCl3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 纯碱-Na2CO3 | B. | 熟石灰-Ca(OH)2 | ||
| C. | 明矾-Al2(SO4)3•12H2O | D. | 胆矾-CuSO4•5H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com