
【题目】下列反应中,属于消去反应的是( )
A. 苯与Fe、Br2混合B. 氯乙烷和NaOH溶液共热
C. 乙醇与乙酸反应生成乙酸乙酯D. 乙醇与浓硫酸共热到170℃
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】X、Y、Z、W四种物质有如下相互转化关系(其中X、W为单质,Y、Z为化合物,未列出反应条件)
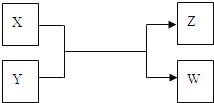
Ⅰ.若Z是生活中常用的调味品,W遇淀粉溶液变蓝,则:
(1)常温下,X的颜色是____________。
(2)工业上Z有多种用途,用化学方程式表示Z的一种用途_________________________。
(3)生活中所用的Z加入了碘酸钾,过量X与Y溶液反应时可以得到这种碘酸盐,此反应的离子方程式是______________________________________。
Ⅱ.若X是工业上用量最大的金属单质,Z是一种具有磁性的黑色晶体,则:
(1)X与Y反应的化学方程式是__________________________________。
(2)将3.48g Z加入50mL 4mol/L的稀HNO3中充分反应,产生112mL的NO(标准状况),向反应后的溶液中滴加NaOH溶液能产生沉淀.当沉淀量最多,至少需要加入2mol/L的NaOH溶液_____mL (精确到0.1)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子中,能在溶液中大量共存的是( )
A.Na+、Mg2+、Br-、SO42-B.K+、Ca2+、HCO3-、OH-
C.Fe2+、H+、SO42-、NO3-D.Na+、Cu2+、Cl-、S2-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定质量的Mg-Al合金投入100mL一定物质的量浓度的某HCl溶液中,充分反应。向反应后的溶液中逐滴加入一定物质的量浓度的NaOH溶液,生成沉淀的质量与所加NaOH溶液的体积关系如下图。回答下列问题:
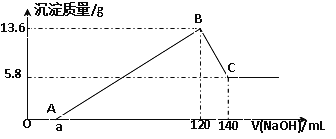
(1)写出OA段和BC段反应的离子方程式:OA:___________ ; BC:___________;
(2)原Mg-Al合金的质量是_____________。
(3)原NaOH溶液的物质的量浓度是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是
A.钠燃烧后得到白色的过氧化钠
B.单晶硅可作为光伏电池的材料
C.除去表面氧化膜的铝片在酒精灯上加热会剧烈燃烧
D.新制氯水使pH试纸先变红后褪色,说明其中含HCl和Cl2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁及铁的化合物应用广泛,如FeCl3可用作印刷电路铜板腐蚀剂。
(1)补全FeCl3溶液腐蚀印刷电路铜板的离子方程式(并配平):Fe3++ Cu=___________。
(2)将以上反应设计成原电池,写出电极反应式。正极反应___________;负极反应___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1 mol过氧化钠与2 mol碳酸氢钠固体混合后,在密闭容器中加热充分反应,排出气体物质后冷却,残留的固体物质是( )
A. Na2CO3 B. Na2O2、Na2CO3
C. NaOH、Na2CO3 D. Na2O2、NaOH、Na2CO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物AX3和单质X在一定条件下反应可生成化合物AX3。反应AX3(g)+X2(g)=AX5(g)在容积为10L的密闭容器中进行。起始时AX3和X2均为0.2mol.反应在不同条件下进行,反应体系总压强随时间的变化如图所示。回答下列问题:

(1)下列式计算实验a从反应开始至达到平衡时的反应速率v(AX5)=_________
(2)图中3组实验从反应开始至达到平衡时的反应速率v(AX5)由大到小的次序为____(填实验序号);与实验a相比,b改变的实验条件及判断依据是:_________
(3)用p0表示开始时总压强,p表示平衡时总压强,α表示AX5的平衡转化率,则a的表达式为_______;实验a和c的平衡转化率:αa为______,αc为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物的结构简式为CH2=CH-CH2-CH2OH,下列关于该有机物的叙述不正确的是( )
A. 能与金属钠发生反应并放出氢气
B. 能在催化剂作用下与H2发生加成反应
C. 能发生银镜反应
D. 在浓H2SO4催化下能与乙酸发生酯化反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com