
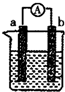
 ��ͼ��ij��ѧ��ȤС��̽����ͬ�����»�ѧ��ת��Ϊ���ܵ�װ�ã�
��ͼ��ij��ѧ��ȤС��̽����ͬ�����»�ѧ��ת��Ϊ���ܵ�װ�ã����� ��1��Fe��Cu��ϡ������Һ���ɵ�ԭ��أ�����Fe������������CuΪ�����������������ӵõ����ӣ�������Feʧȥ���ӣ�����n=$\frac{m}{M}$������������ʵ�����Ȼ������ת�Ƶ��ӵ����ʵ�����
��2�����缫aΪFe���缫bΪCu���������ҺΪ�Ȼ�����Һʱ������Ϊ��������Ϊͭ���������������õ����������������ӣ�
��3�����缫aΪFe���缫bʯī���������ҺΪϡ����ʱ��ʯī��ͭ��������ͬ����������������ط�Ӧ�루1����ͬ��
��� �⣺��1��Fe��Cu��ϡ������Һ���ɵ�ԭ��أ�����Fe������������CuΪ�����������������ӵõ����������������缫��ӦʽΪ��2H++2e-=H2����2.8g�������ʵ���Ϊ��$\frac{2.8g}{56g/mol}$=0.05mol��0.05mol����ȫ��Ӧʧȥ0.1mol���ӣ�
�ʴ�Ϊ��2H++2e-=H2����0.1��
��2�����缫aΪFe���缫bΪCu���������ҺΪ�Ȼ�����Һʱ������������������Ӧ�����������ӣ������ܹ��γ�ԭ��أ�����Ϊ��������Ϊͭ���������������õ����������������ӣ��缫��ӦʽΪ��Fe3++e-=Fe2+��
�ʴ�Ϊ���ܣ� Fe3++e-=Fe2+��
��3�����缫aΪFe���缫bʯī���������ҺΪϡ����ʱ��������ȻΪ��������Ϊʯī�������������ӵõ����������������缫��Ӧ�루1����ȫ��ͬ��
�ʴ�Ϊ����ͬ��
���� ���⿼����ԭ��ع���ԭ������Ӧ�ã���Ŀ�Ѷ��еȣ�ע������ԭ��ع���ԭ������ȷ�ж�ԭ����������ķ������ܹ���ȷ��д�缫��Ӧʽ������������ѧ�����Ӧ�û���֪ʶ��������


 �п������п��Ծ����ϵ�д�
�п������п��Ծ����ϵ�д� ��������״Ԫ��ϵ�д�
��������״Ԫ��ϵ�д� �ƸԿ�����ҵ��ϵ�д�
�ƸԿ�����ҵ��ϵ�д� ��Ԫ����ĩ��ϰ�ȷ��ϵ�д�
��Ԫ����ĩ��ϰ�ȷ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | AlCl3��NaOH | B�� | NaAl02��H2S04 | C�� | Na2C03��HCl | D�� | NaHS04��Ba��OH��2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | $\frac{a+b-2c}{4}$kJ | B�� | $\frac{a+2b-4c}{8}$kJ | C�� | $\frac{b-a-2c}{4}$kJ | D�� | $\frac{2b-a-4c}{8}$kJ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
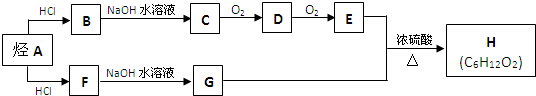
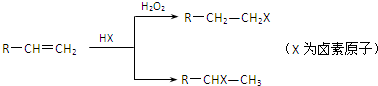
 CH3CH2COOCH��CH3��2+H2O��
CH3CH2COOCH��CH3��2+H2O�� �����ýṹ��ʽ��ʾ��
�����ýṹ��ʽ��ʾ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| X | Y | ||
| Z | W |
| A�� | X��Y��Z��W����Ԫ�ؾ�Ϊ�ǽ���Ԫ�� | |
| B�� | Y��W������⻯���У�Y�ķе�� | |
| C�� | X��Y��Z��W����������Ϊ���ۻ����� | |
| D�� | WԪ�صļ����Ӱ뾶С��ZԪ�صļ����Ӱ뾶 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ���� | Ŀ�� | ���ӷ���ʽ | |
| A | �кͷ� | ��H2SO4�кͼ��Է�ˮ | H++OH-�TH2O |
| B | ������ | ��ȥˮ�������� | Al3++H2O�TAl��OH��3��+H+ |
| C | ������ | ��ȥ��ˮ�е�Hg2+ | Hg2++Na2S�THgS��+Na+ |
| D | ������ | ���� | Cl2+2OH-�TCl-+ClO-+H2O |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
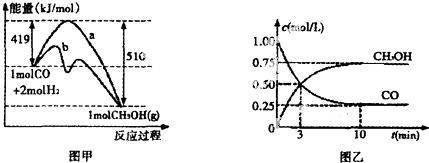
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
 Ӣ����ѧ�ҽ����з���һ����ΪNOTT-202a�����Ͷ�ײ��ϣ��������������������ͨ����Щ������CO2�ᱻ�������ò��ϵķ��ӽṹ��Ԫ������ԭ��Ϊ���ģ���Χ���Ը����л�����������֯�ɵġ����ӡ��������Ͽ����ֳ������������Щ������Ȼ���еķ��ѽṹ�������й�˵����ȷ���ǣ�������
Ӣ����ѧ�ҽ����з���һ����ΪNOTT-202a�����Ͷ�ײ��ϣ��������������������ͨ����Щ������CO2�ᱻ�������ò��ϵķ��ӽṹ��Ԫ������ԭ��Ϊ���ģ���Χ���Ը����л�����������֯�ɵġ����ӡ��������Ͽ����ֳ������������Щ������Ȼ���еķ��ѽṹ�������й�˵����ȷ���ǣ�������| A�� | �ò�����һ�����ͽ����л����� | |
| B�� | �ò����ܲ���CO2������ΪCO2��ò��Ϸ����˻�ѧ��Ӧ | |
| C�� | �ò��ϲ���11.2L CO2������22g | |
| D�� | �����øò��Ͻ������е�CO2��ȫ�������Ӷ���������ЧӦ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com