
【题目】NOx(主要指NO和NO2)是大气主要污染物之一。有效去除大气中的NOx是环境保护的重要课题。
(1)用水吸收NOx的相关热化学方程式如下:
2NO2(g)+H2O(l)![]() HNO3(aq)+HNO2(aq) ΔH=116.1 kJ·mol1
HNO3(aq)+HNO2(aq) ΔH=116.1 kJ·mol1
3HNO2(aq)![]() HNO3(aq)+2NO(g)+H2O(l) ΔH=75.9 kJ·mol1
HNO3(aq)+2NO(g)+H2O(l) ΔH=75.9 kJ·mol1
反应3NO2(g)+H2O(l)![]() 2HNO3(aq)+NO(g)的ΔH=___________kJ·mol1。
2HNO3(aq)+NO(g)的ΔH=___________kJ·mol1。
(2)在有氧条件下,新型催化剂M能催化NH3与NOx反应生成N2。现将一定比例的O2、NH3和NOx的混合气体,匀速通入装有催化剂M的反应器中反应。

反应相同时间NOx的去除率随反应温度的变化曲线如图所示,在50~250 ℃范围内随着温度的升高,NOx的去除率先迅速上升后上升缓慢的主要原因是______________________ ;
当反应温度高于380 ℃时,NOx的去除率迅速下降的原因可能是___________________ 。

【答案】-136.2 迅速上升段是催化剂活性随温度升高增大与温度升高共同使NOx去除反应速率迅速增大,上升缓慢段主要是温度升高引起的NOx去除反应速率增大 催化剂活性下降,NH3与O2反应生成了NO
【解析】
(1). 已知①2NO2(g)+H2O(l)![]() HNO3(aq)+HNO2(aq) ΔH=116.1 kJ·mol1、②3HNO2(aq)
HNO3(aq)+HNO2(aq) ΔH=116.1 kJ·mol1、②3HNO2(aq)![]() HNO3(aq)+2NO(g)+H2O(l) ΔH=75.9 kJ·mol1,根据盖斯定律,(①×3+②)÷2得3NO2(g)+H2O(l)
HNO3(aq)+2NO(g)+H2O(l) ΔH=75.9 kJ·mol1,根据盖斯定律,(①×3+②)÷2得3NO2(g)+H2O(l)![]() 2HNO3(aq)+NO(g) ΔH=(-116.1 kJ·mol1×3+75.9 kJ·mol1)÷2=-136.2kJ·mol1,故答案为:-136.2;
2HNO3(aq)+NO(g) ΔH=(-116.1 kJ·mol1×3+75.9 kJ·mol1)÷2=-136.2kJ·mol1,故答案为:-136.2;
(2). 在50~250℃范围内曲线迅速上升的主要原因是催化剂的活性随温度升高而增大使反应速率迅速增大,且温度升高也使NOx去除反应速率增大,上升缓慢的原因是温度升高引起去除反应速率增大,但此时催化剂的活性下降,当反应温度高于380℃时,NOx的去除率迅速下降的原因可能是催化剂活性下降,且NH3与O2反应生成了NO,故答案为:迅速上升段是催化剂活性随温度升高增大与温度升高共同使NOx去除反应速率迅速增大,上升缓慢段主要是温度升高引起的NOx去除反应速率增大;催化剂活性下降,NH3与O2反应生成了NO。


 智慧小复习系列答案
智慧小复习系列答案科目:高中化学 来源: 题型:
【题目】在下列变化①大气固氮②硝酸分解③实验室制取氨气中,按氮元素被氧化、被还原、既不被氧化又不被还原的顺序排列,正确的是
A.③①②B.②①③C.③②①D.①②③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】M是第四周期元素,最外层只有1个电子,次外层的所有原子轨道均充满电子。元素Y的负一价离子的最外层电子数与次外层的相同。回答下列问题:
(1)单质M的晶体中原子间通过______________________作用形成面心立方密堆积,其中M原子的配位数____________。
(2)元素Y的含氧酸中,酸性最强的是________________(写化学式),该酸根离子的立体构型为______________________。
(3)M与Y形成的一种化合物的立方晶胞如图所示。
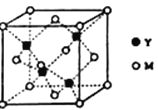
①该化合物的化学式为______________________,已知晶胞参数a=0.542 nm,此晶体的密度为__________________________g·cm–3。(只写出计算式,阿伏加德罗常数为NA)
②该化合物难溶于水但易溶于氨水,其原因是:_____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有下列九种物质:①盐酸溶液 ②石墨 ③蔗糖 ④CO2⑤熔融NaHSO4⑥Ba(OH)2固体 ⑦氨水 ⑧纯硫酸 ⑨NaCl固体
(1)属于电解质的有__________;属于非电解质的有________;能导电的物质有________。
(2)②和SiO2在高温下可发生如下反应:3C+SiO2![]() SiC+2CO↑ (已知SiC中Si元素为+4价),上述反应中还原产物是_______;氧化剂与还原剂物质的量之比为_______。
SiC+2CO↑ (已知SiC中Si元素为+4价),上述反应中还原产物是_______;氧化剂与还原剂物质的量之比为_______。
(3)上述九种物质中有两种物质之间可发生离子反应:H++OH-===H2O,该离子反应对应的化学方程式为________________________
(4)⑤的电离方程式为______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,向1L密闭容器中加入1 mol HI(g),发生反应2HI(g) ![]() H2(g)+I2(g),H2物质的量随时间的变化如图所示。
H2(g)+I2(g),H2物质的量随时间的变化如图所示。

(1)0~2 min内的平均反应速率v(HI)=______________________。 该温度下,H2(g)+I2(g) ![]() 2HI(g)的平衡常数K=________。
2HI(g)的平衡常数K=________。
(2)相同温度下,若开始加入HI(g)的物质的量是原来的2倍,则_________原来的2倍。
a.平衡常数 b.HI的平衡浓度
c.达到平衡的时间 d.平衡时H2的体积分数
(3)实验室用Zn和稀硫酸制取H2,反应时溶液中水的电离平衡________移动(填“向左”、“向右”或“不”);若加入少量下列试剂中的_______,产生H2的速率将增大。
a.NaNO3 b.CuSO4 c.Na2SO4 d.NaHSO3
(4)某固体酸燃料电池以CsHSO4固体为电解质传递H+,其基本结构如图,电池总反应可表示为2H2+O2===2H2O,下列有关说法正确的是___________

A.电子通过外电路从b极流向a极
B.b极上的电极反应式为:O2+2H2O+4e-=4OH-
C.每转移0.1mol电子,消耗1.12L的H2
D.H+由a极通过固体酸电解质传递到b极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于化合物2-苯基丙烯 ,下列说法错误的是
,下列说法错误的是
A. 分子式为C9H10
B. 一定条件下,可以发生取代、加成和氧化反应
C. 1 mol该化合物最多可与4mol氢气发生加成反应
D. 分子中最多有8个碳原子在同一平面上
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】PCl3和Cl2在一定条件下反应生成PCl5。
(1)有88 g CO2与足量H2恰好完全反应,生成气态水和甲醇,可放出1.2014×105 J的热量,试写出该反应的热化学方程式_______________________________________。
(2)25 ℃、101 kPa下,CH4的燃烧热为a kJ/mol,9 g液态水变为水蒸气吸热b kJ,则CH4燃烧生成二氧化碳和水蒸气热化学方程式为________________________________。
(3)硅与氯两元素的单质反应生成1mol硅的最高价化合物,恢复至室温,放热687kJ,已知该化合物的熔、沸点分别为-69℃和58℃,写出该反应的热化学方程式:________________________________________________。
(4)CO2与CH4经催化重整制得合成气:CH4(g)+ CO2(g) ![]() 2CO (g)+ 2H2(g)已知上述反应中相关的化学键键能数据如下:
2CO (g)+ 2H2(g)已知上述反应中相关的化学键键能数据如下:
化学键 | C—H | C=O | H—H | C |
键能/kJ·mol1 | 413 | 745 | 436 | 1075 |
则该反应的ΔH=________________________________。
(5)利用含硫物质热化学循环实现太阳能的转化与存储。过程如下:

反应Ⅰ:2H2SO4(l)![]() 2SO2(g)+2H2O(g)+O2(g) ΔH1=+551 kJ·mol-1
2SO2(g)+2H2O(g)+O2(g) ΔH1=+551 kJ·mol-1
反应Ⅲ:S(s)+O2(g)![]() SO2(g) ΔH3=-297 kJ·mol-1
SO2(g) ΔH3=-297 kJ·mol-1
反应Ⅱ的热化学方程式:___________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】回收利用CO2是环境科学研究的热点课题,是减轻温室效应危害的重要途径。
(1)工业上,利用天然气与二氧化碳反应制备合成气(CO和H2),化学方程式为CO2(g)+CH4(g)=2CO(g)+2H2O(g)上述反应的能量变化如图1所示,该反应是________(填“吸热反应,或“放热反应”)。

(2)工业上用CO2生产甲醇(CH3OH)燃料,可以将CO2变废为宝。在体积为1L的密闭容器中,充入1molO2和4molH2,一定条件下发-反应:CO2(g)+3H2(g)=CH3OH(g)+H2O(g),测得CO2(g)和CH3OH(g)的浓度随时间变化如上图2所示。
①从反应开始到平衡,用CH3OH表示的平均反应速率为______。
②若反应CO2(g)+3H2(g)=CH3OH(g)+H2O(g)在四种不同情况下的反应速率分别为:
A.v(H2)=0.01molL-1s-1 B.v(CO2)=0.15molL-1s-1
C.v(CH3OH)=0.3molL-1min-1 D.v(H2O)=0.45molL-1min-1
该反应进行由快到慢的顺序为______(填字母)。
③下列描述能说明反应达到最大限度的是_______(填字母)。
A.混合气体的密度保持不变
B.混合气体中CH3OH的体积分数约为21.4%
C.混合气体的总质量保持不变
D.H2、CH3OH的生成速率之比为3:1
(3)甲醇(CH3OH)是一种可再生能源,具有广阔的开发和应用前景。以甲醇、氧气和KOH溶液为原料,石墨为电极制造新型手机电池,甲醇在______极反应,电极反应式为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中不正确的是( )
A.  能使溴水、酸性高锰酸钾溶液褪色
能使溴水、酸性高锰酸钾溶液褪色
B. 用燃烧法鉴别乙醇、苯和四氯化碳
C. 油脂的种类很多,但它们水解后都一定有一产物相同
D. 向蔗糖溶液中加入几滴稀硫酸,水浴加热几分钟,再加入新制银氨溶液,水浴加热,来检验蔗糖水解产物具有还原性
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com