
| A. | 煤、石油、天然气是当今世界最重要的三种化石燃料 | |
| B. | 化学反应必然伴随发生能量变化 | |
| C. | 利用生物质能就是间接利用太阳能 | |
| D. | 凡经加热而发生的化学反应都是吸热反应 |
分析 A.煤、石油、天然气均为化石燃料;
B.化学反应中能量守恒、质量守恒;
C.生物质能是指是太阳能以化学能形式贮存在生物质中的能量形式,利用生物质能,就是间接利用太阳能;
D.根据吸热反应实质是反应物所具有的总能量低于生成物所具有的总能量来解答.
解答 解:A.煤、石油、天然气均为化石燃料,是当今世界最重要的三种化石燃料,故A正确;
B.因化学反应中能量守恒,所以化学反应必然伴随发生能量变化,为吸热反应或放热反应,故B正确;
C.利用生物质能就是间接利用太阳能,生物质能是指是太阳能以化学能形式贮存在生物质中的能量形式,即以生物质为载体的能量.它直接或间接地来源于绿色植物的光合作用,可转化为常规的固态、液态和气态燃料,取之不尽、用之不竭,是一种可再生能源,故C正确;
D.放热反应有的需加热,有的不需加热,如木炭的燃烧是一个放热反应,但需要点燃,点燃的目的是使其达到着火点.再如铝热反应也是,吸热反应实质是反应物所具有的总能量低于生成物所具有的总能量,吸热反应与反应条件无关,故D错误;
故选D.
点评 本题考查了化石燃料、生物质能、化学能与热能,明确化学反应中能量变化的实质是解答关键,题目难度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | ①②④ | B. | ③⑤ | C. | ②④⑤ | D. | ③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 原子半径大小:Na>S>O | B. | 还原性强弱:F->Cl->Br->I- | ||
| C. | 碱性强弱:KOH>NaOH>LiOH | D. | 气态氢化物稳定性:HBr>HCl>HF |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | SO2、Cl2都能使品红溶液褪色 | |
| B. | NH4Cl晶体、固体碘受热时都能气化 | |
| C. | 福尔马林、葡萄糖与新制Cu(OH)2共热时都能产生红色沉淀 | |
| D. | 乙烯通入酸性高锰酸钾溶液和溴水都能使其褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

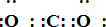 ;写出物质E的电子式:
;写出物质E的电子式: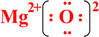 .
.查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com