
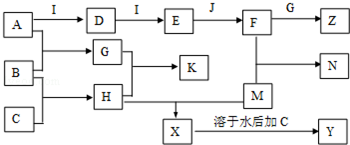
分析 A、B、C、D、E、G、H、I均为气体,A、B、C、I、M为单质,根据题中各物质转化关系,A和B反应生成G,B和C反应生成H,G和H相遇时产生白烟,则该反应为氨气与氯化氢的反应,所以K为NH4Cl,B为H2,A能与I连续反应,且E与J反应,J为常见的液态物质,所以I为O2,J为H2O,则A为N2,所以G为NH3,则H为HCl,D为NO,E为NO2,F为HNO3,F和G反应生成Z为NH4NO3,M能与H盐酸反应生成X,X可以继续与C反应,且M为常用金属,则M为Fe,所以X为FeCl2,Y为FeCl3,铁与硝酸反应生成N为Fe(NO3)3,据此答题.
解答 解:A、B、C、D、E、G、H、I均为气体,A、B、C、I、M为单质,根据题中各物质转化关系,A和B反应生成G,B和C反应生成H,G和H相遇时产生白烟,则该反应为氨气与氯化氢的反应,所以K为NH4Cl,B为H2,A能与I连续反应,且E与J反应,J为常见的液态物质,所以I为O2,J为H2O,则A为N2,所以G为NH3,则H为HCl,D为NO,E为NO2,F为HNO3,F和G反应生成Z为NH4NO3,M能与H盐酸反应生成X,X可以继续与C反应,且M为常用金属,则M为Fe,所以X为FeCl2,Y为FeCl3,铁与硝酸反应生成N为Fe(NO3)3,
(1)根据上面的分析可知,A为N2,K为NH4Cl,K的名称为氯化铵,F为HNO3,硝酸常用作制造氮肥、染料塑料、炸药硝酸盐等,
故答案为:N2;氯化铵;制造氮肥、染料塑料、炸药硝酸盐等;
(2)①实验室用氯化铵与氢氧化钙反应制取氨气,反应的化学方程式为2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O,
故答案为:2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O;
②实验室检验氨气是否收集满的方法可以用湿润的红色石蕊试纸置于集气瓶口,如果红色石蕊试纸变蓝,则说明收集满,
故答案为:用湿润的红色石蕊试纸置于集气瓶口,如果红色石蕊试纸变蓝,则说明收集满;
③氨气在一定条件下催化氧化也可生成NO,该反应的化学方程式为4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O,
故答案为:4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O;
(3)①浓硝酸与木炭在加热的条件下反应,反应的化学方程式为C+4HNO3(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+4NO2↑+2H20,
故答案为:C+4HNO3(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+4NO2↑+2H20;
②浓硝酸部分分解,溶液中含有少量的二氧化氮,所以溶液呈黄色,其化学方程式为4HNO3(浓)$\frac{\underline{\;\;△\;\;}}{\;}$4NO2↑+O2↑+2H2O,若要消除黄色可向其中通入一定量的氧气,二氧化氮、氧气、水反应生成硝酸,
故答案为:4HNO3(浓)$\frac{\underline{\;\;△\;\;}}{\;}$4NO2↑+O2↑+2H2O; 氧气.
点评 本题考查无机物的推断,明确物质的颜色及性质是解答本题的关键,注意B、K是解答本题的突破口,并规范化学用语的应用,题目难度中等.


科目:高中化学 来源: 题型:解答题
 电化学原理在医学医疗中有重要应用.
电化学原理在医学医疗中有重要应用.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 硫酸亚铁是重要的亚铁盐,在农业上用作农药,主要治小麦黑穗病,还可以用作除草剂;在工业上用于染色、制造蓝黑墨水和木材防腐等.
硫酸亚铁是重要的亚铁盐,在农业上用作农药,主要治小麦黑穗病,还可以用作除草剂;在工业上用于染色、制造蓝黑墨水和木材防腐等.| 操作步骤 | 预期实验现象 | 预期实验结论 |
| 向其中一份溶液中加入KSCN溶液 , | 溶液变成血红色 | 固体中含有Fe2O3 |
| 向另一份溶液中滴加2滴黄色K3[Fe(CN)6]溶液 | 产生蓝色沉淀 | 固体中含有FeO |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 CO(g)+H2(g).
CO(g)+H2(g).| 温度/℃ | 400 | 500 | 800 |
| 平衡常数K | 9.94 | 9 | 1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②④⑥⑦ | B. | ②⑤⑦⑧ | C. | ①③⑤⑥ | D. | ②⑤⑥⑧ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HF、HCl、H2S、PH3的稳定性依次增强 | |
| B. | Na、Mg、Al、Si的还原性逐渐增强 | |
| C. | O、S、Na、K的原子半径依次增大 | |
| D. | KOH、Ca(OH)2、Mg(OH)2、Al(OH)3的碱性逐渐增强 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com