
【题目】碲(Te)是一种第VIA族分散稀有元素,主要伴生于铜、镍、铅等金属矿藏中。TeO2属于两性氧化物,难溶于水,易溶于强酸和强碱。工业上可从电解精炼铜的阳极泥(主要成分Cu2Te,还有少量的Ag、Au)中提取碲。其工艺流程如下:
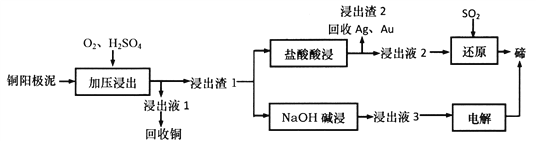
(1)“加压浸出”生成TeO2的离子方程式为________________________,“加压浸出”时控制pH为4.5~5.0,酸性不能过强的原因是_________________________________。
(2)“盐酸酸浸”后将SO2通入浸出液即可得到单质碲,该反应中氧化剂与还原剂物质的量之比为________________,该流程中可循环利用的物质是_____________(填化学式)。
(3)已知:Ksp(Ag2SO4)=7.70×10-5,Ksp(AgC1)=1.80×10-10。盐酸酸浸时,“浸出渣1”中Ag2SO4可充分转化为AgC1。通过计算说明为什么可以实现充分转化_________________。
(4)NaOH碱浸时反应的离子方程式为__________________。流程中,电解过程用石墨为电极得到碲,阴极的电极反应式为__________________________________。
(5)浸出法是工业提取金属常用的方法,某实验小组用1.0mol· L-1的草酸在75℃时浸出镍。随时间变化,不同固液比对镍浸出率的影响曲线如图所示。
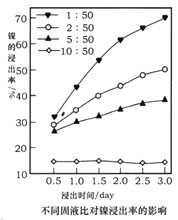
①由图可知,固液比与镍浸出率的关系是______________________。
②除固液比之外,你认为影响金属浸出率的因素还有____________________(至少两项)。
【答案】 Cu2Te+2O2+4H+=2Cu2++TeO2+2H2O 酸性过强TeO2会被酸溶解导致Te产率降低 1:2 H2SO4、HCl ![]() TeO2+2OH-=TeO32-+H2O TeO32-+4e-+3H2O=Te+6OH- 固液比越小,镍的浸出率越高 金属本身、浸液的选择、温度、浓度、浸出时间、搅拌速度等
TeO2+2OH-=TeO32-+H2O TeO32-+4e-+3H2O=Te+6OH- 固液比越小,镍的浸出率越高 金属本身、浸液的选择、温度、浓度、浸出时间、搅拌速度等
【解析】试题分析:本题以电解精炼铜的阳极泥中提取碲的流程为载体,考查流程的分析、方程式的书写、氧化还原反应的分析、溶度积的计算、电解原理、图像的分析。
(1)“加压浸出”时加入O2、H2SO4,根据流程和题意,Cu2Te与O2、H2SO4反应生成CuSO4、TeO2和水,反应的化学方程式为Cu2Te+2O2+2H2SO4=2CuSO4+TeO2+2H2O。反应的离子方程式为Cu2Te+2O2+4H+=2Cu2++TeO2+2H2O。“加压浸出”时控制pH为4.5~5.0,酸性不能过强的原因是:TeO2属于两性氧化物,易溶于强酸和强碱,酸性过强TeO2会被酸溶解导致Te产率降低。
(2)TeO2属于两性氧化物,易溶于强酸和强碱,“盐酸酸浸”时TeO2发生的反应为TeO2+4HCl=TeCl4+2H2O;向浸出液中通入SO2得到单质Te,TeCl4为氧化剂,被还原成Te,SO2为还原剂,被氧化成SO42-,根据得失电子守恒,4n(TeCl4)=2n(SO2),n(TeCl4):n(SO2)=1:2,该反应中氧化剂与还原剂物质的量之比为1:2。反应的化学方程式为:TeCl4+2SO2+4H2O=Te+2H2SO4+4HCl,该流程中可循环利用的物质的化学式为:H2SO4、HCl。
(3)Ag2SO4转化为AgCl的反应为Ag2SO4(s)+2Cl-(aq)![]() 2AgCl(s)+SO42-(aq),该反应的平衡常数K=
2AgCl(s)+SO42-(aq),该反应的平衡常数K=![]() =
=![]() =
=![]() =
=![]() =2.38
=2.38![]() 1015
1015![]() 105,Ag2SO4可充分转化为AgCl。
105,Ag2SO4可充分转化为AgCl。
(4)TeO2属于两性氧化物,易溶于强酸和强碱,NaOH碱浸时反应的化学方程式为TeO2+2NaOH=Na2TeO3+H2O,离子方程式为TeO2+2OH-=TeO32-+H2O。用石墨为电极电解Na2TeO3溶液得到Te,Te元素的化合价由+4价降至0价,电解时阴极发生得电子的还原反应,阴极的电极反应式为TeO32-+4e-+3H2O=Te+6OH-。
(5)①根据图像,固液比与镍浸出率的关系是:浸出时间相同时,固液比越小,镍的浸出率越高。
②除固液比之外,影响金属浸出的因素还有:金属本身、浸液的选择、温度、浓度、浸出时间、搅拌速度等。


科目:高中化学 来源: 题型:
【题目】如图是实验室研究潜水艇中供氧体系反应机理的装置图(夹持仪器略)。
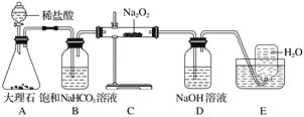
(1)A装置为CO2的发生装置,反应的离子方程式为____________________。
(2)B装置可除去A装置中可能挥发出的___________,反应的离子方程式为_______________。
(3)C装置为O2的发生装置,反应的化学方程式为__________________、________________。
(4)D装置可除去C装置中未反应的__________,反应的离子方程式为____________________。
(5)E装置为排水法收集O2的装置,检验所收集的气体为O2的方法为_____________________。
(6)C装置中固体由淡黄色完全变为白色,检验固体成分的实验方案为取少量C装置中反应后的固体溶于水,向溶液中滴入过量___溶液,若有白色沉淀生成,则证明固体中含有___;过滤,向滤液中滴入几滴酚酞溶液,若__且不褪色,则证明固体中含有__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学在实验报告中记录下列数据,其中正确的是( )
A.用25mL量筒量取12.36mL盐酸
B.用托盘天平称量8.75g食盐
C.用500mL的容量瓶配制480mL溶液
D.用广泛pH试纸测得某溶液的pH为3.5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2017年3月21日是第二十五届“世界水日”,保护水资源,合理利用废水节省水资源,加强废水的回收利用已被越来越多的人所关注。已知:某无色废水中可能含有H+、NH4+、Fe3+、Al3+、Mg2+、Na+、NO3-、CO32-、SO42-中的几种,为分析其成分,分别取废水样品1L,进行了三组实验,其操作和有关图像如下所示:

请回答下列问题:
(1)根据上述3组实验可以分析废水中一定不存在的阴离子是__________,一定存在的阳离子是___________。
(2)写出实验③图像中沉淀达到最大量且质量不再发生变化阶段发生反应的离子反应方程式:________。
(3)分析图像,在原溶液中c(NH4+)与c(Al3+)的比值为______,所得沉淀的最大质量是______g。
(4)若通过实验确定原废水中c(Na+)=0.18 mol·L-1,试判断原废水中NO3-是否存在?____(填“存在”“不存在”或“不确定”)。若存在, c(NO3-) = _____ mol·L-1。(若不存在或不确定则此空不填)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过氧化钠常作漂白剂、杀菌剂、消毒剂。过氧化钠保存不当容易吸收空气中CO2而变质。
(1)某课外活动小组欲探究某过氧化钠样品是否已经变质,取少量样品,溶解,加入______溶液,充分振荡后有白色沉淀,证明Na2O2已经变质。
(2)该课外活动小组为了粗略测定过氧化钠的纯度,他们称取a g样品,并设计用如图装置来测定过氧化钠的质量分数。
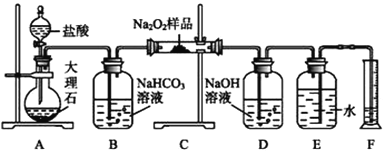
①将仪器连接好以后,必须进行的第一步操作是____________________________________。
②B装置出来的气体是否需要干燥______(填“是”或“否”)。
③D中NaOH溶液的作用____________________。
④实验结束时,读取实验中生成气体的体积时,不合理的是__________。
a.直接读取气体体积,不需冷却到室温
b.上下移动量筒,使得E、F中液面高度相同
c.视线与凹液面的最低点相平读取量筒中水的体积
⑤读出量筒内水的体积后,折算成标准状况下氧气的体积为V mL,则样品中过氧化钠的质量分数为_____________。
⑥实验完成后E到F之间导管内残留水的体积会使测量结果________(填“偏大”“偏小”或“不影响”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】掌握仪器的名称、组装及使用方法是中学化学实验的基础,根据如图所示实验装置,回答下列问题。
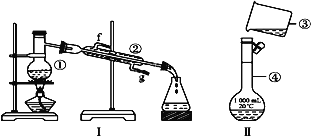
(1)写出下列仪器的名称:①______________,②_____________,④____________。
(2)仪器①~④中,使用时必须检查是否漏水的是____________(填序号)。
(3)若分离酒精和水的混合物,分离方法为___________,该方法适用于分离________不同的混合物,若利用装置Ⅰ分离酒精和水的混合物,还缺少的仪器是_____________;②的进水口是____________(填“f”或“g”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】KClO3和浓盐酸在一定温度下反应,会生成橙黄色的易爆物二氧化氯(ClO2)气体,该反应的化学方程式为2KClO3+4HCl(浓) === 2KCl + 2ClO2↑+ Cl2↑+ 2H2O。
(1)该反应中还原产物与氧化产物的物质的量之比为_________________。
(2)若该反应中有490克KClO3参加反应,则被氧化的HCl的质量为______________。
(3)若该反应产生2.24L(标准状况)ClO2,则转移的电子数目为_____________。
(4)某地生产的食盐氯化钠中含有少量的剧毒物质氰化钠(NaCN),用ClO2可除去其中的氰化钠,从而得到纯净的食盐,同时产生两种无毒气体。写出该反应的化学方程式: ______________________。
(5)用双线桥法表示下列氧化还原反应的电子转移情况:____________________
2KClO3+4HCl(浓) === 2KCl + 2ClO2↑+ Cl2↑+ 2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作错误的是( )
A.分液漏斗使用前需要先检查是否漏液
B.试验中剩余的钠不能再放回原试剂瓶
C.做焰色反应时,铂丝应用盐酸洗净并灼烧至无色
D.蒸馏烧瓶加热时需要垫石棉网
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com