
短周期元素a、b、c、d的原子序数依次增大,c和d位于同主族且原子序数相差8;基态a原子核外有3个能级上容纳电子且每个能级上电子数相等,c原子s能级电子总数与p能级电子数相等,基态e原子的M层上有2个未成对电子且无空轨道。
(1)在a、b、c中,第一电离能由大到小排序为 (用元素符号表示);基态e原子的价层电子排布式为 。
(2)配合物e(ac)4在常温下呈液态,易溶于四氯化碳、苯等有机溶剂。固态e(ac)4的晶体类型是 。已知(dab)2分子中含非极性键,分子中每个原子最外层都达到8个电子稳定结构,1mol(dab)2分子含σ键的数目为 。
(3)写出一种与dab-互为等电子体的分子 (填化学式)。ac32-的中心原子杂化类型为 ;dc32-的空间构型为 。
(4)ec晶胞结构如图所示,其晶胞参数为a pm,列式计算该晶胞的密度为 g·cm-3(不必计算出结果,阿伏伽德罗常数的值为NA),晶胞中c粒子的配位数为 。
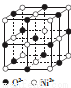
(5)人工合成的ec晶胞存在缺陷,即阳离子有+3、+2价两种。某人工合成的晶体样品组成为e0.96c,则该晶体中+3价、+2价两种离子的个数之比为 。
科目:高中化学 来源:2016-2017年新疆兵团第二师华山中学高二上学前考化学卷(解析版) 题型:推断题
元素周期表与元素周期律在学习、研究和生产实践中有很重要的作用。下表列出了①~⑨九种元素在周期表中的位置。请用相关的化学术语回答下列问题:
族 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA[ | 0 |
2 |
|
|
| ⑤ |
| ⑥ | ⑦ |
|
3 | ① | ③ | ④ |
|
|
| ⑧ | ⑨ |
4 | ② |
|
|
|
|
|
|
|
(1) 在这些元素中,最不活泼的是 ,非金属性最强的是___________,金属性最强的是___________;(填元素符号或化学式,下同。)
(2) 这些元素形成的最高价氧化物对应的水化物中碱性最强的 ,酸性最强的__________;
(3) ①、②、③、④、⑤这五种元素的原子半径由大到小的顺序为 ;
(4) ⑥的氢化物的电子式为 ,① 在空气中燃烧后生成产物的电子式 。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年辽宁省高一上开学考化学卷(解析版) 题型:填空题
二氧化碳的摩尔质量为 ,22gCO2的物质的量为 ,所含的分子数为 个,标准状况下,该气体所占的体积为 。将其溶于水配制成500ml溶液,其物质的量浓度为 ,从中取出1ml,其物质的量浓度为 。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江大庆实验中学高一上开学考化学卷(解析版) 题型:实验题
某同学对“菠菜中富含可溶性草酸盐和碳酸盐,与豆腐同食会引起结石”的说法产生了兴趣。
探究一 菠菜里是否含有可溶性草酸盐和碳酸盐?
【查阅资料】
①可溶的草酸盐、碳酸盐能与CaCl2溶液反应生成难溶于水的草酸钙(CaC2O4)、碳酸钙。
②醋酸不与草酸钙反应,但能与碳酸钙反应生成可溶性盐。
【实验流程】
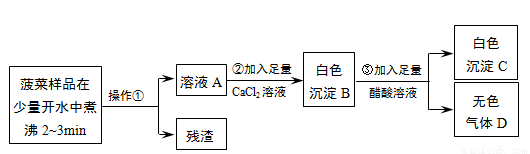
根据流程回答问题:(1)操作①是_________。 ( 2)加入足量CaCl2溶液的目的是_________。
(3)已知气体D能使澄清石灰水变浑浊,步骤③的化学反应方程式为_________。
【实验结论】菠菜里含有可溶性草酸盐和碳酸盐。
探究二 人体结石的主要成分是草酸钙,草酸钙高温分解的产物是什么?
【查阅资料】
① 草酸钙高温完全分解得到两种气态氧化物和一种固态氧化物。
② 12.8 g的草酸钙分解过程中温度与剩余固体的质量关系如下图所示。
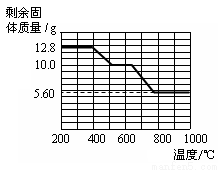
【实验分析】(4)草酸钙高温完全分解的化学方程式为_____________。
(5)通过上图数据分析,700℃时剩余固体的成分是_____________。
(6)请你设计实验,验证700℃时剩余固体的成分。
实验操作 | 实验现象 | 实验结论 |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江大庆实验中学高一上开学考化学卷(解析版) 题型:选择题
除去下列物质中混有的少量杂质,所用除杂试剂及操作方法均正确的是( )
选项 | 物质 | 杂质 | 除杂试剂及操作方法 |
A | FeCl2溶液 | CuCl2溶液 | 加入过量铁粉,充分反应后过滤 |
B | KCl固体 | MnO2固体 | 加足量的水溶解、过滤、洗涤、干燥 |
C | CaO | CaCO3 | 加入适量的稀盐酸至不再生产气体为止 |
D | Cu | C | 在空气中灼烧 |
查看答案和解析>>
科目:高中化学 来源:2017届安徽省高三上学期第一次月考化学试卷(解析版) 题型:选择题
在含有Fe3+、Fe2+、Al3+、NH4+的溶液中,加入足量的Na2O2固体,微热充分反应后,再加入过量的稀盐酸,完全反应后,离子数目没有变化的是
A.Fe3+ B.Al3+ C.Fe2+ D.NH4+
查看答案和解析>>
科目:高中化学 来源:2017届安徽省高三上学期第一次月考化学试卷(解析版) 题型:选择题
下列根据实验操作和实验现象所得出的结论,正确的是
选项 | 实验操作 | 实验现象 | 结论 |
A | 向两份蛋白质溶液中分别滴加饱和Na2SO4溶液和CuSO4溶液 | 均有固体析出 | 蛋白质均发生变性 |
B | 在CuSO4溶液中加入KI溶液,再加入苯,振荡后静置 | 有白色沉淀生成,苯层呈紫红色 | 白色沉淀可能为CuI |
C | 将气体X通入品红溶液中 | 红色褪去 | X一定是SO2 |
D | 将Fe(NO3)2样品溶于稀H2SO4后,滴加KSCN溶液 | 溶液变为血红色 | Fe(NO3)2样品已氧化变质 |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山西省高二上开学考化学试卷(解析版) 题型:选择题
铁粉与足量1mol/l盐酸反应,为了加快反应速率且不影响产生氢气的量可以加入
①2mol/L的硝酸溶液 ②少量CuSO4(s) ③少量铜粉 ④少量CH3COONa(s) ⑤对溶液加热 ⑥向反应液中通入HCl气体 ⑦加入过量铁粉⑧将铁粉改为铁片
A.②③④⑤⑥ B.③⑤⑥ C.①③⑤⑥⑦ D.③⑤⑥⑧
查看答案和解析>>
科目:高中化学 来源:2017届湖北省高三上8月开学考化学试卷(解析版) 题型:选择题
设NA为阿伏伽德罗常数的值,下列叙述正确的是( )
A.10gT2O含有的电子数为5NA
B.常温下,0.2L 0.5mol·L-1NH4NO3溶液的氮原子数小于0.2NA
C.用惰性电极电解CuSO4溶液后,如果加入0.1mol Cu(OH)2能使溶液复原,则电路中转移电子的数目为0.4NA
D.常温常压下,5.6gC2H4和C3H6的混合气体中含氢原子数为0.9NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com