
A、按照系统命名法,化合物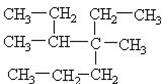 可命名为:4,5-二甲基-4-乙基庚烷 可命名为:4,5-二甲基-4-乙基庚烷 |
B、植物生长平衡因子“S-诱抗素”: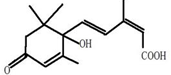 可以发生氧化、取代、酯化、加聚、缩聚反应,与盐酸反应还能生成盐 可以发生氧化、取代、酯化、加聚、缩聚反应,与盐酸反应还能生成盐 |
| C、甲苯的一氯代物和二氯代物的同分异构体总数共有14种 |
| D、分子式为C8H6O2的芳香族化合物中可能含有2个羟基,也可能含有一个羧基,但不可能含有两个醛基 |
 可命名为:3,4-二甲基-4-乙基庚烷,故A错误;
可命名为:3,4-二甲基-4-乙基庚烷,故A错误; 中的碳碳双键可以发生氧化反应,、羧基可以发生取代、酯化反应,碳碳双键可以发生加聚反应,羧基和醇羟基之间可以发生缩聚反应,不可以与盐酸反应生成盐,故B错误;
中的碳碳双键可以发生氧化反应,、羧基可以发生取代、酯化反应,碳碳双键可以发生加聚反应,羧基和醇羟基之间可以发生缩聚反应,不可以与盐酸反应生成盐,故B错误;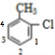 所示四种取代位置,有4种结构,
所示四种取代位置,有4种结构,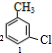 所示2种取代位置,有2种结构;
所示2种取代位置,有2种结构;

科目:高中化学 来源: 题型:
| 物质(杂质) | 除杂试剂 | 除杂方法 | |
| A | 乙醇(水) | CaO | 蒸馏 |
| B | 淀粉溶液(NaCl) | --- | 渗析 |
| C | CO2(HCl) | NaOH溶液 | 洗气 |
| D | NaCl溶液(I2) | CCl4 | 萃取分液 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、168mL | B、224mL |
| C、112mL | D、56mL |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、N2、H2、NH3浓度相等 |
| B、N2,H2,NH3分子数之比为1:3:2 |
| C、单位时间内生成nmolN2同时生成2nmolNH3 |
| D、单位时间内生成nmolN2同时生成3nmolH2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、该一元酸溶液的pH=1 | ||
| B、该溶液中水的离子积常数为1×10-22 | ||
| C、该溶液中HA的电离度为 0.1% | ||
D、若加水稀释,则
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、苯酚有一定毒性,不能作消毒剂和防腐剂 |
| B、棉花、羊毛、木材主要成分都是纤维素 |
| C、油脂皂化生成的高级脂肪酸钠是肥皂的有效成分 |
| D、用食醋去处水壶中的水垢时所发生的是水解放应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、人体缺碘,可通过食用加碘盐补碘 |
| B、染发剂有植物染发剂、无机染发剂、合成染发剂等 |
| C、若不慎接触敌敌畏或甲胺磷,最好用中性皂液清洗 |
| D、缺铁性贫血,可通过食用铁强化酱油预防 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 弱酸 | HCOOH | HNO2 | H2S | H2SO3 | H2C2O4 |
| 电离平衡常数 (25℃) | K=1.8×10-4 | K=5.1×10-4 | K1=9.1×10-8 K2=1.1×10-12 | K1=1.23×10-2 K2=6.6×10-8 | K1=5.4×10-2 K2=5.4×10-5 |
| A. | HNO2+HS-═NO2-+H2S↑ |
| B. | 2HCOOH+SO32-═2HCOO-+H2O+SO2↑ |
| C. | H2SO3+2HCOO-═2HCOOH+SO32- |
| D. | H2SO3+SO32-═2HSO3- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com