
 实验室用乙酸和正丁醇制备乙酸正丁酯.有关物质的相关数据如下表:
实验室用乙酸和正丁醇制备乙酸正丁酯.有关物质的相关数据如下表:| 化合物 | 相对分子质量 | 密度/g•cm-3 | 沸点/℃ | 溶解度/100g水 |
| 正丁醇 | 74 | 0.80 | 118.0 | 9 |
| 冰醋酸 | 60 | 1.045 | 118.1 | 互溶 |
| 乙酸正丁酯 | 116 | 0.882 | 126.1 | 0.7 |

分析 (1)冷凝作用的仪器是冷凝管,水从下口进上口出;
(2)根据酯化反应原理酸脱羟基醇脱氢写出反应的化学方程式;
(3)根据外界条件对化学平衡的影响分析;
(4)乙酸丁酯不溶于饱和碳酸钠溶液,乙酸与碳酸钠反应而被吸收;
(5)分液操作时下层液体从下口放出,上层液体从上口倒出;
(6)若从118℃便开始收集馏分此时的蒸气中含有醋酸和正丁醇,会收集到少量未反应的冰醋酸和正丁醇,导致获得的乙酸正丁酯质量偏大;
(7)先根据酸的量计算理论上酯的量,再根据水的量计算酯的量,实际上酯的量与理论值之比即为酯的产率.
解答 解:(1)为提高冷凝效果,水应从下口进上口出,
故答案为:a;
(2)酯化反应的本质为酸脱羟基,醇脱氢,乙酸与丁醇在浓硫酸作用下加热发生酯化反应生成乙酸丁酯和水,该反应为可逆反应,化学方程式为:CH3COOH+CH3CH2CH2CH2OH$?_{△}^{浓硫酸}$CH3COOCH2CH2CH2CH3+H2O,
故答案为:CH3COOH+CH3CH2CH2CH2OH$?_{△}^{浓硫酸}$CH3COOCH2CH2CH2CH3+H2O;
(3)减少生成物的浓度,平衡向正反应方向移动,使用分水器分离出水,有利于平衡向正反应方向移动,提高反应产率,
故答案为:使用分水器分离出水,使平衡正向移动,提高反应产率;
(4)制备乙酸丁酯时常用饱和碳酸钠溶液,目的是中和挥发出来的乙酸,使之转化为乙酸钠溶于水中,便于闻乙酸丁酯的香味,溶解挥发出来的乙醇;降低乙酸丁酯在水中的溶解度,便于分层得到酯,
故答案为:除去产品中含有的乙酸等杂质;
(5)分液操作时,使用的漏斗是分液漏斗,分液漏斗中下层液体从下口放出,上层液体从上口倒出,以免两种液体相互污染,
故答案为:C;
(6)若从118℃便开始收集馏分此时的蒸气中含有醋酸和正丁醇,会收集到少量未反应的冰醋酸和正丁醇,因此会导致产率偏高,
故答案为:高;会收集到少量未反应的冰醋酸和正丁醇;
(7)正丁醇的质量=0.8 g/mL×18.5mL=14.8g;冰醋酸的质量=1.045g/mL×13.4mL=14.003g;
理论上14.8g正丁醇完全反应生成酯的质量为xg,需乙酸的质量是yg,
乙酸和正丁醇的反应方程式为
60g 74g 116g 18g
yg 14.8g xg
所以x=23.2 y=12g<14.003g,
所以乙酸过量,乙酸正丁酯的产率=$\frac{15.1g}{23.2g}$×100%≈65%.
故答案为:65%.
点评 本题制备方案的设计,题目难度中等,明确乙酸乙酯的制备原理以及运用原理理解实验装置是解答的关键,注意掌握制备方案设计与评价的原则,试题充分培养了学生的分析、理解能力及灵活应用所学知识的能力.


 优学名师名题系列答案
优学名师名题系列答案科目:高中化学 来源: 题型:解答题

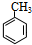 +Br2$\stackrel{光照}{→}$
+Br2$\stackrel{光照}{→}$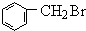 +HBr
+HBr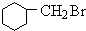 +NaOH$→_{△}^{醇}$
+NaOH$→_{△}^{醇}$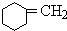 +NaBr+H2O
+NaBr+H2O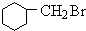 +NaOH$→_{△}^{水}$
+NaOH$→_{△}^{水}$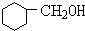 +NaBr.
+NaBr.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | OH-中含有9个质子,9个电子 | |
| B. | Na的原子半径比Cl的大,但Na+的半径比Cl-的小 | |
| C. | 与某非金属反应时甲原子失电子数目比乙的多,说明甲的金属性比乙强 | |
| D. | Na2O 和Na2O2中所含的化学键类型完全相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
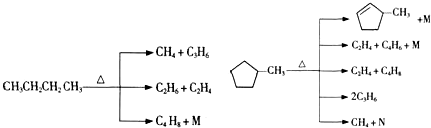
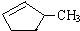 的说法正确的是A.
的说法正确的是A.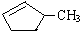 和
和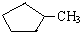
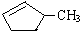 和
和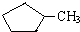 完全燃烧时的耗氧量相同
完全燃烧时的耗氧量相同 可与水以任意比互溶
可与水以任意比互溶查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 5.6g | B. | 2.8g | C. | 11.2g | D. | 1.4g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 6种 | B. | 10种 | C. | 12种 | D. | 14种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验操作 | 现象 | 结论 |
| A | 向滴有酚酞的氢氧化钠溶液中通入过量氯化氢气体 | 溶液红色消失 | 氯化氢具有漂白性 |
| B | 向某溶液中滴加几滴KSCN溶液 | 无明显现象 | 溶液中不含Fe3+和Fe2+ |
| C | 向蛋白质溶液中加入硫酸铵溶液 | 有固体析出 | 蛋白质变性 |
| D | 将铜片放入浓硝酸中 | 产生红棕色气体,溶液变为蓝色 | 体现浓硝酸的酸性和强氧化性 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na放入水中,产生气体:2Na+2H2O═2Na++2OH-+H2↑ | |
| B. | 液氨作为清洁能源的反应原理是:4NH3+5O2$\frac{\underline{\;催化剂\;}}{△}$4NO+6H2O | |
| C. | NaOH溶液不能保存在玻璃塞的试剂瓶中:SiO2+2OH-═SiO32-+H2O | |
| D. | 红热的铁丝与水蒸汽接触,表面形成蓝黑色(或黑色)保护层:3Fe+4H2O(气)$\frac{\underline{\;\;△\;\;}}{\;}$Fe3O4+4H2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com