
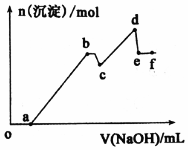
 ��֪25��ʱ��Ksp[Mg��OH��2]=5.61��l0-12��Ksp[Al��OH��3]=1.3��l0-33��Al��OH��3?AlO2-+H++H2O Ka=6.31��l0-13��ij��Һ�п��ܺ��� H+��Na+��Mg2+��Al3+��Cl-��HCO3-�����ӣ������Һ�м���һ�����ʵ���Ũ�ȵ�NaOH��Һʱ���������ɳ��������ʵ�����NaOH��Һ������仯��ͼ��ʾ�������й�˵����ȷ���ǣ�������
��֪25��ʱ��Ksp[Mg��OH��2]=5.61��l0-12��Ksp[Al��OH��3]=1.3��l0-33��Al��OH��3?AlO2-+H++H2O Ka=6.31��l0-13��ij��Һ�п��ܺ��� H+��Na+��Mg2+��Al3+��Cl-��HCO3-�����ӣ������Һ�м���һ�����ʵ���Ũ�ȵ�NaOH��Һʱ���������ɳ��������ʵ�����NaOH��Һ������仯��ͼ��ʾ�������й�˵����ȷ���ǣ�������| A�� | b �����-Al��OH��3��d �����-A1��OH��3��Mg��OH��2��e������-NaA1O2 | |
| B�� | �������⣬��NaOH������ȫ����Mg2+��Al3+���� | |
| C�� | cd �η����ķ�ӦΪ��Mg2++2OH-=Mg��OH��2�� | |
| D�� | bc �η����ķ�ӦΪ��Al��OH��3+OH-=A1O2-+2H2O |
���� �����OH-�ֱ���H+-��HCO3-��Al3+��Mg2+��Ӧ��������OH-�ܽ�Al��OH��3��������0-a��û�����ɳ�����˵����Һ��һ�����������ӻ�̼��������ӣ����ں����г������ɼ����ֳ����ܽ��֪��һ�����������ӣ���һ��������̼��������ӣ�һ�����������ӣ�����Mg��OH��2��Al��OH��3���ܶȻ�������֪��a-b�Σ�����Al��OH��3������b-c�Σ����������ܽ⣬c-d �Σ�Mg��OH��2�����ɵ����ʵ�������Al��OH��3�ļ��ٵ����ʵ�����d-e�Σ�������þ������ȫ���������������ܽ⣬e������ΪNaCl��NaA1O2��
f��ΪMg��OH��2��
A�����ʵ��ܶȻ�ԽС��Խ���γɳ�����e������ΪNaCl��NaA1O2��
B��NaOH������ȫ����Mg2+��Al3+���ӣ�
C��cd �η��������������ܽ��Լ�������þ�����ɣ�
D��b-c�Σ����������ܽ⣮
��� �⣺A����0-a��û�����ɳ�����˵����Һ��һ�����������ӻ�̼��������ӣ����ں����г������ɼ����ֳ����ܽ��֪��һ�����������ӣ���һ��������̼��������ӣ�һ�����������ӣ�����Mg��OH��2��Al��OH��3���ܶȻ�������֪�������Һ�м���һ�����ʵ���Ũ�ȵ�NaOH��Һʱ��������Al��OH��3�ij�����a-b�Σ�����Al��OH��3������b �����-Al��OH��3��b-c�Σ����������ܽ⣬c-d �Σ�Mg��OH��2�����ɵ����ʵ�������Al��OH��3�ļ��ٵ����ʵ�����d �����-A1��OH��3��Mg��OH��2��d-e�Σ�������þ������ȫ���������������ܽ⣬e������ΪNaCl��NaA1O2����A����
B��Ksp[Mg��OH��2]=5.61��l0-12��Ksp[Al��OH��3]=1.3��l0-33��Al��OH��3?AlO2-+H++H2O Ka=6.31��l0-13��Mg��OH��2�ܶȻ�������d-e�Σ�������þ������ȫ���������������ܽ⣬��NaOH����ȫ����Mg2+��Al3+���ӣ���B����
C��c-d �Σ�Mg��OH��2�����ɵ����ʵ�������Al��OH��3�ļ��ٵ����ʵ��������������������ܽ��Լ�������þ�����ɣ���C����
D��b-c�Σ����������ܽ�Al��OH��3+OH-=A1O2-+2H2O����D��ȷ��
��ѡD��
���� ���⿼�������Ӽ���ķ���Ӧ�ã���Ŀ�Ѷ��еȣ���������������������������ǿ�����ͼ���з��������ӷ�Ӧ����Ӧ���Ⱥ�˳���ǽ���ؼ��������ѵ�������θ���ͼ���е������жϺ������ӵĴ��ڣ�


 ����������������ϵ�д�
����������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | SO2��CO��CO2�������������� | B�� | BaSO4��Ca��OH��2��KNO3��Һ���ǵ���� | ||
| C�� | ����ռ��ʯ�Ҷ��Ǽ� | D�� | ϡ������ţ�̡�������Һ���ǽ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����ѹǿ���÷�Ӧ�����淴Ӧ���ʿ��ܲ��� | |
| B�� | �����¶ȣ�����Ӧ���ʱ��淴Ӧ���ʼ�С�ij̶�С | |
| C�� | ��������������������ƽ�������ƶ���ƽ�ⳣ��Kֵ���� | |
| D�� | ����������ʵ�������0.5 molʱ�ﵽƽ�⣬��������·�Ӧ�ų�0.5 Q KJ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
| ����� | �������Լ� | ���뷽�� |
| �ٱ������ӣ� | ||
| ���������������ᣩ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| �¶ȣ��棩 | 20 | 30 | 40 | 50 | 60 | 70 | 80 |
| CaO2ƽ���������ʣ���10-3mol��s-1�� | 7.5 | 8.2 | 9.4 | 8.0 | 7.1 | 6.7 | 5.5 |
| t/min | 0 | 10 | 20 | 30 | 40 |
| �գ�CO�� | 0.250 | 0.235 | 0.225 | 0.200 | 0.200 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | c��NH4+����c��NO3-����c��H+����c��OH-�� | B�� | c��NO3-����c��NH4+����c��H+����c��OH-�� | ||
| C�� | c��H+����c��NH4+����c��NO3-����c��OH-�� | D�� | c��OH-����c��NO3-����c��NH4+����c��H+�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
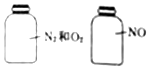
| A�� | Ħ��������� | B�� | �����ܶ���� | C�� | ����������� | D�� | ������������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | KC1 | B�� | SiO2 | C�� | SO3 | D�� | NaOH |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com