
分析 (1)若W和焦炭在高温下发生反应,所制得的半导体材料应用广泛,则W为SiO2;
(2)若取两支试管分别加入少量W溶液,往一支试管中滴入KSCN溶液,无明显现象,则W不含Fe3+,往另一支试管中加入足量氯水,再加入适量CCl4,振荡,静置,下层溶液呈紫红色,说明W含有I-,往上层溶液中滴入KSCN溶液,溶液呈红色,则W含有Fe2+,故W为FeI2;
(3)若W是大气主要污染物之一,也是空气质量预报必报的气体.可用酸性高锰酸钾溶液检验该污染物是二氧化硫气体;
①二氧化硫与高锰酸钾发生氧化还原反应生成硫酸根离子和锰离子,反应的离子方程式为:5 SO2+2 MnO4-+2 H2O=2 Mn2++4 H++5 SO42-;
②由反应5 SO2+2 MnO4-+2 H2O=2 Mn2++4 H++5 SO42-可知5molW参加反应转移10mol电子,则1molW转移电子为2mol;
(4)若W是产生光化学烟雾主要气体之一,其溶于水能生成一种一元强酸,所以W是二氧化氮气体,
①二氧化氮与水的反应生成一氧化氮和硝酸,化学方程式为:3NO2+H2O=2HNO3+NO;
②二氧化氮与氢氧化钠溶液反应生成硝酸钠和亚硝酸钠,反应的离子方程式为:2NO2+2OH-=NO3-+NO2-+H2O.
解答 解:(1)若W和焦炭在高温下发生反应,所制得的半导体材料应用广泛,则W为SiO2,该反应方程式为:2C+SiO2$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑,
故答案为:SiO2 ;2C+SiO2$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑;
(2)若取两支试管分别加入少量W溶液,往一支试管中滴入KSCN溶液,无明显现象,则W不含Fe3+,往另一支试管中加入足量氯水,再加入适量CCl4,振荡,静置,下层溶液呈紫红色,说明W含有I-,往上层溶液中滴入KSCN溶液,溶液呈红色,则W含有Fe2+,故W为FeI2.
①W溶液中所含金属阳离子为:Fe2+,故答案为:Fe2+;
②W(FeI2)与足量氯水反应的离子方程式为:2Fe2++4I-+3Cl2=2Fe3++I2+6Cl-,
故答案为:2Fe2++4I-+3Cl2=2Fe3++I2+6Cl-;
(3)①二氧化硫与高锰酸钾发生氧化还原反应生成硫酸根离子和锰离子,反应的离子方程式为:5 SO2+2 MnO4-+2 H2O=2 Mn2++4 H++5 SO42-,故答案为:5 SO2+2 MnO4-+2 H2O=2 Mn2++4 H++5 SO42-;
②由反应5 SO2+2 MnO4-+2 H2O=2 Mn2++4 H++5 SO42-可知5molW参加反应转移10mol电子,则1molW转移电子为2mol,故答案为:2;
(4)①二氧化氮与水的反应生成一氧化氮和硝酸,化学方程式为:3NO2+H2O=2HNO3+NO,故答案为:3NO2+H2O=2HNO3+NO;
②二氧化氮与氢氧化钠溶液反应生成硝酸钠和亚硝酸钠,反应的离子方程式为:2NO2+2OH-=NO3-+NO2-+H2O.
点评 本题考查无机物推断、物质性质等,侧重考查特殊组成物质的性质,属于并列型题目,需要学生熟练掌握元素化合物性质,难度中等.


 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 根据维生素的溶解性可以将维生素分为脂溶性和水溶性两大类 | |
| B. | 人体需要的维生素都必须从食物中摄取 | |
| C. | 维生素C具有较强的还原能力,容易被还原 | |
| D. | 维生素的作用是维持细胞的正常功能、调节人体新陈代谢 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
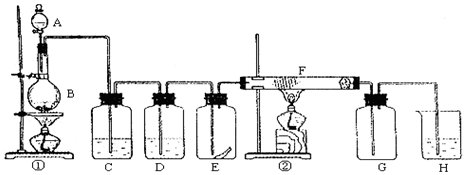
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 编号 | 实验 | 操作 |
| A | 实验室用自来水制备蒸馏水 | 将自来水倒入烧杯中,小心给烧杯加热 |
| B | 配制一定浓度的氯化钾溶液100mL | 将称好的氯化钾固体放入100mL容量瓶中,加水溶解,振荡摇匀,定容 |
| C | 检验溶液中是否含SO42- | 先加入稀盐酸,无明显现象,再加入BaCl2溶液 |
| D | 取出分液漏斗中的上层液体 | 下层液体从分液漏斗下端管口放出,关闭活塞,换一个接收容器,上层液体继续从分液漏斗下端管口放出 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 适量盐酸 | B. | 适量NaOH | C. | 适量NaHCO3 | D. | 适量KOH |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,11.2LH2O 含有的分子数为0.5NA | |
| B. | 在常温常压下,11.2LCl2含有的分子数为0.5NA | |
| C. | 含有NA个氩原子的氩气在标准状况下的体积约为11.2L | |
| D. | 25℃,1.01×105 Pa,64gSO2中含有的原子数为3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 分子中处于四面体中心位置的碳原子数为a,一定在同一直线上的碳原子个数为b,一定在同一平面上的碳原子数为c.则a、b、c分别为( )
分子中处于四面体中心位置的碳原子数为a,一定在同一直线上的碳原子个数为b,一定在同一平面上的碳原子数为c.则a、b、c分别为( )| A. | 4、4、7 | B. | 4、3、6 | C. | 3、5、4 | D. | 2、6、4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com