
| A. | 仅用氨水即可鉴别NaCl、AlBr3、FeI2、AgNO3四种溶液 | |
| B. | 用燃烧法鉴别环己醇、苯和四氯化碳 | |
| C. | 用烧碱溶液鉴别地沟油、甘油和石油 | |
| D. | 用新制氯水鉴别碘的淀粉溶液、含石蕊的烧碱溶液、硫酸铜溶液等三种蓝色溶液 |
分析 A.氨水与NaCl不反应,与AlBr3反应生成白色沉淀,与FeI2反应生成的白色沉淀迅速变为灰绿色最后变为红褐色,与AgNO3反应先生成沉淀后沉淀消失;
B.环己醇燃烧有淡蓝色火焰,苯燃烧冒黑烟,四氯化碳不能燃烧;
C.地沟油与NaOH发生水解反应后油状液体消失、甘油与NaOH混合不分层,石油与NaOH混合分层;
D.氯水中含HClO,具有漂白性,碘的淀粉溶液、含石蕊的烧碱溶液最后均为无色.
解答 解:A.氨水与NaCl不反应,与AlBr3反应生成白色沉淀,与FeI2反应生成的白色沉淀迅速变为灰绿色最后变为红褐色,与AgNO3反应先生成沉淀后沉淀消失,反应现象不同,可鉴别,故A正确;
B.环己醇燃烧有淡蓝色火焰,苯燃烧冒黑烟,四氯化碳不能燃烧,燃烧现象不同,可鉴别,故B正确;
C.地沟油与NaOH发生水解反应后油状液体消失、甘油与NaOH混合不分层,石油与NaOH混合分层,反应现象不同,可鉴别,故C正确;
D.氯水中含HClO,具有漂白性,碘的淀粉溶液、含石蕊的烧碱溶液最后均为无色,则不能鉴别碘的淀粉溶液、含石蕊的烧碱溶液,故D错误;
故选D.
点评 本题考查物质检验实验方案的设计,为高频考点,把握物质的性质、发生的反应及现象为解答的关键,侧重元素化合物知识综合应用及实验能力的考查,题目难度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | 1moL苯乙烯(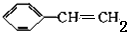 )中含有的碳酸双键数为4NA )中含有的碳酸双键数为4NA | |
| B. | 加热条件下,4.6g金属Na与足量O2反应的产物中阴离子的数目为0.1NA | |
| C. | 室温条件下,pH=9,体积为1L的CH4COONa溶液中,发生电离的水分子数为1.0×10-4NA | |
| D. | 高温条件下,16.6g铁粉与足量水蒸气反应后,转移电子数为0.9NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苹果放在空气中久置变黄和纸张久置变黄原理相似 | |
| B. | 用活性炭为蔗糖脱色和用臭氧漂白纸浆,原理相似 | |
| C. | 钢铁制品和铜制品既能发生吸氧腐蚀又能发生析氢腐蚀 | |
| D. | 黄河入海口沙洲的形成与用卤水点豆腐,都体现了胶体聚沉的性质 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 酯化反应的产物只有酯 | |
| B. | 酯化反应一般需要用NaOH溶液来吸收生成的酯 | |
| C. | 酯化反应是有限度的 | |
| D. | 浓硫酸可做酯化反应的催化剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙醇、糖类和蛋白质都是人体必需的营养物质 | |
| B. | 石油是混合物,其分馏产品汽油也是混合物 | |
| C. | “海水淡化”可以解决“淡水供应危机”,加入明矾可以使海水淡化 | |
| D. | 陶瓷、水晶、水泥、玻璃都属于硅酸盐 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
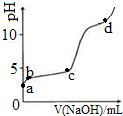 室温下,在0.2mol/LAl2(SO4)3溶液中,逐滴加入1.0mol/LNaOH溶液,实验测得溶液pH随NaOH溶液体积变化曲线如图,下列说法正确的是( )
室温下,在0.2mol/LAl2(SO4)3溶液中,逐滴加入1.0mol/LNaOH溶液,实验测得溶液pH随NaOH溶液体积变化曲线如图,下列说法正确的是( )| A. | a点,离子方程式为:Al3++3OH-→Al(OH)3↓ | |
| B. | a~b段,溶液pH增大,促进了氢氧化铝的碱式电离 | |
| C. | b~c段,加入的OH-主要用于生成Al(OH)3沉淀 | |
| D. | d点时,Al(OH)3沉淀开始溶解 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 58 g乙烯和乙烷的混合气体中碳原子数目一定为4NA | |
| B. | 用惰性电极电解CuSO4溶液后,如果加入0.1mol Cu(OH)2能使溶液复原,则电路中转移电子的数目为0.2NA | |
| C. | 142g Na2SO4和Na2HPO4固体混合物中,阴阳离子总数为3NA | |
| D. | 已知3BrF3+5H2O=HBrO3+Br2+9HF+O2↑ 如果有5mol H2O参加氧化还原反应,则由水还原的BrF3分子数目为3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
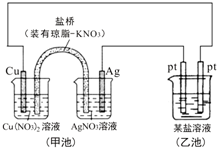
| A. | 图中甲池为原电池装置,Cu电极发生还原反应 | |
| B. | 实验过程中,甲池左侧烧杯中NO3-的浓度不变 | |
| C. | 若甲池中Ag电极质量增加5.4g时,乙池某电极析出1.6g金属,则乙中的某盐溶液可能是AgNO3溶液 | |
| D. | 若用铜制U形物代替“盐桥”,工作一段时间后取出U形物称量,质量会减小 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com