
| A. | >40% | B. | <40% | C. | =40% | D. | 无法确定 |
分析 设体积分别为VmL,30%的H2SO4溶液密度为ρ1,50%的H2SO4溶液密度为ρ2,表示出混合后溶液中溶质质量分数,硫酸的浓度越大密度越大,结合表达式判断质量分数关系.
解答 解:如果等体积混合,设体积分别为VmL,30%的H2SO4溶液密度为ρ1,50%的H2SO4溶液密度为ρ2,则混合后溶液的质量分数为w(H2SO4)=$\frac{V{ρ}_{1×}30%+V{ρ}_{2}×50%}{V{ρ}_{1}+V{ρ}_{2}}$=30%+20%×$\frac{{ρ}_{2}}{{ρ}_{1+}{ρ}_{2}}$,因H2SO4的浓度越大,密度越大,则ρ1<ρ2,则$\frac{{ρ}_{2}}{{ρ}_{1}+{ρ}_{2}}$>$\frac{1}{2}$,故30%+20%×$\frac{{ρ}_{2}}{{ρ}_{1}+{ρ}_{2}}$>40%,故选A.
点评 本题考查有关溶质质量分数计算,难度不大,注意对公式的理解与应用,注意硫酸的浓度越大密度越大.


科目:高中化学 来源: 题型:选择题
| A. | 甲烷与氯气的混合气体在光照下反应,生成的是一氯甲烷与氯化氢 | |
| B. | 向盛有乙醇的烧杯中投入一小块金属钠,可以观察到钠块沉在乙醇液面下面 | |
| C. | 氯仿能发生水解反应和消去反应 | |
| D. | 乙烯可作水果催熟剂,无水乙醇直接用作医疗消毒剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
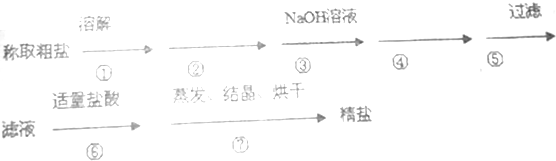
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向某溶液中加入BaCl2溶液,产生白色沉淀,加入HNO3后,白色沉淀不溶解,也无其他现象,说明原溶液中一定含有SO42- | |
| B. | 取少量久置的Na2SO3样品于试管中加水溶解,再加足量盐酸酸化,然后加BaCl2溶液,若加HCl时有气体产生,加BaCl2时有白色沉淀产生,说明Na2SO3样品已部分被氧化 | |
| C. | 向某溶液中加盐酸产生无色气体,该气体能使澄清的石灰水变浑浊,说明该溶液中一定含有CO32-或SO32- | |
| D. | 将某气体通入品红溶液中,品红溶液褪色,该气体一定是SO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 非金属元素组成的化合物中只可能含有共价键 | |
| B. | VIIA族元素气态氢化物的热稳定性从上到下依次减弱 | |
| C. | 第二周期元素原子的半径从左到右依次增大 | |
| D. | 第三周期非金属元素含氧酸的酸性从左到右依次增强 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
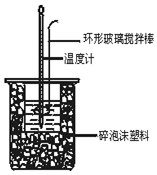 Ⅰ、已知 KI溶液在酸性条件下能与氧气反应. 现有以下实验记录:
Ⅰ、已知 KI溶液在酸性条件下能与氧气反应. 现有以下实验记录:| 实验编号 | ① | ② | ③ | ④ | ⑤ |
| 温度(℃) | 30 | 40 | 50 | 60 | 70 |
| 显色时间(s) | 160 | 80 | 40 | 20 | 10 |
| 实验序号 | 起始温度t1/℃ | 终止温度t2/℃ | |
| 盐酸 | 氢氧化钠 | 混合溶液 | |
| 1 | 20.0 | 20.1 | 23.2 |
| 2 | 20.2 | 20.4 | 23.4 |
| 3 | 20.5 | 20.6 | 23.6 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 开始加入合金的质量可能为5.6g | |
| B. | 参加反应的硝酸的物质的量为0.2mol | |
| C. | 沉淀完全时消耗NaOH溶液的体积为200mL | |
| D. | 标况下产物NO体积为4.48L |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com