
某固体混合物可能由Al、(NH4)2SO4、MgCl2、AlCl3、FeCl2中的一种或几种组成,现对该混合物做如下实验,所得现象和有关数据如图所示(气体体积数据已换算成标准状况下的体积):
回答下列问题:(1)混合物中是否存在FeCl2:____________(填“是”或“否”)。
(2)混合物中是否存在(NH4)2SO4:____________(填“是”或“否”)。
(3)写出反应⑤的离子方程式:________________________。
(4)请根据图中数据分析,原固体混合物的成分为 (写化学式)
(1)否;(2)是;(3)Al(OH)3 + 3H+=Al3+ + 3H2O(4)Al、(NH4)2SO4和MgCl2
解析试题分析:根据题给流程图分析知,28.1g固体在浓氢氧化钠溶液加热的条件下,生成标准状况下11.2L气体(物质的量为0.5mol),气体通过碱石灰体积不变(无酸性气体),通过浓硫酸体积减小,说明剩余的6.72 L气体(物质的量为0.3mol)为氢气,即原固体中一定含有金属Al,根据方程式2Al+2NaOH+2H2O=2NaAlO2+3H2↑计算得,铝的物质的量为0.2mol,质量为5.4 g;生成氨气的物质的量为0.2 mol,则原固体中一定含有 0.1 mol (NH4)2SO4,其质量为13.2 g;得到白色沉淀久置不变色,说明无FeCl2(氢氧化亚铁易被氧化为红棕色的氢氧化铁),因为NaOH过量,所以白色沉淀不可能含有氢氧化铝,则说明5.8 g白色沉淀为Mg(OH)2,为0.1 mol,则固体中MgCl2为0.1 mol,质量为9.5g,无色溶液中有Al与过量NaOH溶液反应后得到的NaAlO2。(1)白色沉淀久置不变色,说明无FeCl2(氢氧化亚铁易被氧化为红棕色的氢氧化铁),答案为:否;(2)气体通过浓硫酸后,体积减少4.48 L,说明气体中有NH3,则原固体中一定含有(NH4)2SO4,(3)反应⑤为氢氧化铝与盐酸反应,方程式为Al(OH)3 + 3H+=Al3+ + 3H2O;(4)由以上分析可知原固体中一定含有金属Al,其质量为5.4 g,一定含有 0.1 mol (NH4)2SO4,其质量为13.2 g,固体中MgCl2为0.1 mol,质量为9.5g,三种物质的质量之和刚好等于28.1g,所以一定没有AlCl3,原固体中一定含有Al、(NH4)2SO4和MgCl2三种物质。
考点:考查物质的分离、提纯以及检验。


科目:高中化学 来源: 题型:单选题
向100mL18mol/L的硫酸中加入足量铜片,加热并充分反应。下列有关说法正确的是
| A.充分反应后转移1.8mol电子 | B.H2SO4只作氧化剂 |
| C.若不加热应生成H2 | D.消耗的铜的质量一定少于57.6g |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
印刷电路的废腐蚀液中含有大量CuCl2、FeCl2和FeCl3,任意排放将导致环境污染及资源的浪费,可从该废液中回收铜,并将铁的化合物全部转化为FeCl3溶液,作为腐蚀液原料循环使用。
(1)测得某废腐蚀液中含CuCl2 1.5 mol·L-1、FeCl2 3.0 mol·L-1、FeCl3 1.0 mol·L-1、HCl 3.0 mol·L-1。
取废腐蚀液200 mL按如下流程在实验室进行实验: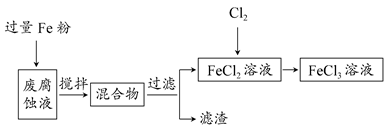
回答下列问题:
①废腐蚀液中加入过量铁粉后,发生反应的离子方程式为________。
②检验废腐蚀液中含有Fe3+的实验操作是________;在上述流程中,“过滤”用到的玻璃仪器有烧杯、玻璃棒、________。
③由滤渣得到纯铜,除杂所需试剂是________。
(2)某化学兴趣小组利用下图所示装置制取氯气并通入到FeCl2溶液中获得FeCl3溶液。
①实验开始前,某同学对实验装置进行了气密性检查,方法是________。
②浓盐酸与二氧化锰加热反应的化学方程式为________;烧杯中NaOH溶液的作用是________。
③参考(1)中数据,按上述流程操作,需称取Fe粉的质量应不少于________g,需通入Cl2的物质的量应不少于________ mol。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
如图所示,将甲、乙两个装有不同物质的针筒用导管连接起来,将乙针筒内的物质压到甲针筒内,进行下表所列的不同实验(气体在同温同压下测定)。试回答下列问题: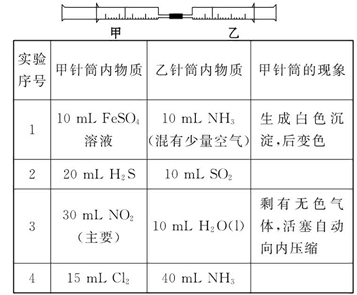
(1)实验1中,沉淀最终变为_______色,写出沉淀变色的化学方程式_____________________。
(2)实验2甲针筒内的现象是:有_______生成,甲筒活塞_______移动(填“向外”、“向内”或“不”)。反应后甲针筒内有少量的残留气体,正确的处理方法是将其通入_______溶液中。
(3)实验3中,甲中的30 mL气体是NO2和N2O4的混合气体,那么甲中最后剩余的无色气体是_______,写出NO2与H2O反应的化学方程式____________________________。
(4)实验4中,已知:3Cl2+2NH3=N2+6HCl。甲针筒除活塞有移动,针筒内有白烟产生外,气体的颜色变化为_______。最后针筒内剩余气体的体积约为_______mL。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
X、Y、Z、Q、R是五种短周期元素,原子序数依次增大。X、Y两元素最高正价与最低负价之和均为0;Q与X同主族;Z、R分别是地壳中含量最高的非金属元素和金属元素。
请回答下列问题:
(1)五种元素原子半径由大到小的顺序是(写元素符号)____________________。
(2)X与Y能形成多种化合物,其中既含极性键又含非极性键,且相对分子质量最小的物质是(写分子式)________________。
(3)由以上某些元素组成的化合物A、B、C、D有如下转化关系:A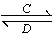 B(在水溶液中进行)
B(在水溶液中进行)
其中,C是溶于水显酸性的气体;D是淡黄色固体。
写出C的结构式:________;D的电子式:________。
①如果A、B均由三种元素组成,B为两性不溶物,则A的化学式为________________________;由A转化为B的离子方程式为___________________。
②如果A由三种元素组成,B由四种元素组成,A、B溶液均显碱性。用离子方程式表示A溶液显碱性的原因:
________________________________________________________________________。
A、B浓度均为0.1 mol·L-1的混合溶液中,离子浓度由大到小的顺序是____________________;常温下,在该溶液中滴加稀盐酸至中性时,溶质的主要成分有________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(6分)某些化学反应可用表示(未配平):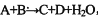 ;请回答下列问题:
;请回答下列问题:
(1)若A、C、D均含有氯元素,且A中氯元素的化合价介于C与D之间,写出该反应的离子方程式:_________________________________________________。
(2)若A为紫红色金属,D为无色刺激性气体,请写出符合上式的化学方程式:______________________________________________________________。
(3)若C、D均为气体(其中C有颜色)且分子具有相同的原子个数比,则符合上式化学方程式是:_____________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
用下图所示装置进行实验(夹持装置已略去)。请回答下列问题: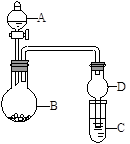
(1)若A中为浓硝酸,B中为铜单质,C中为氢氧化钠溶液。现将浓硝酸滴入B中,则B中发生反应的化学方程式为 。
(2)若A中为浓氨水,B中为生石灰,C中为明矾溶液。
①将浓氨水逐滴滴入B中,可产生大量氨气,原因可能是 _ (填序号)。
a.生石灰和浓氨水反应产生氨气,氨气易溶于水
b.生石灰和水反应,消耗水,使氨气的溶解量减少
c.反应放出大量热,使氨气在水中溶解度明显降低
② C中通入过量氨气时,反应的离子方程式为 。
(3)若A中为水,B中为过氧化钠,C中为酸性淀粉碘化钾溶液,将水滴入B中后,B中的实验现象为 ;若C中溶液变为蓝色,则C中发生反应的离子方程式为_ 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
短周期元素A、B、C、D、E在元素周期表中的位置如下图所示,B是形成化合物种类最多的元素。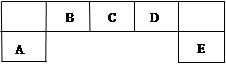
请回答下列问题:
(1)描述D在元素周期表中的位置:_____________________
(2)比较A、C、D元素简单离子半径的大小:______>______>______(填微粒符号)
(3)E的氢化物与其最高价氧化物的水化物的钾盐共热能发生反应,生成一种气体单质,反应的化学反应方程式为_______________________________________________.
(4)F与D同主族且相邻,请说出D的氢化物比F的氢化物稳定的根本原因:______________;
用高能射线照射液态水时,一个水分子能释放出一个电子,同时产生一种具有较强的氧化性的阳离子,试写出阳离子的电子式:________,写出该阳离子与F氢化物的水溶液反应的离子方程式:__________________________________________________________。
(5)在Fe和Cu 的混合物中加入一定量的C的最高价氧化物的水化物稀溶液,充分反应后剩余金属m1g,再向其中加入一定量的稀硫酸,充分反应后,剩余金属m2g。下列说法正确的是( )
A.加入稀硫酸前,加入稀硫酸后的溶液中肯定都有Cu2+
B.加入稀硫酸前,加入稀硫酸后的溶液中肯定都有Fe2+
C.m1一定大于m2
D.剩余固体m1g中一定有单质铜,剩余固体m2g中一定没有单质铜
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列说法正确的是( )
| A.酸雨样品露天放置一段时间,酸性增强,是由于雨水所含成分被氧化的原因 |
| B.CH4、NH3、PH3的热稳定性逐渐增强 |
| C.因为酸性:HC1>HF,所以非金属性:Cl>F |
| D.钠原子在反应中失去的电子比铝原子少,故钠的金属性比铝弱 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com