
【题目】从海水中提取试剂级NaCl及回收金属Mg的工业流程如图:
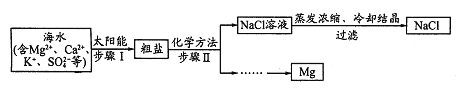
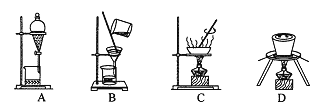
![]() 步骤I原理如图,在实验室中完成该步骤所用装置为 ______
步骤I原理如图,在实验室中完成该步骤所用装置为 ______ ![]() 填序号
填序号![]() 。
。
![]() 某学习小组设计了实验模拟步骤Ⅱ:
某学习小组设计了实验模拟步骤Ⅱ:
粗盐溶解![]() 过滤
过滤![]() NaCl溶液
NaCl溶液
![]() 该实验中加入
该实验中加入![]() 的作用是 ______ ;若向粗盐溶液中加入的是
的作用是 ______ ;若向粗盐溶液中加入的是![]() 浓溶液,则有难溶的
浓溶液,则有难溶的![]() 生成,同时有气体逸出.该反应的离子方程式为 ______。
生成,同时有气体逸出.该反应的离子方程式为 ______。
![]() 学习小组发现上述实验即使
学习小组发现上述实验即使![]() 用量不足,第
用量不足,第![]() 步沉淀中依然含有少量
步沉淀中依然含有少量![]() ,试从平衡角度分析 ______。
,试从平衡角度分析 ______。
![]() 在第
在第![]() 步后增加过滤,并从滤渣中得到
步后增加过滤,并从滤渣中得到![]() ,工业上通过电解获得Mg的化学方程式为 ______ ; 若
,工业上通过电解获得Mg的化学方程式为 ______ ; 若![]() 时直接将
时直接将![]() 熔融,然后用惰性电极电解,发现有固体剩余,则该固体可能是 ______
熔融,然后用惰性电极电解,发现有固体剩余,则该固体可能是 ______ ![]() 写化学式
写化学式![]() ;现有a g滤渣,用上二述方法处理回收Mg时产生标况下
;现有a g滤渣,用上二述方法处理回收Mg时产生标况下![]() ,剩余固体为c g。则滤渣中镁元素的质量分数为
,剩余固体为c g。则滤渣中镁元素的质量分数为 ![]() 不必化简
不必化简![]() 。
。
【答案】C 除去钙离子、钡离子 ![]() 加入
加入![]() 使
使![]() 的溶解平衡向溶解方向移动,从而形成
的溶解平衡向溶解方向移动,从而形成![]()
![]() 熔融
熔融 MgO
MgO 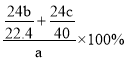
【解析】
由分离流程可知,步骤I利用太阳能进行海水晒盐,与蒸发原理相同,步骤Ⅱ为粗盐溶解![]() 过滤
过滤![]() 溶液,
溶液,![]() 除去硫酸根离子,
除去硫酸根离子,![]() 除去镁离子,
除去镁离子,![]() 除去钙离子及过量的钡离子,最后加盐酸可除去过量的碳酸钠,注意除杂试剂均过量,以此来解答。
除去钙离子及过量的钡离子,最后加盐酸可除去过量的碳酸钠,注意除杂试剂均过量,以此来解答。
(1)步骤I原理为蒸发,在实验室中完成该步骤所用装置为图2中![]() 蒸发
蒸发![]() ;
;
(2)①该实验中加入![]() 的作用是除去钙离子、钡离子;若向粗盐溶液中加入的是
的作用是除去钙离子、钡离子;若向粗盐溶液中加入的是![]() 浓溶液,则有难溶的
浓溶液,则有难溶的![]() 生成,同时有气体逸出,气体为
生成,同时有气体逸出,气体为![]() ,该反应的离子方程式为
,该反应的离子方程式为![]() ;
;
②第③步沉淀中依然含有少量![]() ,是因为加入
,是因为加入![]() 使
使![]() 的溶解平衡向溶解方向移动,从而形成
的溶解平衡向溶解方向移动,从而形成![]() ;
;
![]() 为活泼金属,则工业上通过电解获得Mg的化学方程式为
为活泼金属,则工业上通过电解获得Mg的化学方程式为![]() (熔融)
(熔融)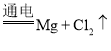 ,
,![]() 时直接将
时直接将![]() 熔融,水解生成
熔融,水解生成![]() ,然后分解生成固体MgO;滤渣中含
,然后分解生成固体MgO;滤渣中含![]() ,产生标况下
,产生标况下![]() b L,由
b L,由![]() (熔融)
(熔融)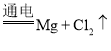 可知含Mg为
可知含Mg为![]() ,剩余固体为c g为MgO的质量,则含Mg为
,剩余固体为c g为MgO的质量,则含Mg为![]() ,则滤渣中镁元素的质量分数为
,则滤渣中镁元素的质量分数为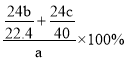 。
。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】秦皮是一种常用的中药,具有抗炎镇痛、抗肿瘤等作用。“秦皮素”是其含有的一种有效成分,结构简式如图所示,有关其性质叙述不正确的是( )

A.该有机物分子式为C10H8O5
B.分子中有四种官能团
C.该有机物能发生加成、氧化、取代等反应
D.1mol该化合物最多能与3molNaOH反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组探究苯和溴的取代反应,并制取少量溴苯。
已知:溴单质易挥发,微溶于水,易溶于四氯化碳等有机溶剂;溴苯密度为1.5 g·cm-3。
(1)甲同学用装置 I 进行实验,3~5 min 后观察到锥形瓶中有浅黄色沉淀,证明苯与溴发生了取代反应,该取代反应的化学方程式是_________________。

(2)乙同学观察到装置 I 烧瓶中有红棕色气体从导管中逸出,他认为甲同学的实验不严谨,设计装置Ⅱ进行实验(a 是防倒吸装置)。b 中试剂是____________(填字母)。
A.浓硫酸 B.氢氧化钠溶液 C.硝酸银溶液 D.四氯化碳
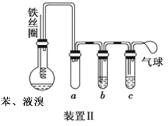
(3)将甲、乙两同学实验后制得的红褐色油状液体合并,进行提纯,步骤如下:
①用 NaOH 溶液多次洗涤有机层至无色,得粗溴苯。NaOH 溶液的作用是______________。
②向粗溴苯中加入无水氯化钙进行干燥,静置、过滤,得滤液。
③滤液中含有少量苯,经 _____________(填操作名称)得溴苯。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】![]() 环境科学
环境科学![]() 刊发了我国科研部门采用零价铁活化过硫酸钠
刊发了我国科研部门采用零价铁活化过硫酸钠![]() ,其中S为
,其中S为![]() 价
价![]() 去除废水中的正五价砷
去除废水中的正五价砷![]() 的研究成果,其反应机制模型如图所示。设阿伏加德罗常数的值为
的研究成果,其反应机制模型如图所示。设阿伏加德罗常数的值为![]() ,
,![]() 。下列叙述正确的是
。下列叙述正确的是![]()

A.![]() 过硫酸钠
过硫酸钠![]() 含
含![]() 个过氧键
个过氧键
B.若![]() 参加反应,共有
参加反应,共有![]() 个
个![]() 被还原
被还原
C.室温下,中间产物![]() 溶于水所得饱和溶液中
溶于水所得饱和溶液中![]() 为
为![]()
D.pH越小,越有利于去除废水中的正五价砷
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机化合物H的结构简式为![]() ,其合成路线如下(部分反应略去试剂和条件):
,其合成路线如下(部分反应略去试剂和条件):
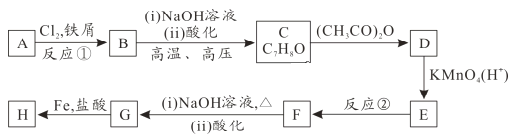
已知:①![]()
②![]() (苯胺易被氧化)
(苯胺易被氧化)
请回答下列问题:
(1)烃A的名称为_______,B中官能团为_______,H的分子式为_______,反应②的反应类型是_______。
(2)上述流程中设计C→D的目的是_______。
(3)写出D与足量NaOH溶液反应的化学方程式为_______。
(4)符合下列条件的D的同分异构体共有_______种。
A.属于芳香族化合物 B.既能发生银镜反应又能发生水解反应
写出其中核磁共振氢谱图中峰面积之比为6∶2∶1∶1的同分异构体的结构简式:______。(任写一种)
(5)已知:苯环上连有烷基时再引入一个取代基,常取代在烷基的邻对位,而当苯环上连有羧基时则取代在间位,据此按先后顺序写出以烃A为原料合成邻氨基苯甲酸(![]() )合成路线(无机试剂任选)。_______
)合成路线(无机试剂任选)。_______
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将4 mol A气体和2 mol B气体在2 L的容器中混合并在一定条件下发生如下反应:2A(气)+B(气)![]() 2C(气)。若经2 s(秒)后测得C的浓度为0.6 mol·L-1,现有下列几种说法:
2C(气)。若经2 s(秒)后测得C的浓度为0.6 mol·L-1,现有下列几种说法:
①用物质A表示的反应平均速率为0.3 mol·L-1·s-1
②用物质B表示的反应的平均速率为0.6 mol·L-1·s-1
③2s时物质A的转化率为70%
④2s时物质B的浓度为0.7 mol·L-1
其中正确的是:
A.①③B.①④C.②③D.③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在铜、锌、稀硫酸构成的原电池中(如图所示)
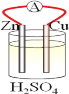
(1)负极是__________(填“铜”或“锌”),_________电子(填“失去”或“得到”),发__________(填“氧化”或 “还原”),电极反应方程式______________;
(2)电流由__________流向__________(填“铜”或“锌),铜片上观察到的现象是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Na2CO3与NaHCO3在生产、生活中用途非常广泛,同学们在实验室中探究Na2CO3和NaHCO3的性质。称取Na2CO3、NaHCO3固体各2g,分别加入两支大试管中,再各加10mL蒸馏水,充分溶解后,恢复至室温,各滴入2滴酚酞溶液,观察到如图所示现象。

(1)下列说法中,正确的是_____(填字母序号)。
a.两溶液中所含分子、离子种类完全相同
b.左侧试管中的现象解释了Na2CO3的俗名为什么叫做“纯碱”
c.向两支试管中加入过量硼酸饱和溶液,均有无色气体生成
(2)两溶液中的离子浓度都存在下式的数量关系,请你补充完整:c(Na+)+c(H+)=_____。
(3)NaHCO3溶液中存在下列两种变化趋势:
变化i.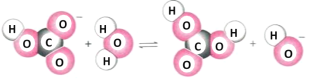
变化ii.(用离子方程式表示)_____。
溶液中滴加酚酞变为粉色,是因为以_____为主(填“变化i”或“变化ii”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】臭氧是理想的烟气脱硝剂,其脱硝反应为:2NO2(g)+O3(g)![]() N2O5(g)+O2(g),反应在恒容密闭容器中进行,下列由该反应相关图像作出的判断正确的是()
N2O5(g)+O2(g),反应在恒容密闭容器中进行,下列由该反应相关图像作出的判断正确的是()
A | B | C | D |
|
|
|
|
升高温度,正反应方向平衡常数减小 | 0~3s内,反应速率为:v(NO2)=0.2 mol·L-1·s-1 | t1时仅加入催化剂,平衡正向移动 | 达平衡时,仅改变x,则x为c(O2) |
A. AB. BC. CD. D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com